Clear Sky Science · de
LncRNA P4HA2-AS1 fördert renale interstitielle Fibrose über TRIM32-vermittelte K63-Ubiquitinierung von ULK1 und autophagische Dysregulation
Warum Nierenvernarbung wichtig ist
Chronische Nierenerkrankung betrifft weltweit Hunderte Millionen Menschen und schreitet oft still voran, bis Dialyse oder Transplantation die einzigen Überlebensmöglichkeiten sind. Im Zentrum dieses Funktionsverlusts steht ein Prozess, der Vernarbung genannt wird: normales Nierengewebe wird allmählich durch starres, nicht funktionsfähiges Material ersetzt. Die Studie stellt eine einfache, aber entscheidende Frage: Welche molekularen Schalter in Nierenzellen treiben sie in Richtung dieser schädlichen Vernarbung, und lassen sich diese Schalter wieder umlegen?
Ein versteckter RNA‑Schalter in Nierenzellen
Unsere Nieren filtern das Blut mithilfe komplexer Netzwerke winziger Tubuli. Werden diese Tubuli durch Harnabflussstörungen, hohen Blutzucker oder plötzlichen Blutverlust geschädigt, antworten sie mit Ablagerung von Narbengewebe zwischen den Zellen. Die Forschenden untersuchten die Nieren von Mäusen mit verschiedenen Verletzungsformen und verglichen sie per RNA‑Sequenzierung — einer Methode, die abliest, welche Gene aktiviert sind — mit gesunden Nieren. Sie entdeckten ein wenig bekanntes Molekül namens P4HA2‑AS1, eine lange nicht kodierende RNA, die kein Protein produziert und in geschädigten, narbenbildenden Nieren sowie in im Labor gestressten menschlichen Nierenzellen konstant erhöht war. Diese RNA fand sich hauptsächlich im zytosolischen, flüssigkeitsgefüllten Bereich der Zellen, was darauf hindeutet, dass sie dort andere Proteine steuern könnte. 
Die RNA herunterregeln, um die Niere zu schützen
Um zu prüfen, ob P4HA2‑AS1 nur ein Beiwerk oder ein aktiver Treiber der Schädigung ist, verringerten die Forschenden deren Menge in Mäusen und in kultivierten menschlichen Nierenzellen. In einem etablierten Mausmodell, bei dem ein Harnleiter zu einer langfristigen Obstruktion gebunden wird, milderte die gezielte virale Reduktion dieser RNA viele Kennzeichen der Vernarbung: Tubuli blieben intakter, es gab weniger Kollagen und andere Narbenproteine im Interstitium, und die Blutwerte zur Nierenfunktion verbesserten sich. In Kulturen menschlicher Nierenzellen reduzierte die Verminderung von P4HA2‑AS1 auch die Reaktion auf ein starkes narbenbildendes Signal, TGF‑β, sodass weniger Fibronectin, Kollagen und andere pro‑fibrotische Faktoren produziert wurden. Diese Experimente zeigten, dass die RNA nicht nur ein Marker der Schädigung ist, sondern aktiv den Vernarbungsprozess antreibt.
Autophagie: von Reinigung bis Schaden
Die Forschenden fragten dann, wie diese RNA Schaden verursacht. Ihre Genexpressions‑ und Bildgebungsdaten deuteten auf die Autophagie hin, das zelluläre Recyclingsystem, das abgenutzte Proteine und Organellen abbaut. Unter normalen Bedingungen ist Autophagie ein gesundes Haushaltsprogramm, doch wird sie sie zu stark und zu lange aktiviert, kann sie verletzte Nieren in eine maladaptive Reparatur und zur Vernarbung treiben. In gestressten Nierenzellen erhöhte P4HA2‑AS1 den Fluss durch die Autophagie und führte zu einer Anhäufung von Recyclingvesikeln. Wurde die RNA blockiert, normalisierte sich diese übermäßige Recyclingaktivität wieder, sowohl in Zellen als auch in Nieren von obstruierten Mäusen. Mäuse ohne ULK1, ein zentrales Initiationsenzym der Autophagie, waren ebenfalls vor Vernarbung geschützt; in diesen Tieren konnte eine Überexpression von P4HA2‑AS1 den Schaden nicht mehr verschlimmern, was die Verbindung der RNA‑Effekte mit diesem Weg bestätigte.
Eine dreiteilige molekulare Kette
Bei tiefergehenden Untersuchungen nutzte das Team biochemische ‚Angeltechniken‘, um Proteine zu identifizieren, die physisch an P4HA2‑AS1 binden. Eines stach hervor: TRIM32, ein Enzym, das andere Proteine mit kleinen molekularen „Flaggen“ namens Ubiquitin versieht. Die RNA bindet an TRIM32 und schützt es davor, abgebaut zu werden, wodurch seine Konzentration in Nierenzellen steigt. Das stabilisierte TRIM32 wiederum hängt an ULK1 eine spezifische Ubiquitinkette vom K63‑Typ. Anstatt ULK1 zur Zerstörung zu markieren, wirkt diese Kette wie eine Leistungssteigerung und erhöht ULK1s Fähigkeit, Autophagie auszulösen. Entfernten die Wissenschaftler TRIM32 in Mäusen oder schalteten es in Nierenzellen stumm, nahmen sowohl die Vernarbung als auch die übermäßige Autophagie ab. Die Wiedereinführung von TRIM32 in Zellen, in denen P4HA2‑AS1 blockiert war, stellte die narbenbildende Reaktion teilweise wieder her und zeigte, dass dieses Enzym eine zentrale Mittlerrolle in der Kette einnimmt. 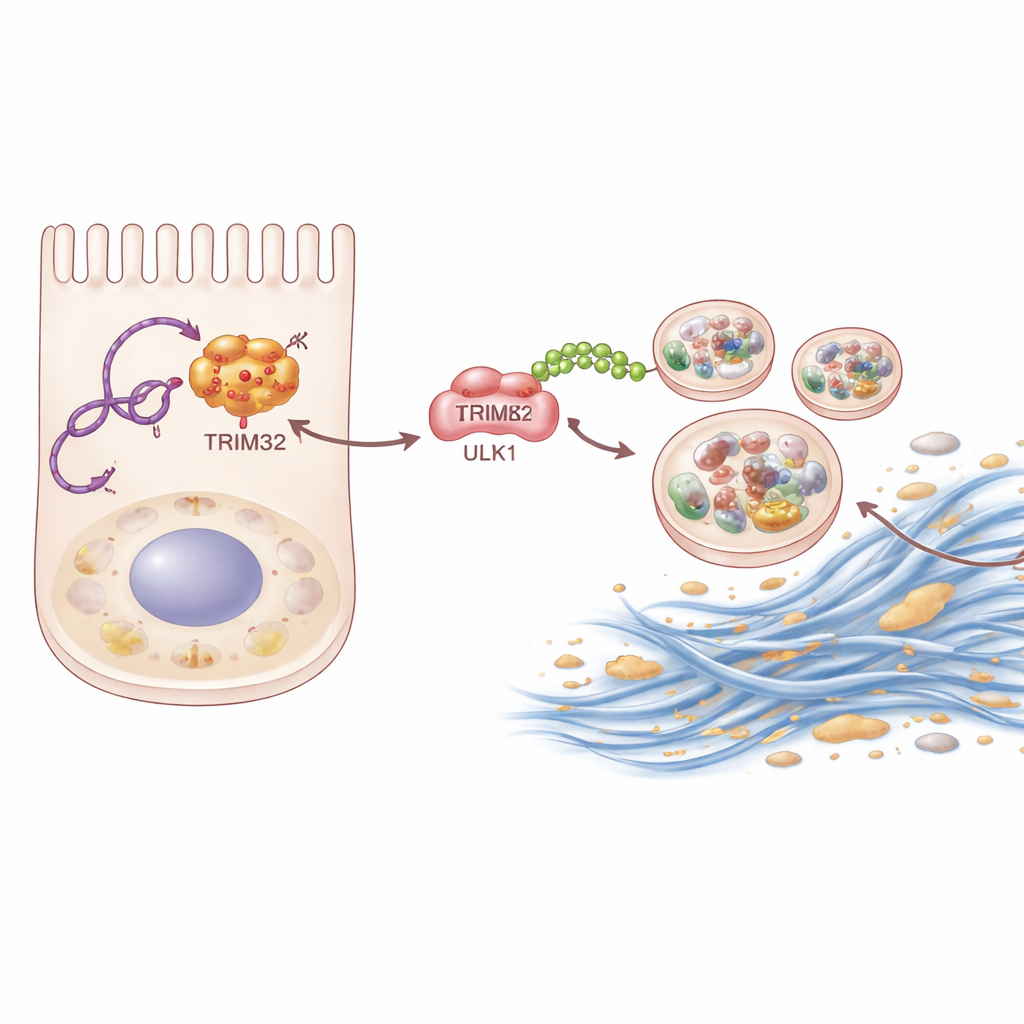
Neue Wege zu weicheren Nieren
In der Summe offenbart die Arbeit eine bislang unbekannte molekulare Route, die lange nicht‑kodierende RNA, Protein‑Markierung und zelluläres Recycling mit dem Aufbau von Nierennarbengewebe verbindet. In verletzten Nieren steigt P4HA2‑AS1 an, stabilisiert TRIM32, aktiviert ULK1 übermäßig und treibt die Autophagie über ihr nützliches Maß hinaus, was letztlich zur Ansammlung fibrotischer Proteine und zum Funktionsverlust führt. Für Nicht‑Spezialisten lautet die Kernbotschaft: Nierenvernarbung ist kein unvermeidliches schwarzes Loch — sie wird von identifizierbaren Schaltern gesteuert, die potenziell medikamentös angreifbar sind. Die Zielsetzung der P4HA2‑AS1–TRIM32–ULK1‑Achse — durch Senken der abtrünnigen RNA, Dämpfung von TRIM32 oder Feinabstimmung von ULK1‑Aktivität — könnte eines Tages neue Behandlungsansätze bieten, um das Fortschreiten der chronischen Nierenerkrankung zu verlangsamen oder zu verhindern.
Zitation: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Schlüsselwörter: chronische Nierenerkrankung, renale Fibrose, Autophagie, lange nicht-kodierende RNA, Nierentubuli