Clear Sky Science · de
Reverse-Transkriptase-Inhibitoren ermöglichen die Erzeugung fruchtbarer Spermatiden aus fetalen Maus-Hoden in vitro
Frühe Keimzellen in funktionsfähige Spermien verwandeln
Behandlungen von Unfruchtbarkeit und Grundlagenforschung beruhen gleichermaßen darauf, zu verstehen, wie unreife Keimzellen im Hoden zu Spermien werden. Diese Studie zeigt, dass es jetzt möglich ist, sehr frühe fetale Maus-Hoden, entnommen kurz nachdem das Geschlecht des Embryos festgelegt ist, vollständig in einer Kultur durch diese Umwandlung zu führen. Durch sorgfältiges Abstimmen der chemischen Umgebung und des Sauerstoffniveaus erzeugten die Forschenden nicht nur reife spermienähnliche Zellen, sondern nutzten diese auch zur Erzeugung gesunder, fruchtbarer Nachkommen.
Warum frühe Hodenentwicklung schwer nachzubilden ist
Spermien außerhalb des Körpers zu erzeugen wurde bereits mit Hodengewebe von Neugeborenen oder älteren Mäusen erreicht, die Effizienz war jedoch gering, und Versuche mit deutlich früherem fetalem Gewebe schlugen weitgehend fehl. In diesem frühen Stadium baut der Hoden noch seine innere Architektur auf, und Keimzellen durchlaufen tiefgreifende Veränderungen in der Verpackung und Markierung ihrer DNA. Diese komplexe Choreographie in einer Kultur nachzubilden ist herausfordernd, und frühere Kulturen kamen bei Hoden, die um Embryonaltag 12,5 gesammelt wurden — kurz nach Festlegung des Geschlechts — selten über die frühen Schritte hinaus.
Antivirale Medikamente ausleihen, um sich entwickelnde Zellen zu schützen
Das Team konzentrierte sich auf ein verborgenes Hindernis: mobile DNA-Elemente, sogenannte Retrotransposons, die sich kopieren und an neuen Stellen im Genom einfügen können. In normalen Hodengeweben im Körper werden diese Elemente besonders in Keimzellen streng kontrolliert. In Kultur allerdings stellten die Autorinnen und Autoren fest, dass die Aktivität von Retrotransposons deutlich höher war, während die zelleigenen Abwehrgene leiser blieben. Dieses Ungleichgewicht korrelierte mit schlechter Spermienentwicklung. Da Retrotransposons eine Reverse-Transkriptase-Enzym nutzen, ähnlich wie manche Viren, testeten die Forschenden mehrere ursprünglich als Reverse-Transkriptase-Inhibitoren entwickelte Medikamente. Eine spezifische Dreifach-Kombination, bezeichnet AEC, verdoppelte etwa den Anteil spermatogener Zellen und vervielfachte bei kultivierten neugeborenen Hoden den Anteil haploider, spermienähnlicher Zellen gegenüber unbehandelten Kontrollen.
Von winzigen fetalen Hoden zu funktionellen Spermien
Mit diesem Arzneimittelcocktail wandten sich die Wissenschaftler den fetalen Hoden zu. In Gewebe, das kurz vor der Geburt entnommen wurde, förderten die Inhibitoren das Auftreten fortgeschrittener Spermatiden. Bemerkenswerter noch: Als sie Hoden von Embryonen am Tag 12,5 kultivierten — ein Stadium, das zuvor noch nie gezeigt worden war, vollständig in vitro zu spermatogenisieren — konnten sie nun runde und gestreckte Spermatiden erzeugen. Die größten Fortschritte erzielten sie, wenn sie die Inhibitoren mit einer sauerstoffarmen Atmosphäre kombinierten, die die Bedingungen im sich entwickelnden Körper besser nachahmt. Unter diesen hypoxischen Bedingungen zeigte etwa ein Drittel der Gewebeareale Marker fortgeschrittener Keimzellreifung, und Spermien mit Schwänzen konnten aus den Kulturen gewonnen werden.
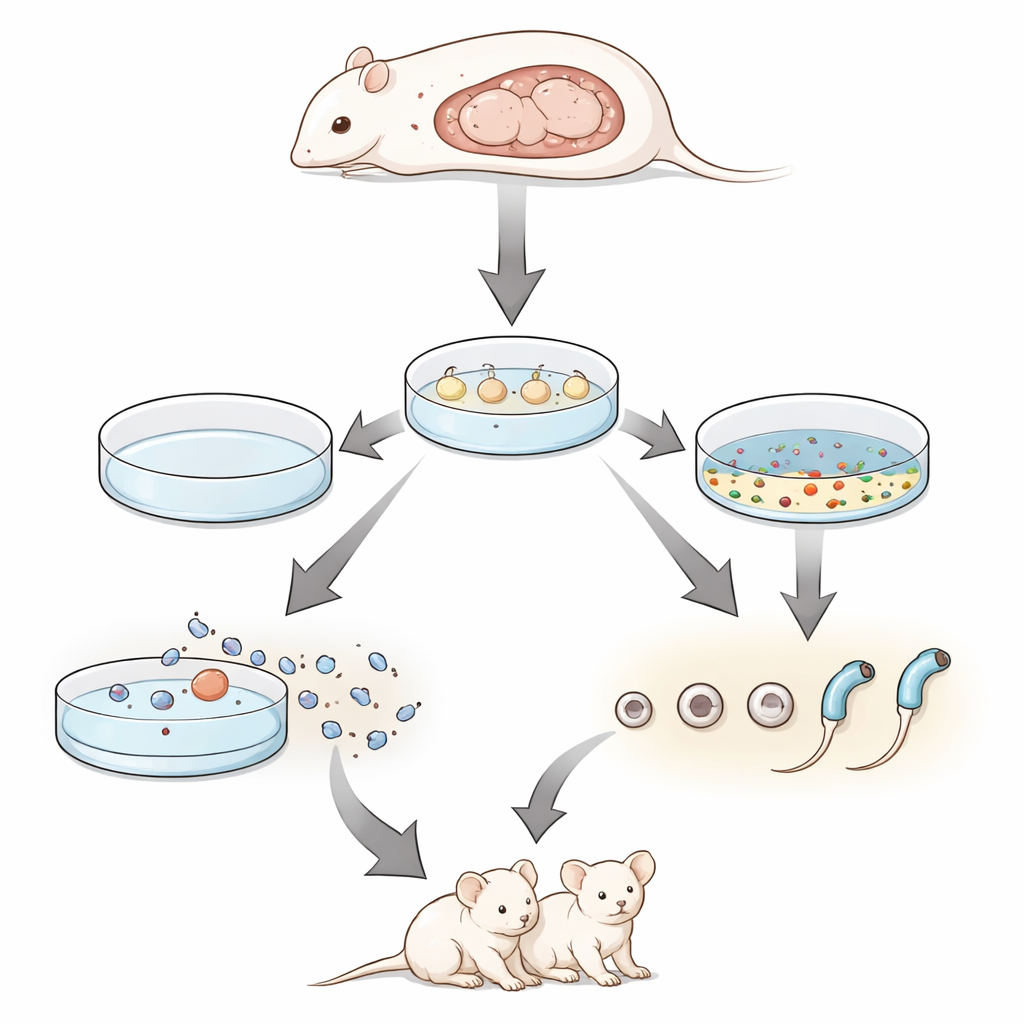
Prüfung, ob im Labor erzeugte Spermatiden wirklich funktionieren
Um herauszufinden, ob diese in vitro gewonnenen Zellen tatsächlich funktional waren, verwendete das Team eine Technik namens Round-Spermatid-Injektion. Sie isolierten runde Spermatiden aus den kultivierten fetalen Hoden und injizierten sie in Mäuseeizellen, die sanft aktiviert worden waren. Die entstehenden Embryonen wurden in Ammentiere übertragen. Aus nur zwei kultivierten Hodenstücken ergab das Verfahren mehrere lebende Junge, von denen viele ein fluoreszierendes Markergen trugen, das ihre Herkunft aus der Kultur bestätigte. Als diese Tiere der ersten Generation sich paaren durften, brachten sie normal große Würfe gesunder Nachkommen der zweiten Generation zur Welt, was demonstriert, dass die im Labor erzeugten Spermatiden nicht nur die Entwicklung bis zur Geburt unterstützen, sondern auch volle Fruchtbarkeit ermöglichen.
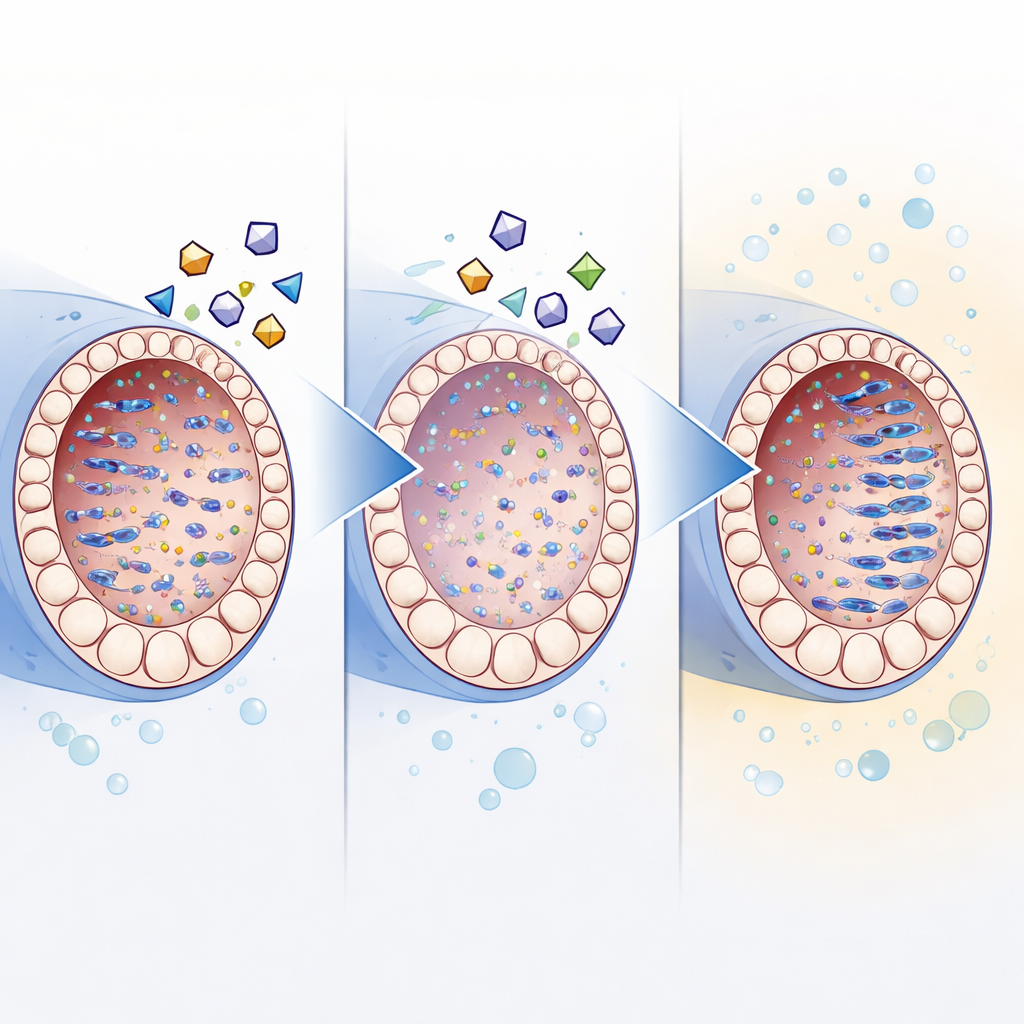
Wie das Blockieren mobiler DNA künftige Therapien ermöglichen könnte
Weitere Experimente stützten die Idee, dass Reverse-Transkriptase-Inhibitoren hauptsächlich dadurch helfen, mobile DNA in Schach zu halten. Im Vergleich zu altersentsprechenden Hoden im Körper zeigten kultivierte Hoden höhere Spiegel von Retrotransposon-Proteinen und zusätzliche Kopien ihrer DNA sowie eine reduzierte Expression der natürlichen Stummschaltungsmaschinerie der Zellen. Das Hinzufügen des Inhibitor-Cocktails verringerte diese Anhäufung und verbesserte gleichzeitig die Reifung der Keimzellen. Obwohl die Medikamente das Gewebewachstum insgesamt leicht verlangsamten, verbesserten Versuche, dies mit serum-basierten Zusätzen auszugleichen, die Spermienausbeute nicht, was darauf hindeutet, dass Wachstum und richtige Differenzierung sorgfältig ausbalanciert werden müssen.
Was das für die Reproduktionsforschung bedeutet
Diese Arbeit zeigt, dass sehr unreife fetale Hoden bereits alle Zutaten enthalten, die nötig sind, um eine funktionierende Spermienproduktion aufzubauen, vorausgesetzt, die Umgebung schützt ihr Genom und ahmt Schlüsselaspekte des Lebens in der Gebärmutter nach. Durch die Kombination antiviraler Wirkstoffe mit niedrigem Sauerstoff schufen die Forschenden ein Kultursystem, das die vollständige Spermatogenese aus einem der frühesten bisher getesteten Stadien nachbildet und Nachkommen hervorbringt, die normal wachsen und sich fortpflanzen. Obwohl die Studie an Mäusen durchgeführt wurde und klinisch noch weit entfernt ist, eröffnet sie ein starkes Fenster in die frühesten Schritte der Entwicklung männlicher Keimzellen und liefert Hinweise, die eines Tages helfen könnten, die Fruchtbarkeit von Patienten zu erhalten oder wiederherzustellen, deren Fortpflanzungszellen früh im Leben geschädigt wurden.
Zitation: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Schlüsselwörter: in vitro Spermatogenese, fetale Hoden-Kultur, Reverse-Transkriptase-Inhibitoren, Retrotransposons, männliche Fruchtbarkeit