Clear Sky Science · de
Adipositas beeinträchtigt die Spermatogenese durch Leydig‑Zell‑Ferroptose, induziert von leberabgeleitetem exosomalem miR-122-5p
Warum Gewicht und Fruchtbarkeit zusammenhängen
Adipositas wird meist im Zusammenhang mit Herzkrankheiten und Diabetes diskutiert, kann aber auch schleichend die männliche Fruchtbarkeit untergraben. Diese Studie an Mäusen legt einen überraschenden Mechanismus dar, wie eine fettreiche Ernährung Testosteron senken und die Spermienproduktion schädigen kann: die Leber sendet winzige „Botenbläschen“ ins Blut, die in den hormonproduzierenden Zellen des Hodens eine besondere Form des Zelltods auslösen. Das Verständnis dieser versteckten Leber‑zu‑Hoden‑Kommunikation kann erklären, warum übergewichtige Männer häufig unter niedrigem Testosteron und Unfruchtbarkeit leiden, und auf neue Therapieansätze hinweisen.
Verborgene Post zwischen Organen
Unsere Organe kommunizieren ständig miteinander über Hormone und andere chemische Botenstoffe. Eine Form dieser Kommunikation nutzt Exosomen — nanometergroße Bläschen, die von Zellen freigesetzt werden und Lipide, Proteine sowie genetisches Material transportieren. Die Forscher arbeiteten mit Mäusen, die entweder eine normale oder eine fettreiche Diät erhielten, die zu Adipositas, Insulinresistenz und gestörter Blutzuckerregulation führte. Adipöse Mäuse hatten kleinere, weniger aktive Hoden: Spermienzahl, Testosteronspiegel sowie Größe und Anzahl der spermienproduzierenden Tubuli waren verringert. Bei der Untersuchung wichtiger Zellmarker im Hoden fanden sich weniger testosteronproduzierende Leydig‑Zellen sowie weniger frühe und späte Spermienzellen, was bestätigt, dass die gesamte Spermatogenese beeinträchtigt war. 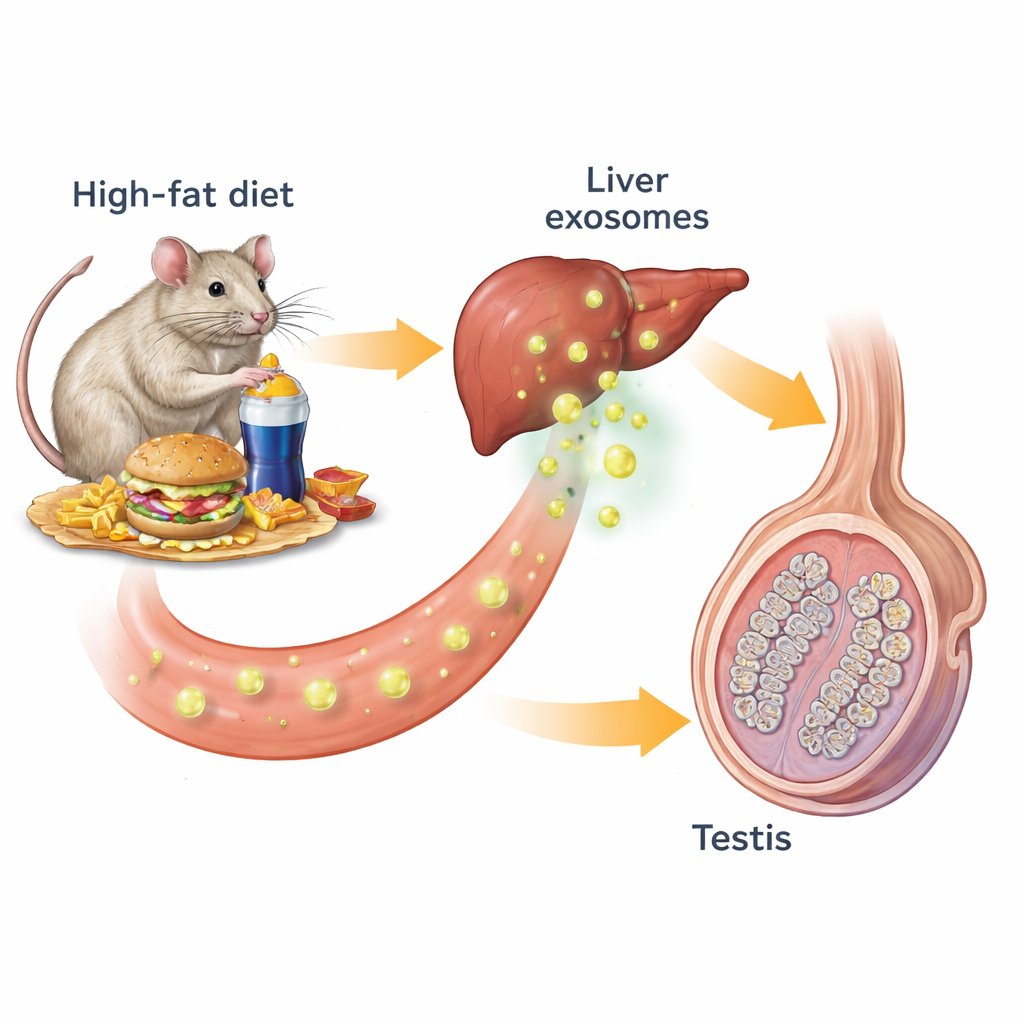
Exosomen verbreiten den Schaden
Um zu testen, ob zirkulierende Exosomen an dieser Schädigung beteiligt sind, reinigten die Wissenschaftler Exosomen aus dem Blut von adipösen und schlanken Mäusen. Die Injektion von Exosomen aus adipösen Mäusen in gesunde, schlanke Empfänger war ausreichend, um viele der Probleme zu reproduzieren: Die Empfänger zeigten Anzeichen metabolischer Störungen, ihr Testosteron sank, und Spermienzahl sowie Hodengewebe verschlechterten sich. Die Hemmung der Exosomenfreisetzung bei adipösen Mäusen mit dem Wirkstoff GW4869 kehrte diese Veränderungen weitgehend um und stellte Spermienzahl, Testosteron und normale Hodenarchitektur wieder her. Diese Ergebnisse zeigen, dass zirkulierende Exosomen nicht nur Statisten sind, sondern aktiv schädliche Signale der Adipositas zum Reproduktionssystem transportieren.
Eine toxische Form des Zelltods
Das Team untersuchte dann, was die Exosomen genau in Leydig‑Zellen bewirken. Sie konzentrierten sich auf Ferroptose, eine eisengetriebene Form des Zelltods, gekennzeichnet durch Eisenakkumulation, oxidative Schädigung von Lipiden und geschädigte Mitochondrien — die Kraftwerke der Zelle. In adipösen Mäusen und in gesunden Mäusen, die Exosomen aus adipösen Tieren erhalten hatten, zeigten die Hoden erhöhte Eisen‑ und Malondialdehyd‑Spiegel (ein Nebenprodukt von Lipidoxidation) sowie deutliche mitochondriale Schäden im Elektronenmikroskop. Die Behandlung adipöser Mäuse mit einem Ferroptose‑Hemmer, Ferrostatin‑1, schützte Leydig‑Zellen, erhöhte Testosteron und Spermienzahl und verbesserte die mitochondriale Gesundheit. In Zellkulturen schützte dasselbe Mittel isolierte Leydig‑Zellen vor durch Exosomen aus adipösen Tieren induziertem Zelltod und oxidativem Stress. Zusammen zeigen diese Experimente, dass Ferroptose ein zentraler Zusammenhang zwischen Adipositas und versagender Testosteronproduktion ist.
Die Botschaft der Leber und der SCD2‑Schalter
Um die Botschaft innerhalb der Exosomen zu identifizieren, sequenzierten die Forscher deren kleine RNA‑Fracht und fanden, dass ein bestimmtes microRNA, miR‑122‑5p, in Exosomen adipöser Mäuse stark erhöht war. Dieses microRNA war besonders in der Leber und in leberabgeleiteten Exosomen reichlich vertreten, und diese Leber‑Exosomen konnten auf dem Weg zu den Hoden nachverfolgt werden. Als die miR‑122‑5p‑Spiegel experimentell in Exosomen gesenkt wurden, waren Leydig‑Zellen weniger anfällig für Ferroptose und die Testosteronproduktion verbesserte sich, obwohl die Tiere metabolisch weiterhin beeinträchtigt waren. Weitere Tests zeigten, dass miR‑122‑5p direkt das Gen Scd2 herunterreguliert, das dabei hilft, bestimmte Fette in Formen umzuwandeln, die Zellen vor oxidativen Schäden schützen. Die Verminderung von Scd2 in Leydig‑Zellen machte sie anfälliger für Ferroptose und senkte das Testosteron, während die Erhöhung von Scd2 in adipösen Mäusen die Hormonspiegel, die Spermienproduktion und die mitochondriale Struktur teilweise wiederherstellte. 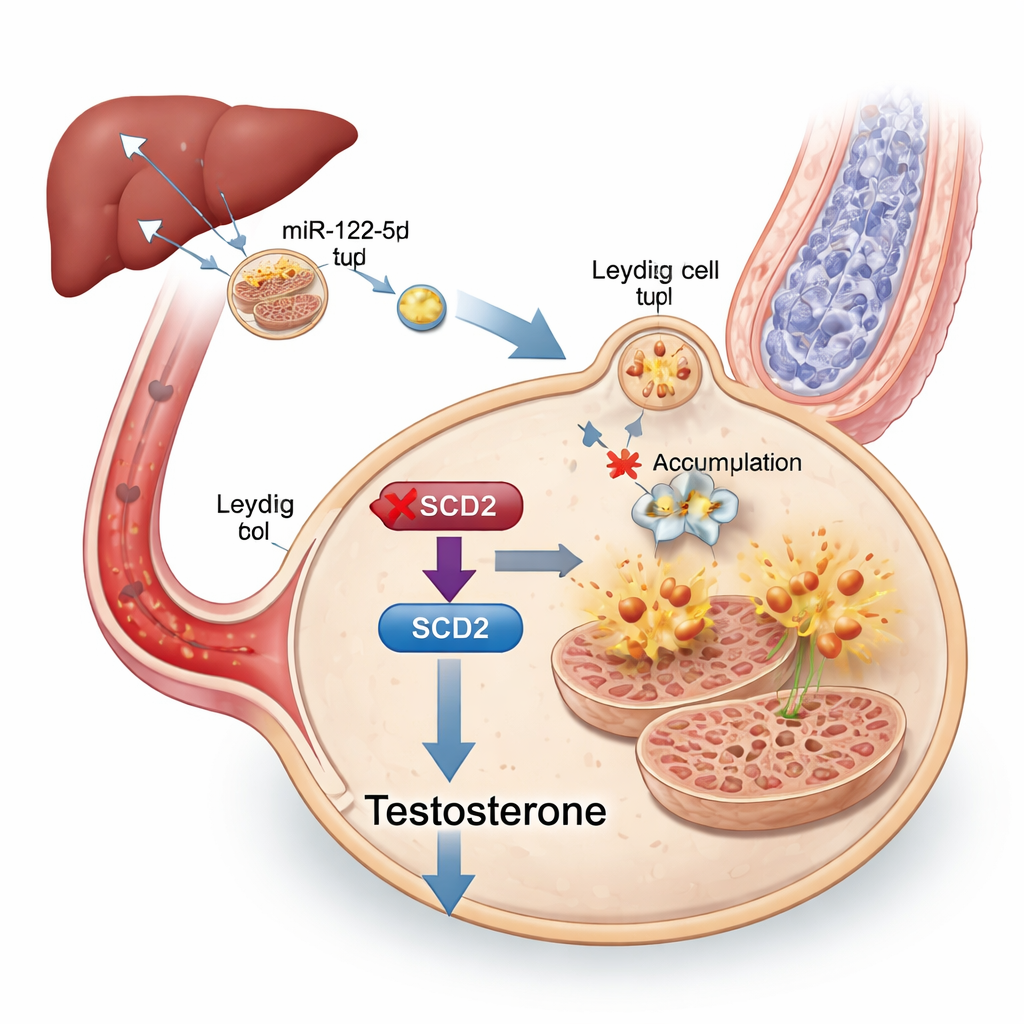
Was das für die menschliche Gesundheit bedeutet
Kurz gesagt zeigt diese Arbeit, dass eine fettreiche Ernährung die Leber dazu veranlassen kann, Exosomen mit einem Übermaß an miR‑122‑5p zu beladen. Diese Exosomen reisen durch das Blut zu den Hoden, wo das microRNA in Leydig‑Zellen den Scd2‑„Fettverarbeitungs“‑Schalter ausschaltet. Ohne Scd2 sammeln sich eisenbedingte oxidative Schäden an, die Zellen unterliegen Ferroptose, produzieren weniger Testosteron und unterstützen letztlich weniger gesunde Spermien. Obwohl diese Forschung an Mäusen durchgeführt wurde und noch beim Menschen bestätigt werden muss, identifiziert sie leberabgeleitete Exosomen, miR‑122‑5p, Ferroptose und Scd2 als vielversprechende Biomarker und potenzielle Arzneimittelziele zur Behandlung von adipositasbedingter männlicher Unfruchtbarkeit — und unterstreicht einen weiteren Grund, warum langfristig fettreiche Ernährungsweisen die reproduktive Gesundheit schleichend schädigen können.
Zitation: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Schlüsselwörter: Adipositas und männliche Fruchtbarkeit, Testosteron, Exosomen, Leydig‑Zellen, Ferroptose