Clear Sky Science · de
Zwei‑in‑einem-Protein‑Tag ermöglicht lösliche Expression und Calcium‑abhängige Aufreinigung von Einzelketten‑Antikörperfragmenten
Mächtige Antikörper leichter herstellbar machen
Moderne Medikamente basieren zunehmend auf Antikörperfragmenten — kleinen, präzisen „Lenkgeschossen“, die Krebszellen, entzündete Gewebe oder krankheitsverursachende Moleküle gezielt ansteuern können. Dennoch sind diese vielversprechenden Wirkstoffe überraschend schwer herzustellen: In bakteriellen Produktionssystemen neigen sie zum Verklumpen, Fehlfalten und sind schwer mit Standardverfahren zu reinigen. Diese Studie beschreibt einen neuen Protein‑Anhänger, genannt CSQ‑Tag, der beide Probleme gleichzeitig angeht und diese Fragmente in einfacher, kostengünstiger Weise besser produzier‑ und aufreinigbar macht.
Warum verkleinerte Antikörper wichtig sind
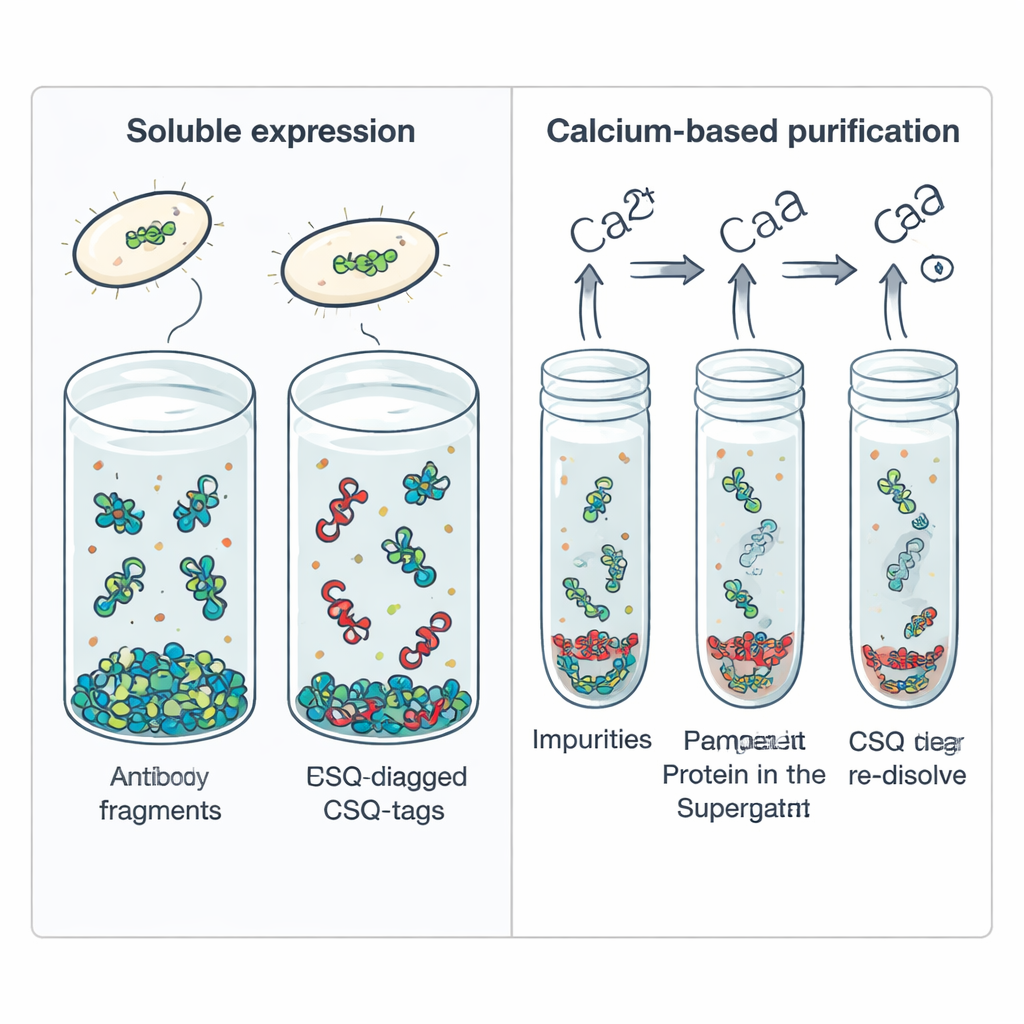
Vollständige Antikörper haben die Behandlung von Krebs, Autoimmunerkrankungen und Augenleiden revolutioniert, doch ihre große Größe und komplexe Struktur bringen Nachteile mit sich. Sie werden langsam aus dem Körper eliminiert, dringen unter Umständen schlecht in Tumore oder Gewebe ein und sind teuer in der Produktion. Einzelkettige variablere Fragmente, oder scFvs, behalten nur das wirksame Erkennungsstück eines Antikörpers — die Zielbindende Domäne — und verknüpfen es zu einer einzigen Kette. Diese kompakten Moleküle durchdringen Gewebe leichter und lassen sich zu ausgefeilten Therapeutika und Diagnostika weiterentwickeln. Werden scFvs jedoch in üblichen Bakterien wie Escherichia coli hergestellt, lagern sich viele in unlöslichen Klumpen, sogenannten Einschlusskörpern, ab, und es fehlt oft ein universelles, einfaches Verfahren zur Aufreinigung.
Ein Helfer‑Tag mit doppelter Wirkung
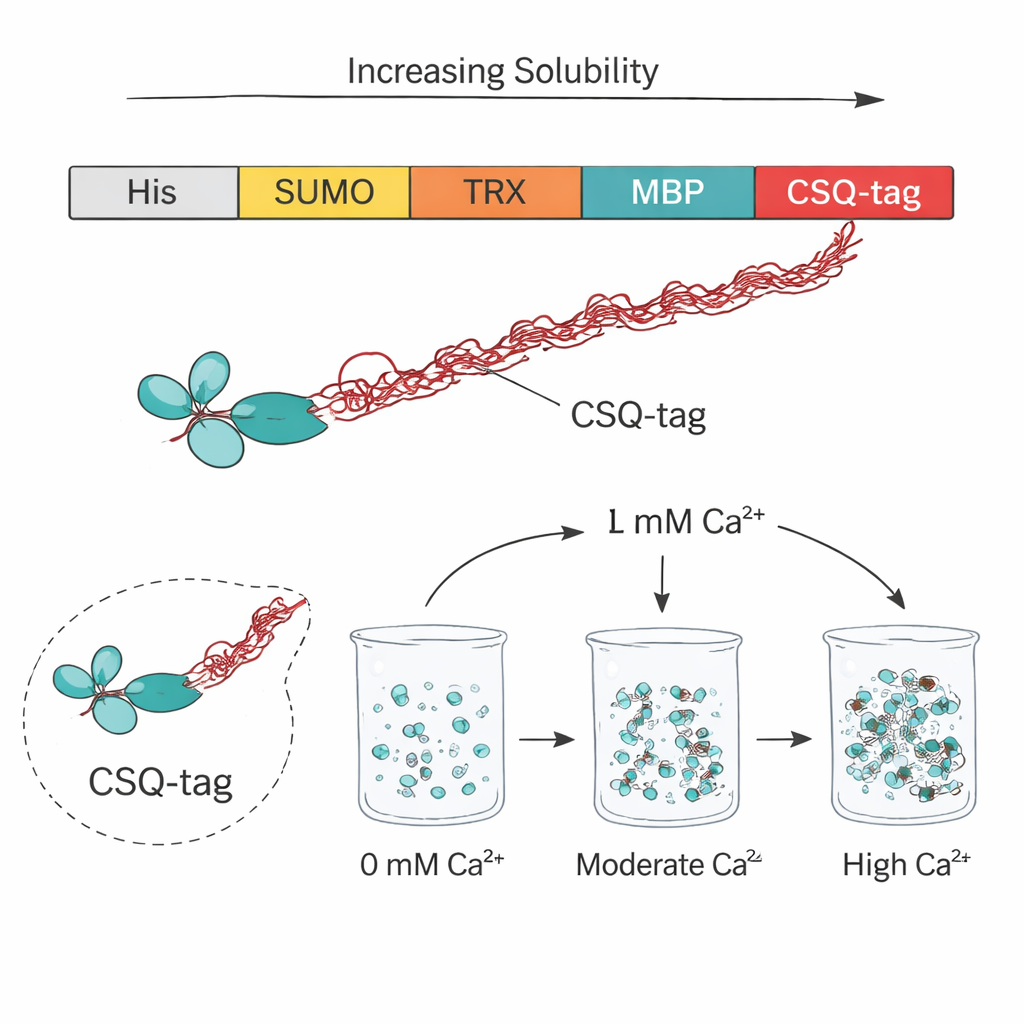
Die Forscher griffen auf Calsequestrin zurück, ein natürliches Calcium‑speicherndes Protein in Muskelzellen, und entwarfen daraus den Hilfs‑Tag CSQ‑Tag. Dieser Tag ist ungewöhnlich sauer und sehr flexibel, mit langen, ungeordneten Bereichen, die wie „entropische Bürsten“ den Raum um das angehängte Protein freihalten. Wenn er an vier verschiedene therapeutische scFvs fusioniert wurde, die normalerweise aggregieren, steigerte der CSQ‑Tag deutlich den Anteil, der in Standard‑E. coli‑Zellen gelöst blieb. Während dieselben scFvs mit nur einem einfachen His‑Tag nahezu vollständig unlöslich waren, erreichten die CSQ‑getaggten Varianten eine mittlere Löslichkeit von etwa 84 Prozent — selbst in einem bakteriellen Stamm, der üblicherweise ein chemisch herausforderndes Faltungsumfeld bietet.
Übertrifft etablierte Tag‑Technologien
Um zu prüfen, wie sich der CSQ‑Tag gegenüber gängigen Protein‑Tags behauptet, verglich das Team ihn mit SUMO, Thioredoxin, GST und MBP, die oft verwendet werden, um problematische Proteine in Lösung zu bringen. In diesem direkten Vergleich mit einem anti‑VEGF‑scFv (der Grundlage des Augenmedikaments Brolucizumab) verbesserten nur MBP und CSQ die Löslichkeit deutlich, wobei CSQ klar die beste Leistung zeigte. Über vier verschiedene scFvs erhöhte CSQ die lösliche Produktion um etwa das 1,8‑fache gegenüber MBP, das lange als eine der besten Optionen galt. Weitere Experimente zeigten, dass der sauerste und ungeordnetste Abschnitt der Calsequestrin, bekannt als Domäne 3, für diesen Effekt entscheidend war: Seine Entfernung reduzierte die Löslichkeit stark, was unterstreicht, wie die negative Ladung und die strukturelle Flexibilität des Tags verhindern, dass die Partnerproteine aneinanderhaften.
Calcium als einfacher Reinigungs‑Schalter
Neben der Förderung der Löslichkeit bietet der CSQ‑Tag einen eingebauten Reinigungs‑Trick. Calsequestrin neigt dazu, bei Calciumbindung zu aggregieren und bei Calcium‑Entzug wieder zu dissoziieren. Die Autoren nutzten dieses Verhalten, indem sie einer Zellaufschlämmung mit CSQ‑getaggten scFvs Calcium zufügten, wodurch die getaggten Fusionsproteine ausfielen, während die meisten bakteriellen Verunreinigungen in Lösung blieben. Ein kurzer Zentrifugationsschritt pellete die CSQ‑getaggten Proteine; die Zugabe des Calcium‑chelatierenden Mittels EDTA löste sie anschließend mit hoher Reinheit (über 95 Prozent) wieder auf — ohne teure Chromatographieharze. Dieser calciumgetriebene Phasenübergang ließ sich wiederholen, ohne das Protein zu schädigen, und ist daher attraktiv für die großtechnische Produktion.
Die Wirksamkeit der Arznei bewahren
Für jedes Therapeutikum zählt die erhöhte Produktion nur, wenn das Endprodukt weiterhin wirkt. Nach Einsatz eines üblichen Enzyms zum Entfernen des CSQ‑Tags und einem abschließenden Polierschritt testete das Team das freie anti‑VEGF‑scFv. Es band sein Ziel mit einer Affinität, die im Wesentlichen mit dem zugelassenen Medikament Brolucizumab übereinstimmte, und detaillierte chemische Analysen bestätigten korrekte innere Bindungen und das Fehlen schädlicher Aggregate. Ein zweites, besonders problematisches scFv gegen den CD3‑Rezeptor zeigte eine ähnliche Erhaltung der Aktivität. Die Gesamtausbeuten des CSQ‑Tag‑Prozesses lagen mehrere Male höher als bei traditionellen Umlöseverfahren, während einfachere Ausrüstung und günstigere Reagenzien zum Einsatz kamen.
Was das für künftige Therapien bedeuten könnte
Indem verbesserte Löslichkeit und eine einfache Aufreinigungshilfe in einem einzelnen Tag kombiniert werden, löst das CSQ‑System zwei langjährige Engpässe in der Produktion von Antikörperfragmenten. Es ermöglicht Wirkstoffentwicklern, schnell wachsende, kostengünstige E. coli‑Stämme zu nutzen und dennoch hochwertige scFvs zu erhalten, die ihre Bindekraft behalten. Zwar ist noch etwas Optimierung nötig, insbesondere um Verluste nach der Tag‑Entfernung zu reduzieren, doch könnte dieser calcium‑steuerbare Tag die Herstellung nicht nur von Antikörperfragmenten, sondern auch anderer empfindlicher therapeutischer Proteine vereinfachen. Für Patientinnen und Patienten könnte das langfristig zu einem breiteren Angebot gezielter Biologika führen, die effizienter und kostengünstiger produziert werden.
Zitation: Lee, J., Park, H., Jeong, S. et al. Two-in-one protein tag enables the soluble expression and calcium-dependent purification of single-chain antibody fragments. Commun Biol 9, 326 (2026). https://doi.org/10.1038/s42003-026-09611-0
Schlüsselwörter: Einzelketten‑Antikörperfragmente, Proteinexpression, Calsequestrin‑Tag, Calcium‑abhängige Aufreinigung, therapeutische Antikörper