Clear Sky Science · de
Histon-Demethylase KDM7A reguliert die fibrotische Makrophagen-Polarisation und das Fortschreiten der Lungenfibrose negativ
Warum vernarbte Lungen uns alle betreffen
Wenn die Lunge hartnäckige Narben bildet, wird Atmen zur täglichen Belastung. Dieser Zustand, bekannt als Lungenfibrose, betrifft Millionen Menschen und ist derzeit nicht heilbar — es gibt nur Medikamente, die das Fortschreiten verlangsamen. In dieser Studie entdecken Forschende eine zuvor verborgene molekulare „Bremse“ in Immunzellen namens Makrophagen, die hilft, die Vernarbung der Lunge in Schach zu halten. Das Verständnis dieser Bremse könnte neue Behandlungsansätze eröffnen — nicht nur für Lungenfibrose, sondern möglicherweise auch für andere Erkrankungen, bei denen schädliche Vernarbung und unkontrollierte Entzündung zusammen auftreten.
Eine Geschichte formwandelnder Immunzellen
Makrophagen sind vorderste Immunzellen, die Gewebe überwachen, Trümmer entfernen und bei der Reparatur helfen. Sie sind aber auch Gestaltwandler: In manchen Situationen werden sie zu pro-inflammatorischen Kämpfern, in anderen zu Wundheilern, die Narbenbildung fördern können. Ein besonders narbenfördernder Typ, sogenannte profibrotische Makrophagen (Fib-Mac), steht in engem Zusammenhang mit Lungenfibrose. Diese Zellen produzieren Moleküle, die Fibroblasten aktivieren, welche daraufhin übermäßig Kollagen und andere Matrixbestandteile ablagern und so die Lunge langsam versteifen. Die Autorinnen und Autoren wollten wissen, wie die genetischen „Einstellungen“ in Makrophagen entscheiden, ob sie zu diesen gefährlichen Fib-Mac-Zellen werden oder in ausgeglicheneren, schützenden Zuständen bleiben.
Eine epigenetische Bremse im Genom
Das Team begann mit dem Durchforsten hunderter bekannter epigenetischer Regulatoren — Proteine, die feinjustieren, wie eng DNA verpackt ist und welche Gene an- oder abgeschaltet werden. Mittels RNA-Sequenzierung in menschlichen und Maus-Makrophagen fanden sie, dass ein Enzym namens KDM7A stark hochreguliert wurde, wenn Makrophagen in einen fibrotischen, wundeheilungsartigen Zustand gedrängt wurden. KDM7A ist eine „Histon-Demethylase“: sie entfernt bestimmte chemische Markierungen von Histonproteinen, um die DNA gewickelt ist. Dieses Muster deutete darauf hin, dass KDM7A als eingebauter Rückkopplungsbremsmechanismus wirken könnte, der genau dann aktiviert wird, wenn Makrophagen beginnen, in eine narbenfördernde Identität abzudriften.
Um das zu prüfen, setzten die Forschenden Mäuse ohne das Gen Kdm7a ein und lösten mit dem Chemotherapeutikum Bleomycin eine Lungenschädigung aus — ein Standardmodell der Lungenfibrose. Kurz nach der Verletzung sah das Lungengewebe bei normalen und Kdm7a-defizienten Tieren ähnlich aus. Nach drei Wochen zeigten die Mäuse ohne Kdm7a jedoch deutlich ausgeprägtere Vernarbungen, Kollaps der kleinen Lufthalten und höhere „Ashcroft“-Werte, die Fibrose quantifizieren. Gene, die an der Kollagenproduktion und anderen fibrotischen Wegen beteiligt sind, waren in diesen Knockout-Mäusen stärker aktiv, was bestätigt, dass der Verlust von Kdm7a die Lunge anfälliger für anhaltende, schädliche Narbenbildung macht.
Wie KDM7A Makrophagen von einer narbenfördernden Schicksalsbestimmung ablenkt
Mittels Einzelzell-RNA-Sequenzierung zoomten die Autorinnen und Autoren auf einzelne Lungenzellen verletzter Mäuse hinein. Sie entdeckten, dass ohne Kdm7a eine bestimmte Makrophagen-Untergruppe im stützenden Lungengewebe dramatisch expandierte und ein starkes Fib-Mac-Signaturbild annahm, mit Expression von Genen wie Arg1, Spp1 und Trem2. Weitere Experimente in kultivierten Makrophagen zeigten, dass das Entfernen von Kdm7a Fib-Mac-Marker-Gene verstärkte und den Stoffwechsel der Zellen in Richtungen umlenkte, die Kollagenproduktion und anhaltende Aktivierung unterstützen. Anders gesagt: KDM7A bremst normalerweise sowohl die genetischen als auch die metabolischen Programme, die Makrophagen in einen fibrosefördernden Zustand treiben.
Bei tiefer gehenden Untersuchungen identifizierten die Forschenden einen zentralen Partner dieses Bremssystems: das Sensorsignalprotein TLR8, das RNA-Bruchstücke in Immunzellen erkennt. Sie fanden heraus, dass KDM7A dabei hilft, das Gen Tlr8 eingeschaltet zu halten, indem es eine repressive chemische Markierung (H3K27me2) an einem Enhancer in der Nähe von Tlr8 entfernt. Wenn Kdm7a abgeschaltet war, häufte sich diese Markierung, Tlr8-Spiegel sanken und Fib-Mac-Merkmale intensivierten sich. Auch eine direkte Reduktion von Tlr8 in Makrophagen trieb diese in Richtung einer fibrotischen Identität, während die Aktivierung oder Überexpression von TLR8 sie zurückzog — selbst wenn Kdm7a fehlte. Das ordnet den KDM7A–TLR8-Weg in die Mitte eines molekularen Schaltkreises ein, der die Lunge vor übermäßiger Vernarbung schützt.
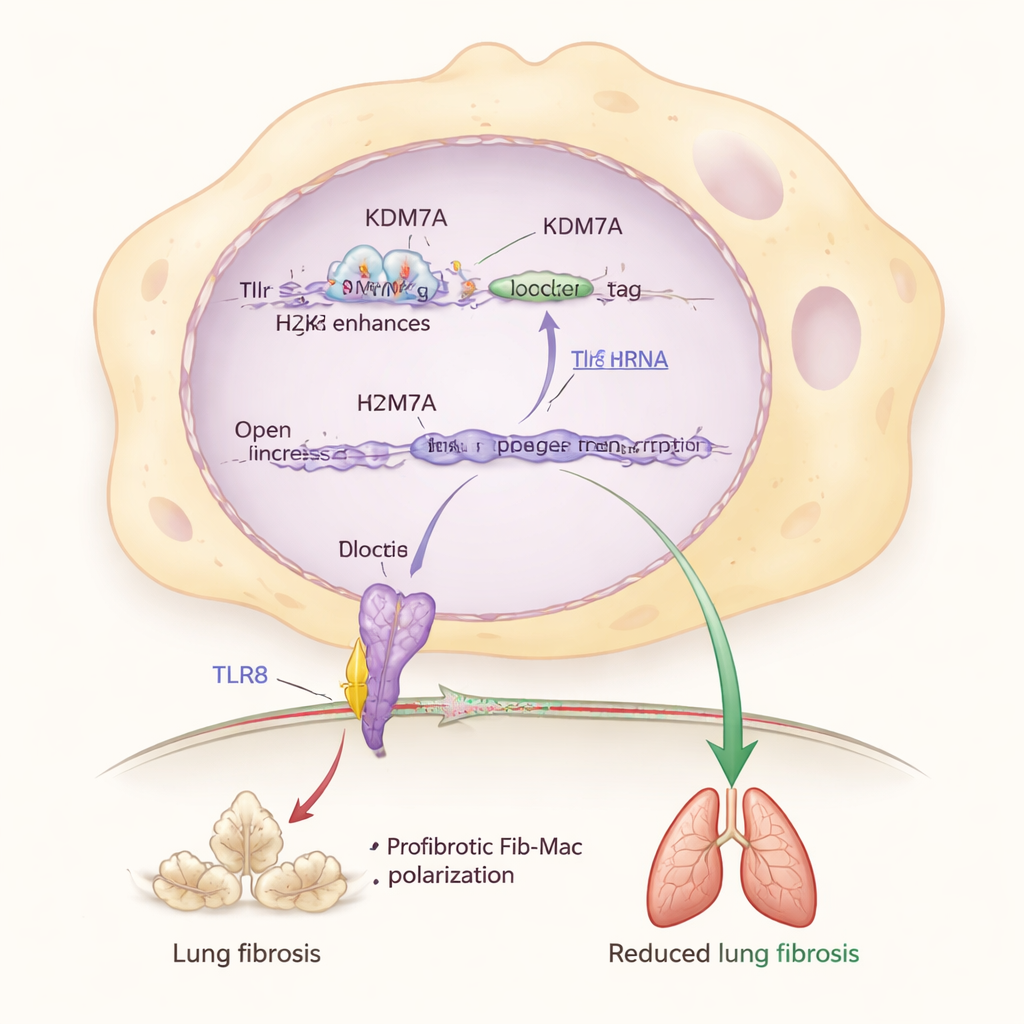
Von alternden Lungen bis zur menschlichen Krankheit
Um die Befunde auf den Menschen zu beziehen, untersuchte das Team Lungengewebe von Patientinnen und Patienten mit fibrotischer Lungenerkrankung. Im Vergleich zu nicht erkranktem Kontrollgewebe enthielten fibrotische Lungen deutlich mehr Makrophagen mit Fib-Mac-Markern, doch diese Zellen zeigten gleichzeitig merklich reduzierte KDM7A- und TLR8-Spiegel. Die Reanalyse vorhandener Einzelzell-Datensätze von Patientinnen und Patienten mit idiopathischer Lungenfibrose bestätigte dieses Muster: Mit steigendem Fib-Mac-Signaturlevel fiel die KDM7A-Expression. Die Forschenden durchsuchten außerdem ein großes Maus-Atlas-Dataset und fanden, dass die Expression von Kdm7a und Tlr8 in Makrophagen mit dem Alter bei Männchen abnahm, was das höhere Risiko für Lungenfibrose bei älteren Männern widerspiegelt. Das deutet darauf hin, dass die alters- und geschlechtsbedingte Abschwächung der KDM7A–TLR8-Bremse mit erklären könnte, wer besonders anfällig für schwere Lungenvernarbung ist.
Was das für zukünftige Therapien bedeutet
Kurz gesagt zeigt diese Arbeit, dass unser Immunsystem einen internen Sicherheitsmechanismus besitzt, der verhindert, dass hilfreiche Reparaturzellen übermütig werden und zu Treibern permanenter Narben werden. KDM7A hält über TLR8 Makrophagen davon ab, in einen profibrotischen Modus zu verfallen, und hilft so, nach einer Verletzung flexibles, funktionelles Lungengewebe zu erhalten. Versagt dieses System — durch genetischen Verlust, Alterung oder andere Faktoren — neigen Makrophagen eher dazu, zu „Narbenverstärkern“ zu werden und die Fibrose zu verschlimmern. Indem die Studie diese epigenetische Bremse offenlegt, weist sie auf neue therapeutische Strategien hin: Medikamente, die KDM7A-Aktivität stärken, seine Effekte nachahmen oder TLR8 gezielt stimulieren, könnten eines Tages die bestehenden antifibrotischen Therapien ergänzen und besseren Schutz gegen fortschreitende, lebensbegrenzende Lungenvernarbung bieten.
Zitation: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
Schlüsselwörter: Lungenfibrose, Makrophagen, Epigenetik, KDM7A, TLR8