Clear Sky Science · de
Erkennung und Bindung von Glykolipiden durch Siglec-6 beruht auf Wechselwirkungen mit der Zellmembran
Wie unsere Zellen Freund von Feind unterscheiden
Das Immunsystem durchmustert ständig die eigenen Zellen und entscheidet, wann es ruhig bleiben und wann es angreifen soll. Ein zentraler Bestandteil dieser Überwachung ist die Erkennung von zuckerartigen Strukturen auf Zelloberflächen. Diese Studie zeigt, dass ein menschlicher Immunrezeptor, Siglec-6, nicht nur diese Zucker nutzt, sondern auch die umgebende Zellmembran selbst einbezieht, um besonders präzise Bindungsentscheidungen zu treffen. Diese ungewöhnliche Strategie könnte erklären, wie der Körper Immunantworten feinabstimmt, und neue Wege für gezielte Therapien eröffnen.
Ein zuckererkennender Torwächter auf Immunzellen
Siglecs sind eine Familie von Rezeptoren auf Immunzellen, die sialinsäurehaltige Zucker erkennen und dem Immunsystem helfen, „selbst“ von „nicht-selbst“ zu unterscheiden. Die meisten Siglecs verlassen sich auf einen einzelnen, stark konservierten Baustein — eine Arginin-Aminosäure — um an diese Zucker zu binden. Wird diese Arginin entfernt, schlägt die Bindung normalerweise fehl. Siglec-6 ist jedoch ein Sonderfall: Frühere Arbeiten zeigten, dass es einige zuckertragende Lipide weiterhin binden kann, selbst wenn dieses Schlüssel-Arginin mutiert ist. Die neue Studie wollte aufklären, wie Siglec-6 diese scheinbare Regel umgehen kann und welche Bedeutung das für seine Rolle auf Mastzellen, Gedächtnis-B-Zellen und in der menschlichen Plazenta hat.
Die speziellen Lipide, nach denen Siglec-6 sucht
Auf Zelloberflächen können relevante Zucker sowohl an Proteine als auch an Lipide gebunden sein. Diese Arbeit konzentriert sich auf eine Gruppe von zuckertragenden Lipiden, die Ganglioside genannt werden, insbesondere drei eng verwandte Typen: GM1, GM2 und GM3. Alle drei ragen mit einer sialinsäuregekappten „Kopfgruppe“ aus der Membran heraus. Frühere Experimente zeigten, dass Siglec-6 stark an GM1 in einer Membran bindet, aber kaum an GM2 oder GM3, obwohl ihre Zucker-Köpfe sehr ähnlich sind. Mithilfe detaillierter Computersimulationen realistischer Membranen bestätigten die Autoren, dass die Sialinsäure in GM1 und GM3 gleichermaßen exponiert und zugänglich ist. Anders ausgedrückt: einfache physische Zugänglichkeit erklärt nicht den Sonderstatus von GM1. Stattdessen erwies sich ein zusätzliches Zuckerbaustein an der Spitze von GM1 — das terminale Galactose — als kritisches Element, das hilft, Siglec-6 korrekt an der Membran zu positionieren.
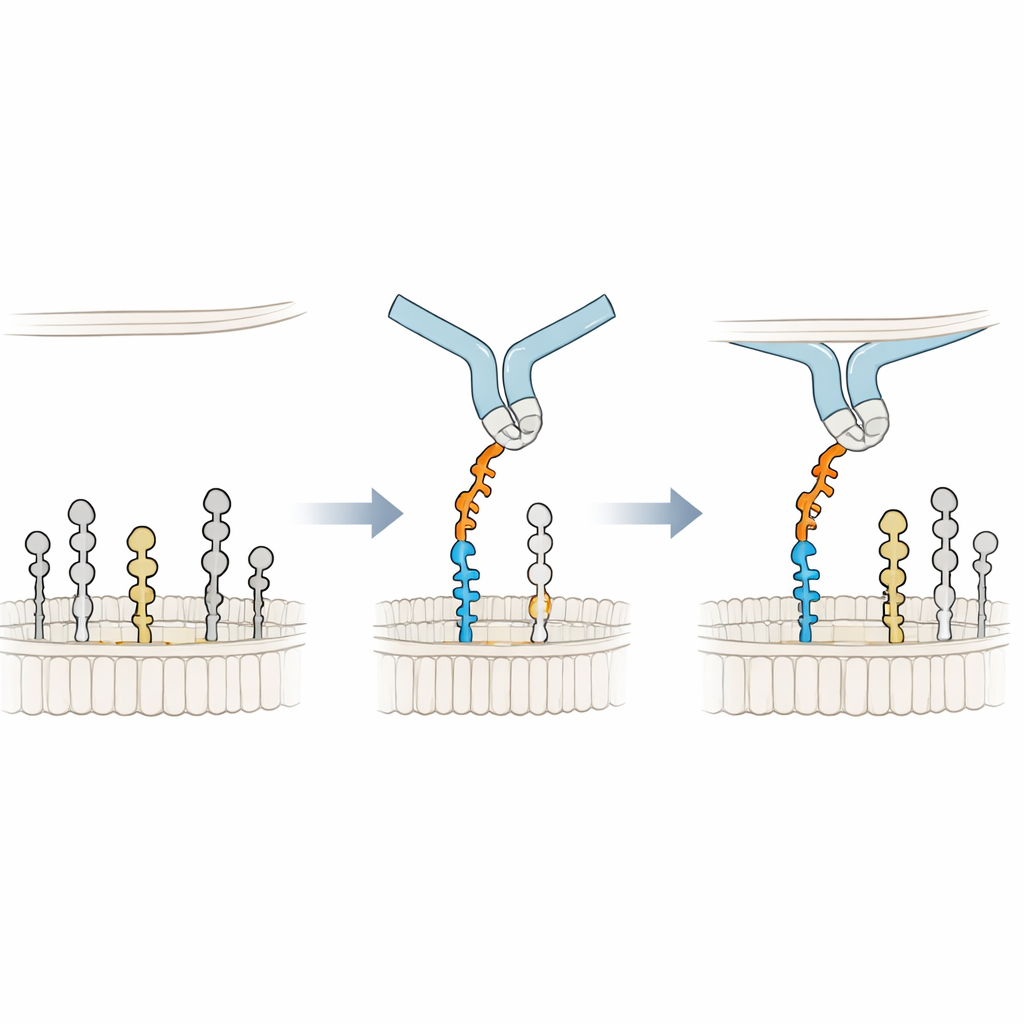
Auf die Membran stützen für besseren Halt
Um den Bindungsmechanismus auf atomarer Ebene zu verstehen, bauten die Forscher 3D-Modelle von Siglec-6 in Kontakt mit GM1 in einer Membran und führten lange Molekulardynamik-Simulationen durch. Sie fanden heraus, dass Siglec-6 weiterhin sein kanonisches Arginin (Arg122) nutzt, um die Sialinsäure zu kontaktieren, wobei dieser Kontakt jedoch über die Zeit an- und abschwillt. Stabilität gewinnt der Komplex durch etwas Neues: ein benachbartes Tryptophan (Trp127) dringt in den fettigen Teil der Membran ein, während ein angrenzendes Lysin (Lys126) mit den geladenen Kopfgruppen umliegender Lipide interagiert. Diese „Keil“-Einschiebung in die Membran ergänzt die übliche Zucker–Arginin-Wechselwirkung und entleiht so Bindungsenergie aus der Lipidumgebung. Wird die terminale Galactose von GM1 entfernt, um GM2 zu imitieren, schwingt eine flexible Schleife in Siglec-6 in den freigewordenen Raum, zieht den Rezeptor von der Membran weg und stört diesen membranunterstützten Halt — was den Verlust stabiler Bindung erklärt.
Experimente, die den Mechanismus prüfen
Das Team prüfte diese computergestützten Einsichten in lebenden Zellen und biochemischen Tests. Sie erzeugten Zellen, die normales oder mutiertes Siglec-6 exprimieren, und maßen, wie gut diese Zellen an fluoreszenzmarkierte Liposome und kleine Lipidscheiben mit GM1 binden. Die Mutation des kanonischen Arginins verringerte die Bindung nur moderat, wenn GM1 in einer Membran vorlag, was bestätigt, dass Siglec-6 in diesem Kontext nicht ausschließlich auf diese Aminosäure angewiesen ist. Im Gegensatz dazu beseitigte die Mutation von Trp127 nahezu vollständig die Bindung an GM1-enthaltende Liposome, und die kombinierte Mutation von Trp127 und Lys126 vernichtete die Bindung nahezu vollständig. Dieselben Mutanten banden jedoch normal an GM1-ähnliche Zucker, die außerhalb einer Membran präsentiert wurden, was zeigt, dass die Grundstruktur von Siglec-6 intakt war. Native Massenspektrometrie-Experimente zeigten zudem, dass Siglec-6 nicht nur an GM1, sondern auch an gewöhnliche Phospholipide binden kann, und dass diese Lipidinteraktion verschwindet, wenn Trp127 entfernt wird. Bemerkenswerterweise haftet Siglec-6 sogar an „nackten“ Liposomen ohne GM1, wiederum abhängig von Trp127, was darauf hindeutet, dass es die Membran zunächst sondieren und dann bei Begegnung mit GM1 einrasten könnte.
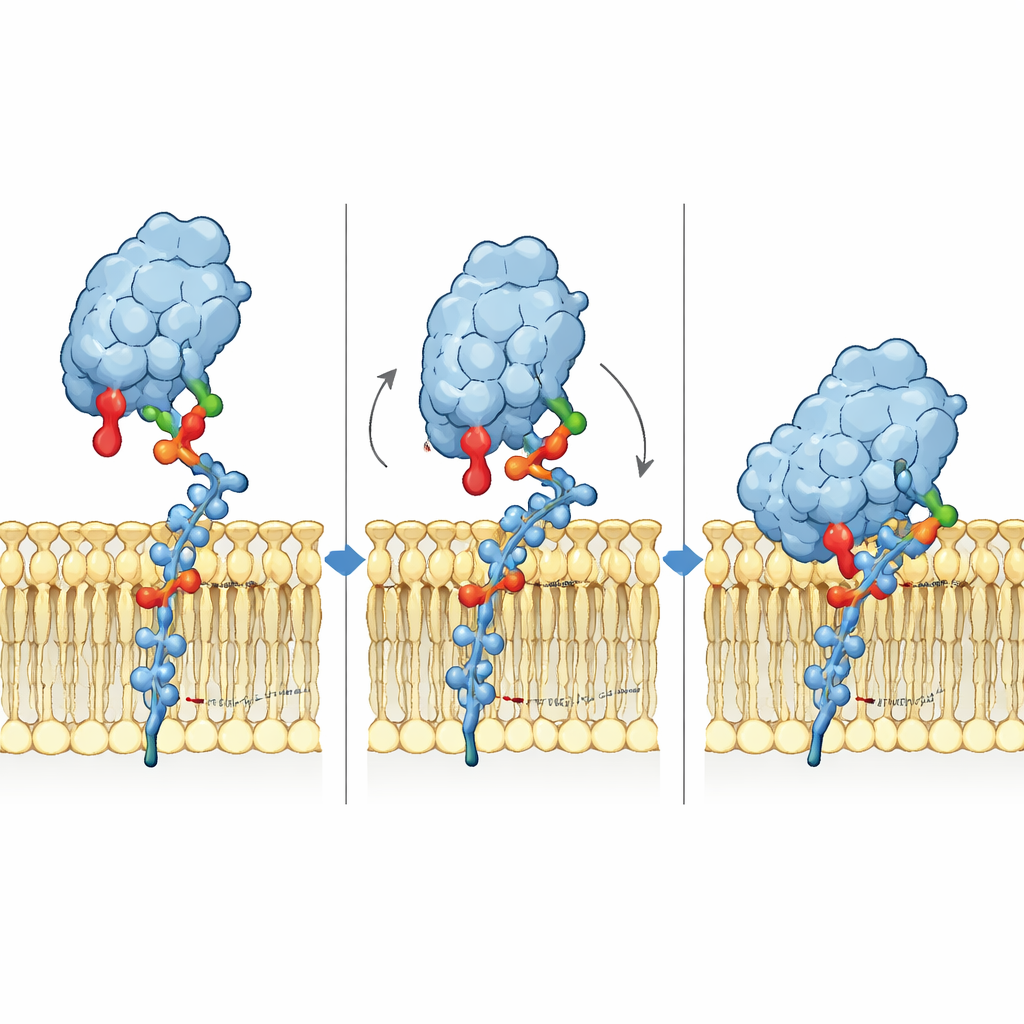
Freie Zucker erzählen eine andere Geschichte
Wenn dieselben drei Ganglioside als frei im Lösungsmittel vorliegende Zuckerteile statt als Teil einer Membran getestet wurden, verhielt sich Siglec-6 eher wie seine Verwandten. In Lösung band es GM1, GM2 und GM3 mit ähnlich schwacher Affinität, und jetzt war das kanonische Arginin essentiell: Die Mutation von Arg122 reduzierte die Bindung stark, während die Mutation von Trp127 kaum einen Effekt hatte. Dieser Kontrast zeigt, dass Siglec-6 je nach Kontext zwischen zwei Mechanismen umschaltet — abhängig davon, ob es Zucker in einer Membran oder in freier Form erkennt. In Membranen stützt es sich auf eine kooperative Partnerschaft zwischen der Zuckerkopfgruppe, der terminalen Galactose von GM1 und direktem Membrankontakt; in Lösung kehrt es zum klassischen, argininzentrierten Erkennungsmodus zurück.
Warum das für die Immunsteuerung wichtig ist
In der Summe stellt die Studie Siglec-6 als einen fein abgestimmten Sensor dar, der den physikalischen Kontext der Membran nutzt, um seine Spezifität zu schärfen. Durch teilweises Verankern in den umgebenden Lipiden kann es selektiv GM1 unter sehr ähnlichen Gangliosiden erkennen und so einen allgemeinen „Sialinsäure-Leser“ in einen hochpräzisen Detektor für ein bestimmtes Oberflächenmuster verwandeln. Diese membranunterstützte Strategie scheint unter den bisher untersuchten Siglecs einzigartig zu sein und könnte Siglec-6 dabei helfen, Zelloberflächen nach spezifischen Glykolipid-Signaturen zu durchsuchen, die Immunantworten regulieren oder bestimmte Gewebe markieren, etwa die menschliche Plazenta. Das Verständnis dieses dualen Erkennungsmodus könnte die Entwicklung von Therapien und Diagnostika fördern, die die ungewöhnliche Kombination aus Zucker- und Membranerkennung von Siglec-6 ausnutzen.
Zitation: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Schlüsselwörter: Siglec-6, Ganglioside, Zellmembran, Glykolipid-Erkennung, Immunregulation