Clear Sky Science · de
Destabilisierung der Hülle durch Überexpression von AcrAB2NodT verbindet Antibiotikaresistenz mit Metallempfindlichkeit in Caulobacter vibrioides
Wenn der Kampf gegen Antibiotika einen versteckten Preis hat
Wenn sich Antibiotikaresistenz ausbreitet, stellen wir uns oft vor, dass Bakterien einfach robuster und schwerer zu töten werden. Diese Studie zeigt eine überraschende Wendung: Bei einem häufigen Süßwasserbakterium macht eine Form der Arzneimittelresistenz die Zellen tatsächlich verwundbarer gegenüber bestimmten Metallen wie Kupfer und Zink. Das Verständnis dieses versteckten Trade-offs könnte neue Wege eröffnen, das Gleichgewicht wieder zu unseren Gunsten zu kippen, indem Antibiotika mit zusätzlichen Stressfaktoren kombiniert werden, die bakterielle Schwächen ausnutzen.
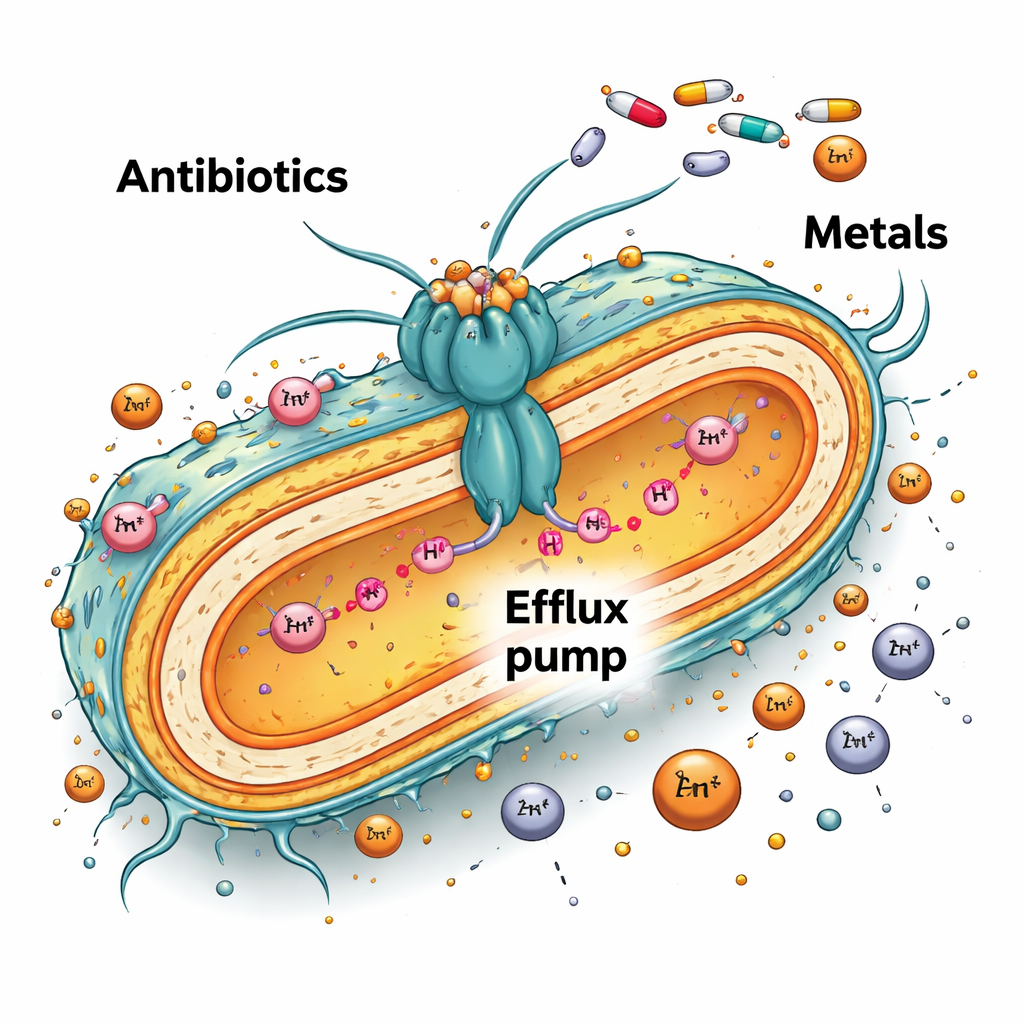
Eine bakterielle Pumpe mit doppelter Rolle
Viele Bakterien verteidigen sich mit kraftvollen molekularen Pumpen in ihren äußeren Schichten, die schädliche Verbindungen, einschließlich Antibiotika, ausstoßen. Bei Caulobacter vibrioides, einem freilebenden Mikroorganismus, der in nährstoffarmen Seen und Flüssen gedeiht, heißt eine solche Pumpe AcrAB2NodT. Sie überspannt die innere und äußere Membran der Zelle und wird normalerweise von einem Regulationsprotein namens TipR in Schach gehalten. Wenn TipR vorhanden ist, wird die Pumpe nur bei Bedarf produziert. Die Forschenden untersuchten, was passiert, wenn tipR gelöscht wird und ein Mutant entsteht, der diese Pumpe dauerhaft auf Volllast laufen lässt.
Gewinnen gegen Medikamente, Verlieren gegen Metalle
Der tipR-loser Mutant widerstand tatsächlich bestimmten Beta-Lactam-Antibiotika besser, was bestätigt, dass die überaktive Pumpe den Zellen hilft, Medikamente auszustoßen. Doch als das Team diese Zellen Kupfer und anderen Metallen wie Zink, Nickel und Cadmium aussetzte, kippte das Bild: Der Mutant wurde deutlich empfindlicher als normale Zellen. Sorgfältige Messungen zeigten, dass diese Empfindlichkeit nicht darauf zurückzuführen war, dass die Zellen zusätzliches Kupfer anhäuften oder mehr schädliche reaktive Sauerstoffspezies bildeten. Stattdessen blieb der gesamte Metallgehalt im Inneren des Mutanten ähnlich dem normaler Zellen, und übliche Indikatoren für oxidativen Stress stiegen nicht an. Das bedeutet, dass die Verwundbarkeit aus Veränderungen in der Zellstruktur oder der grundlegenden Physiologie resultieren musste, nicht aus einfacher Metallüberladung.
Eine fragile Haut und eine undichte Barriere
Bei näherer Betrachtung der Zelloberfläche nutzten die Wissenschaftler Elektronenmikroskope und Proteinanalyse und zeigten, dass die Überexpression von AcrAB2NodT die bakterielle „Haut“, die Zellhülle, stört. Mutante Zellen zeigten Ausbuchtungen, abnorme Formen und einen welligen, unregelmäßigen Abstand zwischen innerer und äußerer Membran. Proteine, die am Aufbau und an der Umgestaltung der Hülle beteiligt sind, waren vermehrt vorhanden, was darauf hindeutet, dass die Zellen ständig Reparaturmaßnahmen ergreifen. Zusätzliche Tests zeigten, dass die Hülle des Mutanten durchlässiger war und Farbstoffe leichter eindringen konnten, sobald die Pumpe experimentell daran gehindert wurde, sie auszustoßen. Wenn die Forschenden die Pumpe vollständig deaktivierten — entweder durch Löschung ihrer Gene oder durch subtile Mutationen, die sie zwar erhalten, aber weitgehend inaktiv machen — verschwanden sowohl die ungewöhnlichen Zellformen als auch die Metallempfindlichkeit weitgehend, obwohl einige Pumpenkomponenten weiterhin vorhanden waren.
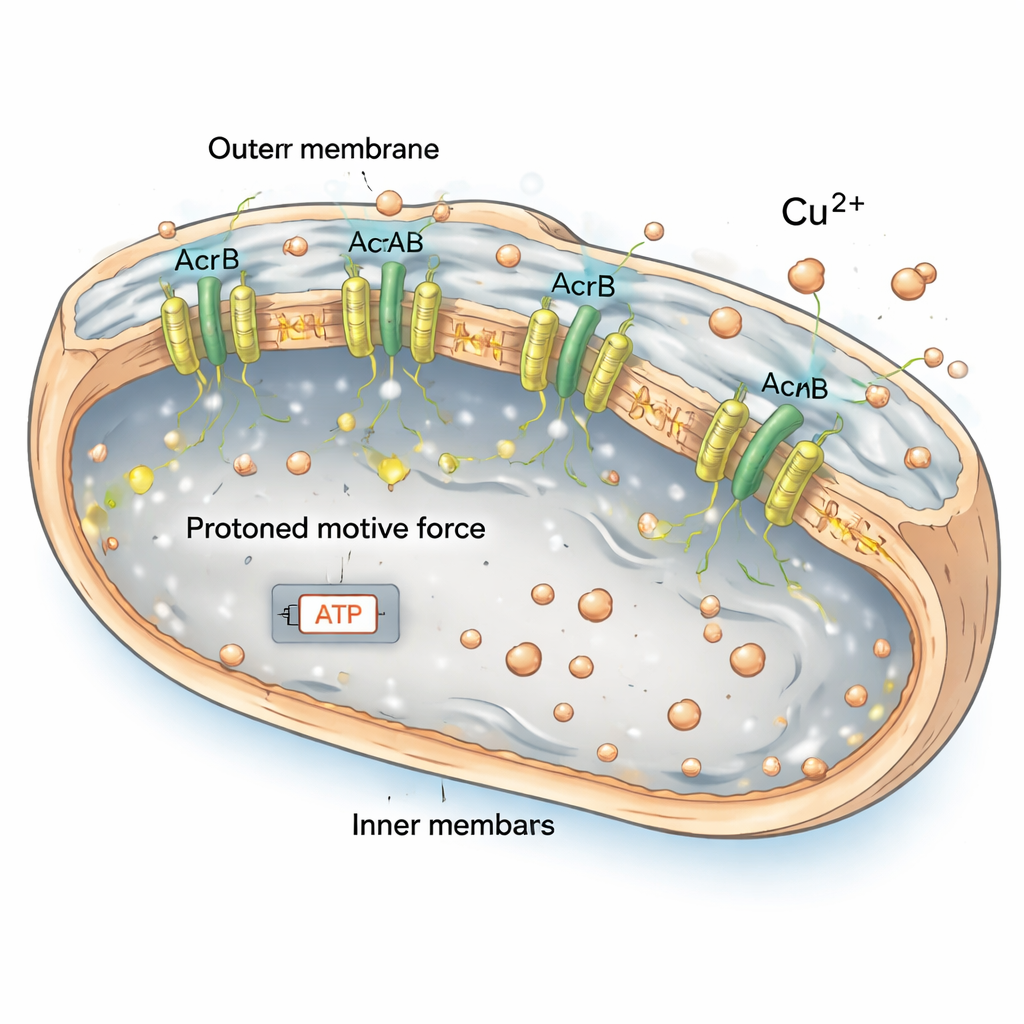
Leere Batterien und energetische Belastung
Effluxpumpen wie AcrAB2NodT werden durch die Protonengradientenkraft angetrieben, eine Art winziger Batterie, die durch geladene Teilchen über die innere Membran entsteht. In dem Mutanten, der die Pumpe ununterbrochen betreibt, war diese Batterie teilweise entladen: Ein Farbstoff, der die Membranspannung anzeigt, lieferte ein schwächeres Signal, und die Zellen hatten niedrigere ATP-Spiegel, ihre wichtigste Energiequelle. Die Bakterien versuchten, dies auszugleichen, indem sie Wege hochfuhren, die Energie produzieren, etwa jene zur Fettabbau, aber das reichte nicht aus, um den allgemeinen Energiemangel zu verhindern. Als die Forschenden in ansonsten normalen Zellen chemisch den Protonengradienten zusammenbrechen ließen, begannen diese Zellen dem Mutanten ähnlicher zu werden hinsichtlich ihrer schlechten Handhabung von Kupfer. Das legt nahe, dass die Kombination aus einer geschwächten Hülle und chronisch niedriger Energie die pumpenüberproduzierenden Bakterien besonders anfällig für Metallstress macht.
Eine Schwäche in eine Behandlungsstrategie verwandeln
Für Nichtfachleute ist die zentrale Botschaft: Antibiotikaresistenz kann einen Preis haben: Bakterien überleben Medikamente besser, werden aber in anderer Hinsicht fragiler. Bei Caulobacter belastet das ständige Betreiben einer leistungsstarken Wirkstoffpumpe die äußeren Schichten und die Energieversorgung der Zelle, sodass sie weniger gut mit Metallen wie Kupfer zurechtkommt. Dieser Trade-off deutet auf neue Behandlungsideen hin. Wenn ähnliche Schwächen bei krankheitserregenden Bakterien existieren, könnten Ärztinnen und Ärzte die Wirksamkeit von Antibiotika steigern, indem sie sie mit Metallen oder anderen Agenzien kombinieren, die die energetische und strukturelle Belastung von Resistenmechanismen ausnutzen und resistente Mikroben über ihre Belastungsgrenze treiben.
Zitation: Ote, M., Lardinois, L., Hendrickx, E. et al. Envelope destabilization by AcrAB2NodT overexpression links antibiotic resistance to metal sensitivity in Caulobacter vibrioides. Commun Biol 9, 313 (2026). https://doi.org/10.1038/s42003-026-09606-x
Schlüsselwörter: Antibiotikaresistenz, Effluxpumpen, Kupferempfindlichkeit, bakterielle Hülle, Energiestoffwechsel