Clear Sky Science · de
Integrierte Analyse von GWAS und molQTLs zeigt zellspezifische genetische Varianten im porzinen Immunsystem
Warum Schweineimmunität für uns alle wichtig ist
Schweine tragen wesentlich zur weltweiten Nahrungsmittelversorgung bei und dienen außerdem in der medizinischen Forschung als wichtige Modellorganismen für den Menschen. Infektionskrankheiten bei Schweinen verursachen jedoch jährliche Verluste in Milliardenhöhe für Landwirte und führen zu einem hohen Antibiotikaeinsatz. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Wie beeinflussen winzige DNA-Unterschiede die Funktionsweise von Immunzellen beim Schwein und lassen sich diese Effekte bis zum Verhalten einzelner Zelltypen im Blut zurückverfolgen? Das Verständnis dieser Kausalkette könnte die Zucht gesünderer Bestände leiten und Hinweise auf unser eigenes Immunsystem liefern.
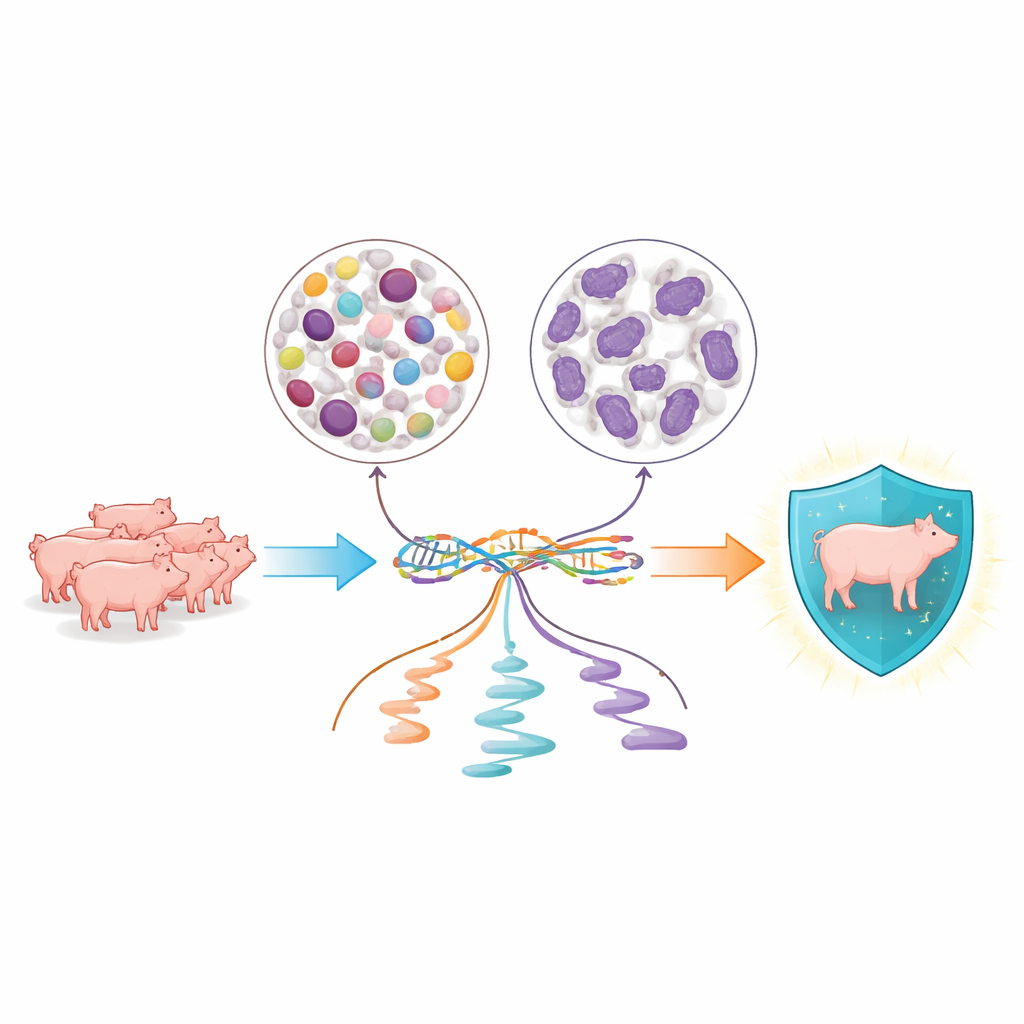
Genauer Blick auf zwei wichtige Blutzellfamilien
Die Forschenden konzentrierten sich auf zwei große Gruppen weißer Blutkörperchen, die das Schweineblut dauerhaft patrouillieren: periphere mononukleäre Blutzellen, zu denen Lymphozyten und Monozyten gehören und die an langsameren, zielgerichteten Abwehrreaktionen beteiligt sind, und Neutrophile, die schnelle Erstangriffe gegen Mikroben ausführen. Von 134 jungen Yorkshire‑Schweinen reinigten sie jeden Zelltyp separat und gewannen sowohl Ganzgenom‑DNA‑Daten als auch detaillierte Momentaufnahmen der RNA, der Moleküle, die genetische Anweisungen innerhalb der Zellen tragen. So konnten sie nicht nur erkennen, welche Gene aktiviert waren, sondern auch, wie die Zelle diese Botschaften vor der Nutzung zuschneidet und fertigstellt.
Verknüpfung von DNA‑Varianten mit molekularen Schaltern
Statt nur zu untersuchen, welche DNA‑Varianten mit Krankheitsrisiken assoziiert sind, kartierten die Forschenden, wie Varianten drei Arten molekularer Merkmale in jedem Zelltyp beeinflussen. Manche Varianten veränderten, wie viel RNA ein Gen produzierte. Andere beeinflussten das Spleißen der RNA, also das Kürzen oder Umordnen von Abschnitten. Eine dritte Klasse verschob, wie die RNA am 3'-Ende abgeschlossen wird — ein Prozess namens Polyadenylierung, der die Stabilität der Botschaft beeinflussen kann. Diese Variant‑Wirkungs‑Paare nennt man molekulare quantitative Trait‑Loci oder molQTLs. Die Karten zeigten jeweils Tausende solcher Stellen in den Zelltypen, und auffällig war, dass mehr als vier von fünf spezifisch entweder für die gemischten mononukleären Zellen oder für die Neutrophilen waren — ein Hinweis darauf, wie unterschiedlich dasselbe Genom in verschiedenen Immunzellen gelesen werden kann.
Netzwerke finden, die Gene mit realen Immunmerkmalen verbinden
Um zu sehen, wie diese molekularen Schalter mit der Immunität des ganzen Tiers zusammenhängen, kombinierten die Wissenschaftler die molQTL‑Karten mit Standardbluttests und Messungen immuner Signalmoleküle. Sie bauten Koexpressionsnetzwerke — Gruppen von Genen, die dazu neigen, gemeinsam an- oder abzuschalten — und prüften, welche davon mit Merkmalen wie dem Anteil an Neutrophilen oder Lymphozyten, der weißen Blutkörperchenzahl oder den Spiegeln von Interferonen und Tumor‑nekrose‑Faktor korrelieren. Module, die mit Lymphozytenmerkmalen verbunden waren, waren bereichert für adaptive Immunwege, während solche, die mit Neutrophilenmerkmalen assoziiert waren, schnelle angeborene Abwehrmechanismen und entzündliche Signalwege hervorhoben. Viele Schlüsselgene in diesen Modulen wurden direkt durch zellspezifische molQTLs reguliert, was klare Pfade von einer DNA‑Variante zu veränderter Zellzusammensetzung oder -funktion nahelegt.
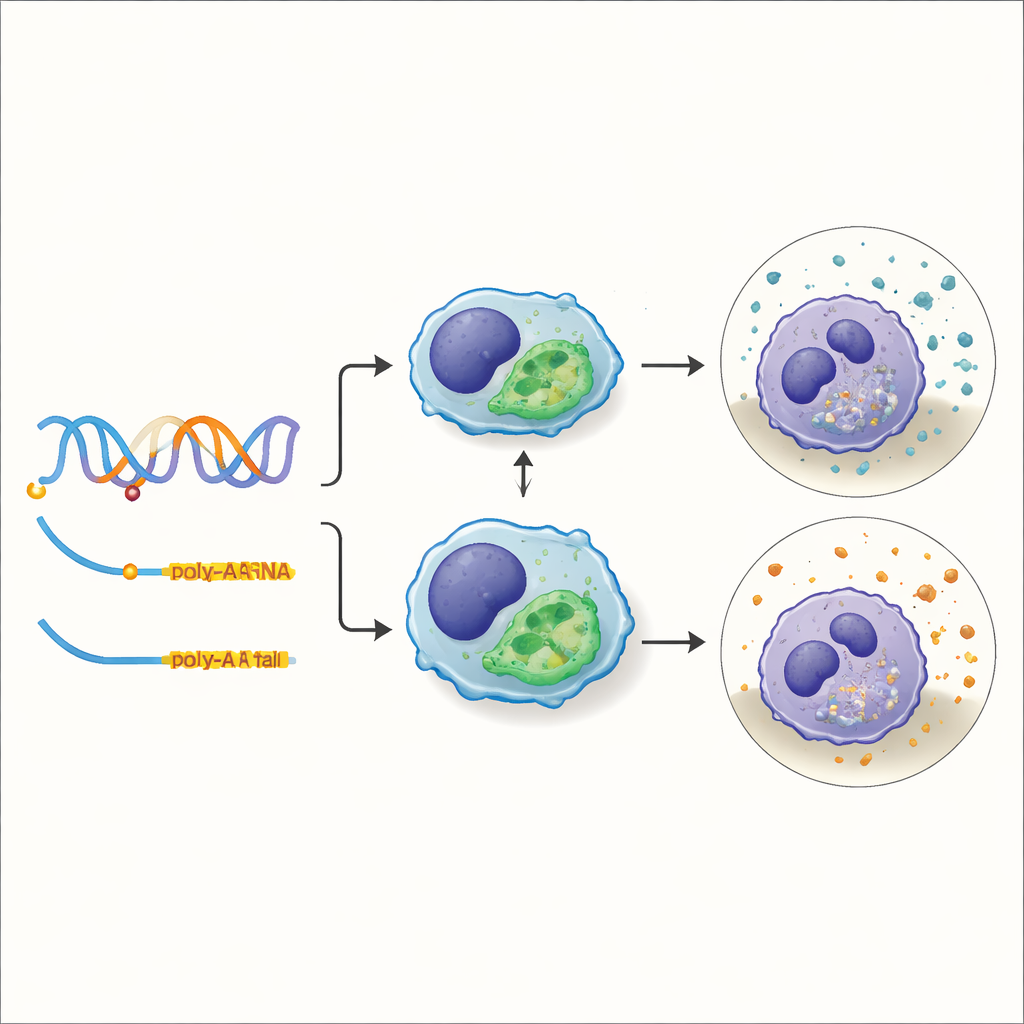
Hineinzoomen auf eine Variante, die die zelluläre „Reinigungs“fähigkeit abstimmt
Eines der praktischsten Merkmale, das das Team untersuchte, war die phagozytische Kapazität — die Fähigkeit von Immunzellen, Fremdstoffe oder Krankheitserreger aufzunehmen und zu entfernen. Durch Überlagerung ihrer molQTLs mit den Ergebnissen früherer genomweiter Assoziationsstudien zur Phagozytose identifizierten sie 588 Regionen, in denen wahrscheinlich dieselbe DNA‑Änderung sowohl einen molekularen Effekt als auch eine Veränderung der zellulären Reinigungsleistung verursacht. Ein herausragendes Beispiel war eine Variante innerhalb eines Gens namens TXNDC15. Diese Veränderung schaltete das Gen nicht einfach ein oder aus; stattdessen veränderte sie, welche Polyadenylierungsstelle die Zelle für die RNA des Gens wählte. Schweine mit einer Version der Variante bevorzugten einen kürzeren RNA‑Schwanz, der stabiler war und sich in höheren Mengen ansammelte, und diese Tiere zeigten eine stärkere phagozytische Aktivität ihrer Immunzellen.
Was das für gesündere Schweine und darüber hinaus bedeutet
Einfach ausgedrückt zeigt diese Arbeit, wie kleine DNA‑Unterschiede die „Anleitungen“ in bestimmten Immunzelltypen neu verdrahten können und dadurch beeinflussen, wie viele dieser Zellen vorhanden sind und wie gut sie ihre Aufgaben erfüllen. Durch die sorgfältige Trennung der Zelltypen und die Verfolgung nicht nur der Genaktivität, sondern auch davon, wie Botschaften zugeschnitten und fertiggestellt werden, deckt die Studie Kontrollpunkte auf, die in Untersuchungen an gemischtem Gewebe verborgen bleiben. Die resultierende genetische Karte bietet eine Grundlage für die Zucht von Schweinen mit natürlicherer Krankheitsresistenz und kann so potenziell den Antibiotikaeinsatz reduzieren. Da die Immunität des Schweins unserem eigenen System ähnelt, können diese Erkenntnisse gleichzeitig Forschern helfen, zu verstehen, wie vergleichbare Mechanismen beim Menschen Gesundheit und Krankheit beeinflussen.
Zitation: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Schlüsselwörter: Schweineimmunität, genetische Varianten, Immunzellen, Phagozytose, molekulare QTLs