Clear Sky Science · de
ATM-Inhibition verbessert Knock-in-Effizienz durch Unterdrückung der AAV‑induzierten Aktivierung apoptotischer Wege
Geneditierung effektiver machen
CRISPR-Geneditierung verspricht Therapien für Erbkrankheiten, robustere Nutzpflanzen und leistungsfähige Forschungstools. Eine der wertvollsten Anwendungen — das präzise Einfügen neuer DNA an einer gewählten Stelle im Genom, bekannt als „Knock-in“ — bleibt jedoch ineffizient. Diese Studie untersucht, warum einige Zellen neues DNA-Material eher annehmen als andere, und zeigt einen Weg, Zellen dazu zu bringen, präzise Veränderungen häufiger vorzunehmen, insbesondere bei Verwendung von adeno-assoziiertem Virus (AAV), einem führenden Vektor in der Gentherapie.
DNA-Reparatur in Echtzeit beobachten
Um zu verstehen, was präzises Genseinfügen fördert oder behindert, bauten die Forschenden ein ausgeklügeltes „Dashboard“ in murinen embryonalen Stammzellen. Dieses Dreifach-Reportersystem verwendet drei fluoreszierende Marker, um in denselben Zellen zu verfolgen, ob CRISPR die DNA geschnitten hat, ob ein präziser Knock-in stattgefunden hat und ob die Zelle stattdessen die Donor-DNA mithilfe einer gröberen Reparaturmethode eingeklebt hat. Durch Auslesen verschiedener Farbkombinationen mittels Durchflusszytometrie konnten sie saubere, templatesbasierte Editierungen von fehleranfälligen Insertionsereignissen und unbearbeiteten Zellen trennen. Dieses parallele Tracking erlaubte es, mit deutlich höherer Auflösung als ältere PCR-basierte Tests abzubilden, wie unterschiedliche DNA-Reparaturwege zu jedem Ergebnis beitragen.
Zwei DNA‑Geber, zwei sehr unterschiedliche Antworten
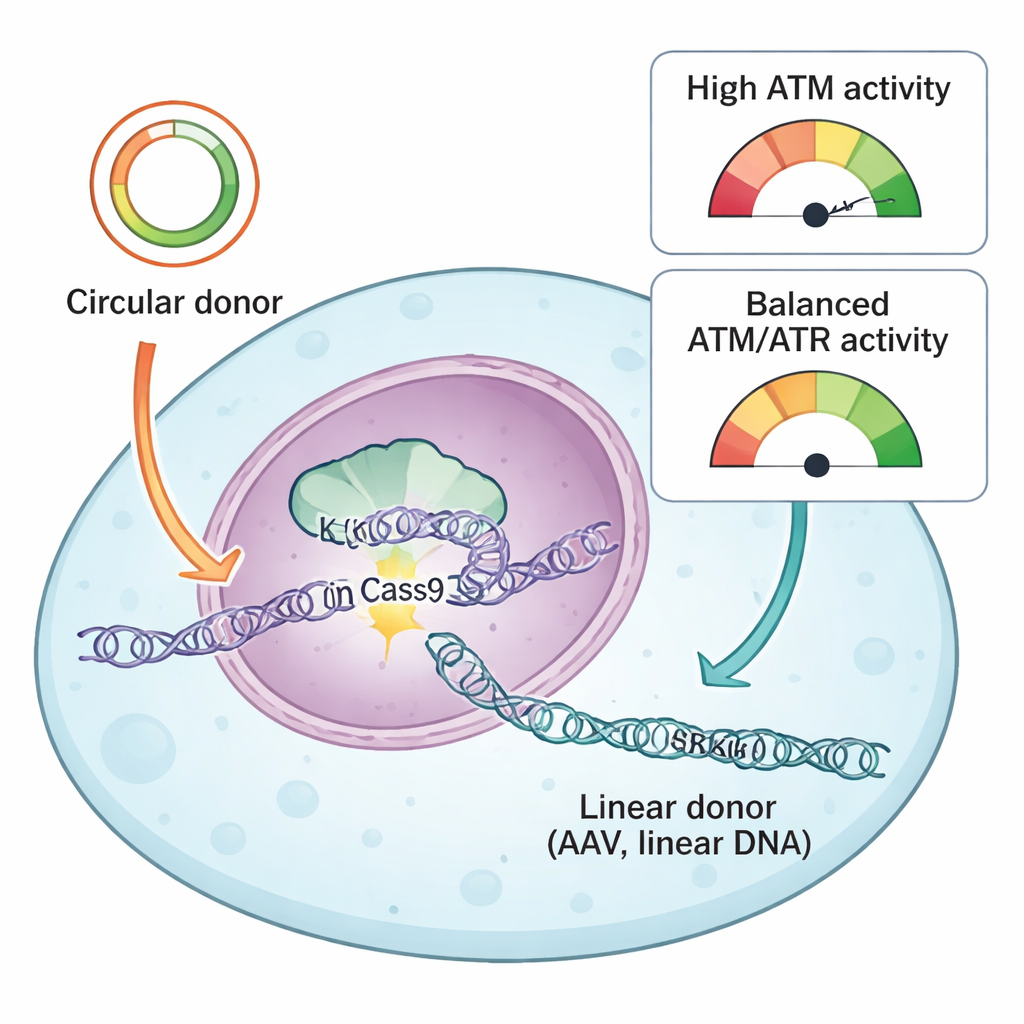
Das Team verglich zwei gebräuchliche Typen von Donor-DNA, die CRISPR-Reparaturen leiten: zirkuläre Plasmide und lineare, von AAV abgeleitete DNA. Beide tragen passende „Homologiearme“, die der Zelle zeigen, wo die neue Sequenz eingefügt werden soll, treten aber in unterschiedlichen physikalischen Formen in die Zelle ein. Zirkuläre Plasmide sind geschlossene Doppelstrang‑DNA‑Schleifen, während AAV-Donoren typischerweise als einzelne lineare Moleküle vorliegen. Mithilfe ihres Reportersystems und einer Bibliothek von Wirkstoffen, die Proteine der DNA‑Schadensantwort gezielt beeinflussen, fanden die Autoren, dass ein Schlüsselprotein, ATR, durchgängig essentiell für erfolgreiche Knock-ins mit beiden Donortypen war. Die Hemmung von ATR reduzierte präzise Inserts stark, während eine moderate Steigerung der ATR‑Aktivität über den KEAP1–NRF2‑Weg Knock-ins effizienter machte, besonders bei AAV‑Donoren.
Wenn DNA‑Schutz nach hinten losgeht
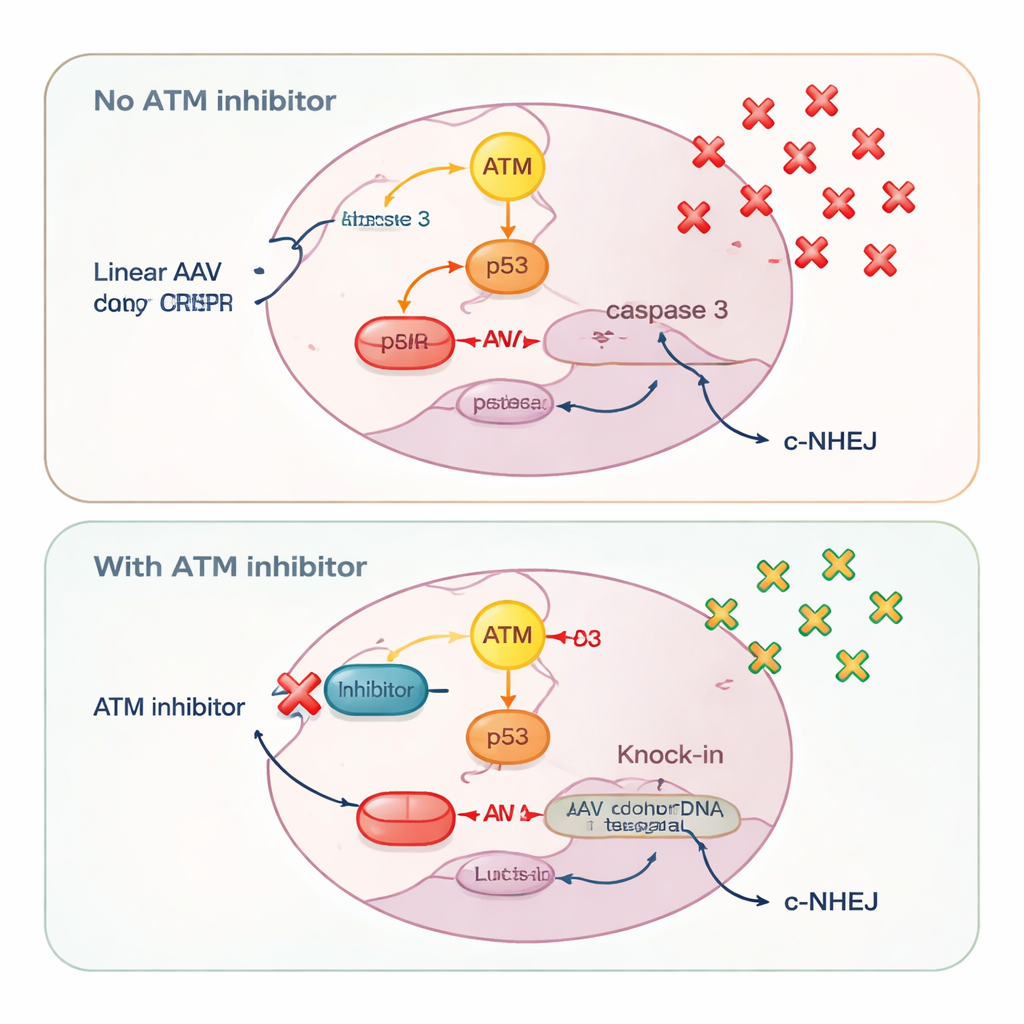
Ein anderer Sensor der DNA‑Schadensantwort, ATM, zeigte ein auffallend donorenabhängiges Verhalten. Bei zirkulären Plasmiddonoren verringerte die Blockade von ATM sowohl präzise Knock-ins als auch end-joining–vermittelte Insertionsereignisse, was seiner klassischen Rolle beim Helfen der Zellen zur Reparatur von Doppelstrangbrüchen entspricht. Bei linearer DNA — egal ob von AAV, selbstkomplementärem AAV oder in gerade Stücke geschnittenen Plasmiden — wirkte sich die ATM‑Hemmung jedoch genau entgegengesetzt aus: Sie erhöhte die Knock-in‑Effizienz. Die Forschenden führten diesen Effekt darauf zurück, wie Zellen auf eine Flut linearer DNA reagieren. Hohe AAV‑Dosen aktivierten ATM stark, was wiederum p53 und Caspase‑3 anschaltete, zentrale Akteure des programmierten Zelltods. Zellen, die viele Kopien der Donor‑DNA aufgenommen hatten und damit die höchste Chance für einen erfolgreichen Knock-in besaßen, wurden durch dieses Alarmsystem gleichzeitig am ehesten getötet.
Die am besten ausgerüsteten Zellen retten
Durch Zugabe von ATM‑Inhibitoren dämpften die Wissenschaftler den ATM–p53–Caspase‑3‑Todesweg. Dadurch blieben Zellen mit hohen Donor‑DNA‑Mengen erhalten und konnten länger überleben, um einen präzisen Knock-in abzuschließen. Messungen der viralen Genomkopien bestätigten, dass ATM‑Hemmung die Zahl der in Zellen verbleibenden AAV‑Moleküle erhöhte. Gleichzeitig schwächte die ATM‑Blockade geringfügig eine schnelle, stumpfe Reparaturroute namens klassische nicht-homologe Endverknüpfung (c-NHEJ), wie die reduzierte Aktivierung von DNA‑PK, einem Kernenzym dieses Weges, zeigte. Das Abschwächen dieser konkurrierenden Reparaturoption lenkte mehr CRISPR‑Schnitte in Richtung homologiegestützter Knock-ins statt in schnelle Flickarbeiten, die die Donorvorlage ignorieren.
Was das für zukünftige Gentherapien bedeutet
Für Nicht‑Spezialisten lautet die Botschaft: Dieselben zellulären Schutzmechanismen, die uns vor DNA‑Schäden bewahren, können präzise Geneditierung unbeabsichtigt sabotieren, besonders wenn große Mengen viraler Donor‑DNA verwendet werden. Diese Arbeit zeigt, dass ein sensibles Einstellen dieser Schutzmechanismen — ATR aktiv halten, aber ATM vorübergehend zurückhalten, wenn lineare Donoren wie AAV vorhanden sind — CRISPR‑Knock‑ins verlässlicher und effizienter machen kann. Eine solche Strategie könnte Gentherapien, Zellengineering und Krankheitsmodelle verbessern, indem mehr Zellen die beabsichtigte Veränderung übernehmen, während unnötiger Zellverlust vermieden wird.
Zitation: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Schlüsselwörter: CRISPR Knock-in, AAV-Geneditierung, DNA-Schadensantwort, ATM-Inhibition, Genom-Engineering