Clear Sky Science · de
STING steuert Glykolyse und Histon-Lactylierung und treibt die metabolische Umprogrammierung von Makrophagen bei postoperativem Ileus voran
Wenn Operationen den Darm auf Pause stellen
Nach Bauchoperationen erleben viele Patienten, dass sich ihr Darm einfach nicht wieder in Gang setzt. Diese Verlangsamung, postoperativer Ileus genannt, bedeutet oft Tage mit Übelkeit, Völlegefühl und verzögerter Genesung. Die hier zusammengefasste Studie stellt eine auf den ersten Blick einfache Frage: Warum halten bestimmte Immunzellen im Darm den Darm blockiert, und könnte das Absenken eines einzelnen molekularen Schalters dem Darm helfen, die Bewegung wieder aufzunehmen?
Wie ein Routineeingriff Darmentzündung auslöst
Bauchoperationen stören unvermeidlich den Darm. Bei Mäusen reichte schon sanftes Handhaben des Darms aus, um Schwellungen, Flüssigkeitsansammlungen und verstopfte Inhalte im Dünndarm zu verursachen. Als die Forschenden verfolgten, wie weit ein harmloser fluoreszierender Farbstoff durch den Darm wanderte, stellten sie fest, dass die Operation seinen Fortschritt stark verlangsamte – ein Zeichen für beeinträchtigte Motilität. Die mikroskopische Untersuchung der Darmwand zeigte, dass die Muskelschicht – das Gewebe, das sich kontrahiert, um Nahrung voranzutreiben – entzündet war und von einströmenden Immunzellen, vor allem Makrophagen und Neutrophilen, überfüllt wurde. Diese Befunde deuten darauf hin, dass sich die muskuläre Schicht des Darms nach einer Operation in ein entzündetes Schlachtfeld verwandelt, und diese lokale Entzündung eng mit der Lähmung des Darms verknüpft ist.
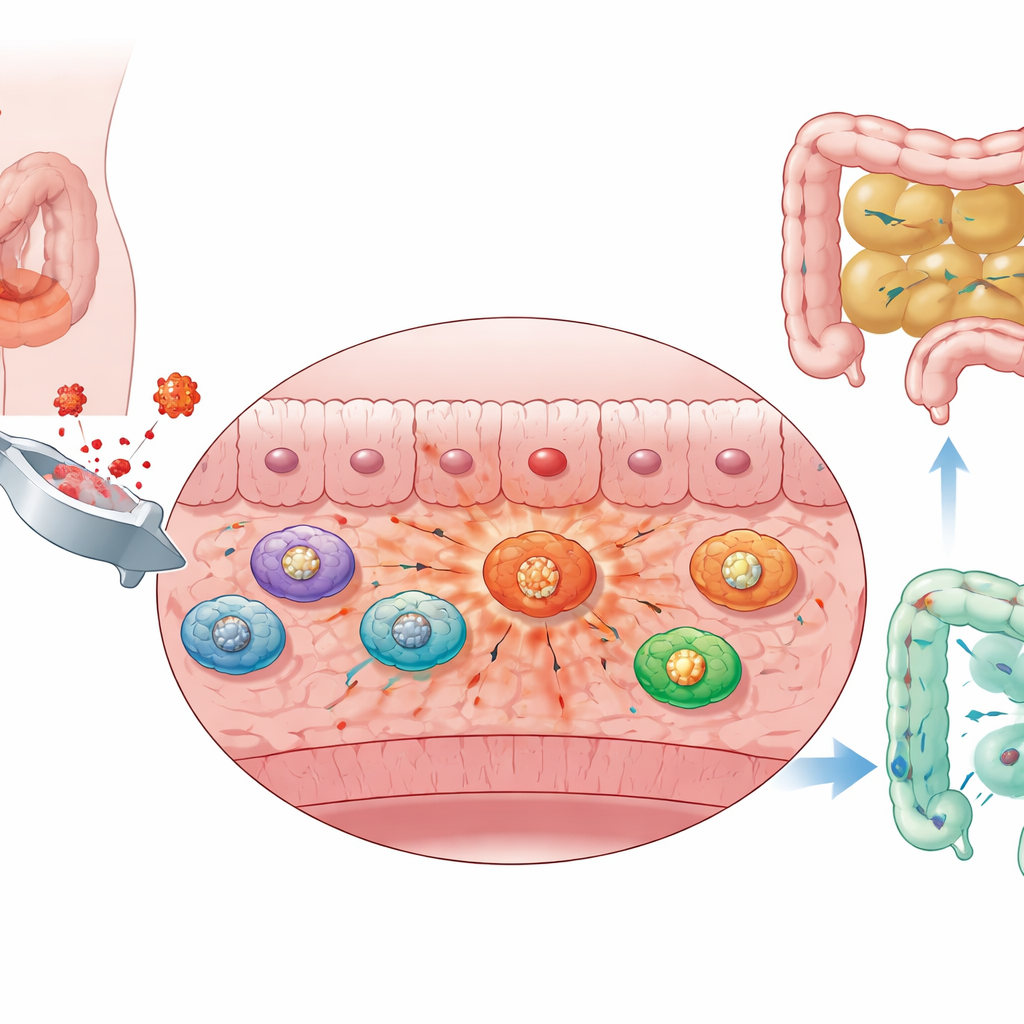
Makrophagen wechseln ihren Brennstoff und schüren die Entzündung
Um zu verstehen, was diese einströmenden Makrophagen taten, wertete das Team groß angelegte RNA- und Einzelzell-Sequenzierungsdaten aus der Darmmuskelschicht aus. Sie fanden heraus, dass Makrophagen in operierten Tieren einen schnellen, zuckerverbrauchenden Stoffwechselweg, bekannt als Glykolyse, stark hochfuhren. Verglichen mit anderen Immunzellen im selben Gewebe zeigten die einströmenden Makrophagen die höchsten Glykolyse-Werte und exprimierten erhöhte Mengen wichtiger glykolytischer Enzyme. Eine eigene Untergruppe dieser Zellen war stark von Glykolyse abhängig, trug ausgeprägte entzündliche Signaturen und reagierte heftig auf bakterielle Komponenten wie Lipopolysaccharid. Im Wesentlichen hatten die Makrophagen in einen Hochzucker-/Hochentzündungs-Modus geschaltet, der offenbar die Entzündung der Muskelschicht verschärft und so die Darmbewegung weiter behindert.
Ein molekularer Schalter, der Gefahrenerkennung mit Zuckerabbau koppelt
Die Forschenden konzentrierten sich dann auf STING, ein Protein, das vor allem als Alarmmechanismus für fremde DNA bekannt ist, zunehmend aber auch als Stoffwechselregulator erkannt wird. In der entzündeten Darmmuskulatur zeigte die stark glykolytische Makrophagen-Untergruppe deutlich höhere STING-Werte, ein Muster, das sich auch in Gewebefärbungen bestätigte. In Zellkultur führte die Exposition von Makrophagen mit bakteriellen Lipopolysacchariden zu einer Steigerung sowohl der STING-Aktivität als auch der glykolytischen Enzyme, die Glukose in Energie und Laktat umwandeln. Als die Wissenschaftler das STING-Gen ausschalteten, brach dieser Zuckerverbrennungs-Schub zusammen: Glykolyse-Intermediärstoffe sanken, die Ansäuerung des Kulturmediums nahm ab und es wurden weniger reaktive Sauerstoffspezies produziert. Diese STING-defizienten Zellen erzeugten auch weniger Laktat, was darauf hindeutet, dass der Alarmweg und der metabolische Motor eng gekoppelt sind.
Vom Zuckerabbau zum epigenetischen Gedächtnis
Laktat wird oft als Stoffwechselabfall betrachtet, spielt hier jedoch eine subtilere Rolle. Das Team zeigte, dass in normalen Makrophagen die Flut an Laktat genutzt wird, um Histone – die Proteine, die DNA verpacken – chemisch zu modifizieren, ein Prozess, der als Lactylierung bezeichnet wird. Diese Modifikation war besonders ausgeprägt an einer Stelle namens H4K8 auf Histonen in der Nähe des Gens für HK2, ein Schlüsselenzym der Glykolyse. In STING-defizienten Zellen waren Histon-Lactylierung und die Zugänglichkeit des Chromatins am HK2-Promotor reduziert, und spezialisierte Sequenziermethoden bestätigten, dass diese Änderungen die Aktivierung von HK2 einschränkten. Gleichzeitig wurde ein nachgelagerter Transkriptionsfaktor, IRF3, eher an den HK2-Promotor gebunden, wenn diese Histon-Lactylierungsmarke vorhanden war. Zusammen schaffen diese Schritte eine sich selbst verstärkende Schleife: STING stabilisiert Faktoren, die die Glykolyse fördern, die Glykolyse produziert Laktat, Laktat markiert Histone, um das HK2-Gen zu öffnen, und IRF3 erhöht die HK2-Expression, was wiederum Glykolyse und Entzündung weiter antreibt.
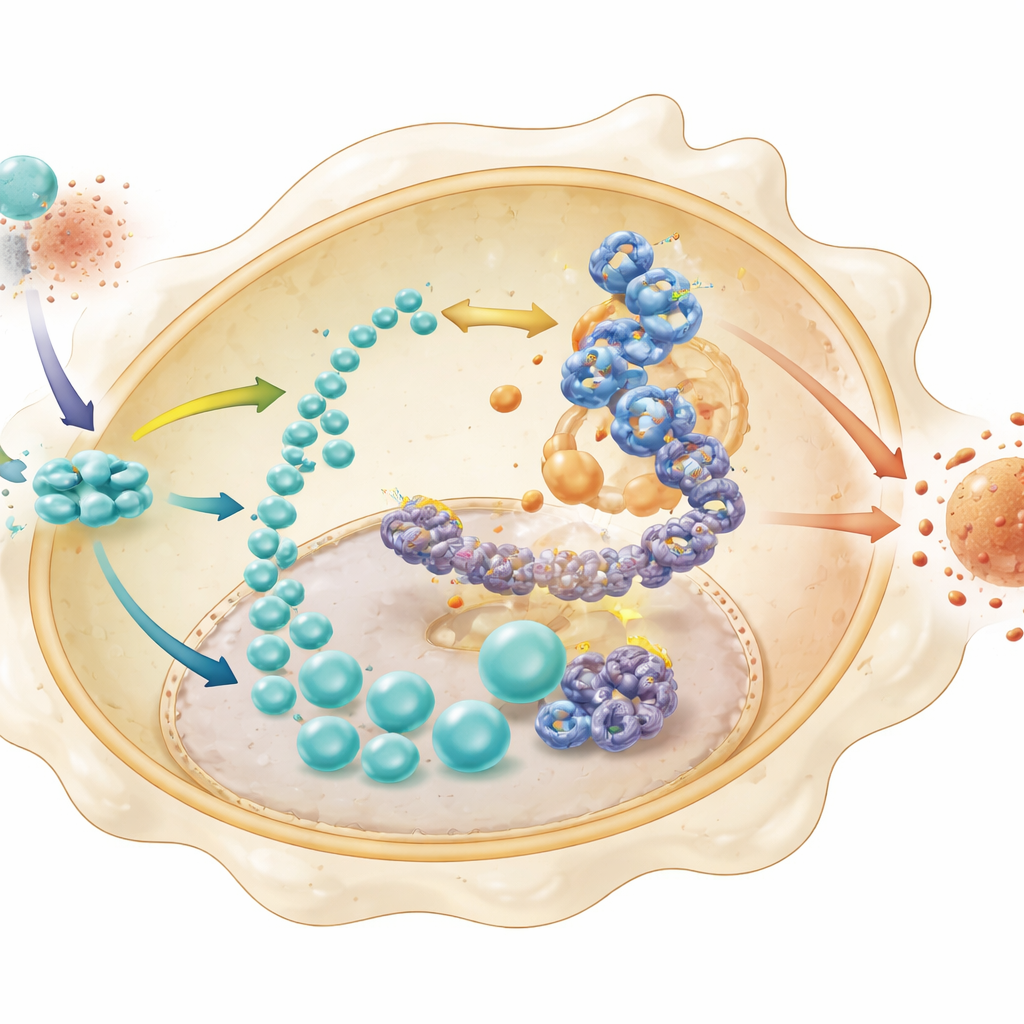
Die Schleife durchbrechen, damit sich der Darm erholt
Schließlich untersuchten die Forschenden, ob das Durchbrechen dieser Schleife Tieren tatsächlich bei der Erholung vom postoperativen Ileus helfen könnte. Bei Mäusen ohne STING exprimierte das Darmmuskelgewebe weniger glykolytische Enzyme, enthielt weniger entzündliche Makrophagen und zeigte eine Verschiebung weg von einem aggressiven, proinflammatorischen Makrophagenzustand hin zu einem eher lösenden Profil. Die Infiltration von Neutrophilen war geringer und der Darmpassageverbesserte sich. Die pharmakologische Blockade von STING in normalen Mäusen brachte ähnliche Vorteile, während die Reaktivierung des HK2-Enzyms in STING-defizienten Tieren Entzündung und Motilitätsstörungen teilweise wiederherstellte. Für eine/n Laien ist die Botschaft klar: Ein einziger Gefahrensensor in Darmmakrophagen kann ihren Stoffwechsel so umlenken, dass der Darm nach einer Operation in eine anhaltende Pause gelangt. Die gezielte Beeinflussung von STING – oder des von ihm kontrollierten Zucker verbrennenden, Laktat-vermittelten Rückkopplungskreises – bietet einen vielversprechenden Weg, die Erholung zu beschleunigen und eine der hartnäckigsten Komplikationen von Bauchoperationen zu lindern.
Zitation: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Schlüsselwörter: postoperativer Ileus, Makrophagenstoffwechsel, STING-Signalweg, Glykolyse, Darmentzündung