Clear Sky Science · de
Allergenspezifisches humanes IgE, isoliert durch eine allergen-agnostische Pipeline — Verständnis von Immunantwort und Allergenerkennung
Warum das für Allergiegeplagte wichtig ist
Saisonales Niesen und juckende Augen mögen einfach erscheinen, doch die Moleküle, die diese Reaktionen auslösen, sind es nicht. Diese Studie zeigt eine neue Methode, um die exakten humanen Antikörper, die eine Gräserpollenallergie antreiben, direkt aus allergischen Patienten zu erfassen und zu untersuchen. Durch die bisher unerreichte Kartierung dieser Antikörper eröffnet die Arbeit Wege zu präziseren Diagnosen, intelligenteren Allergieimpfungen und künftigen Wirkstoffen, die Symptome an ihrer molekularen Quelle blockieren könnten. 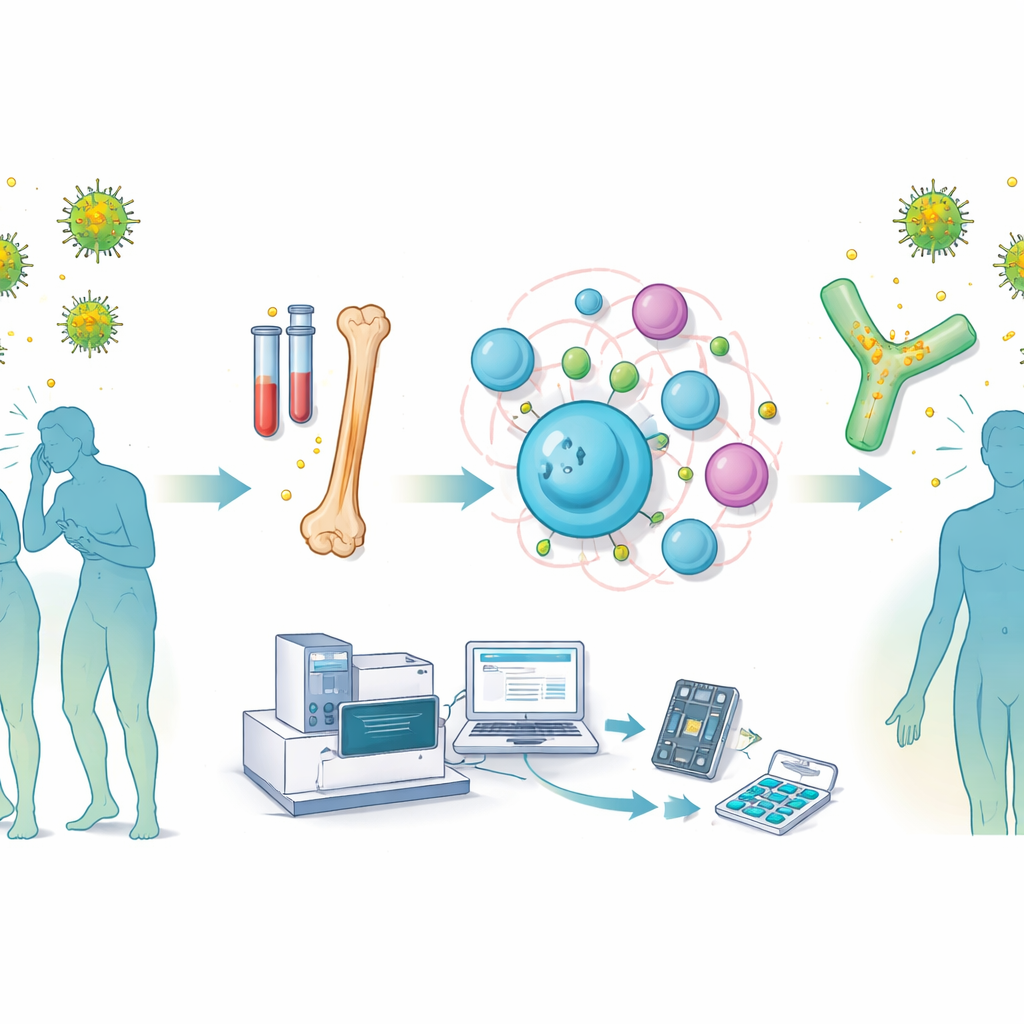
Ein neues Fenster zu Allergenmolekülen
Allergische Reaktionen auf Pollen werden von einer speziellen Antikörperklasse namens IgE angetrieben, die auf Immunzellen sitzen und bei Kontakt mit einem Allergen Entzündungen auslösen. IgE-produzierende Zellen sind jedoch selten, und bisher standen Wissenschaftlern überraschend wenige vollständig humane IgE-Antikörper zur Verfügung. Die Forscher bauten eine „Pipeline“, die dieses Problem überwindet. Sie sammelten Blut und Knochenmark von sechs Personen mit durch Gräserpollen induzierter Heuschnupfen und nutzten Einzelzell-Sequenzierung, um Zelle für Zelle die gepaarten schweren und leichten Kettengene zu lesen, die jeden Antikörper ausmachen. Parallel dazu verwendeten sie Tiefensequenzierung aller Antikörpergene jeder Person, um zu sehen, welche Antikörperfamilien IgE-Versionen enthielten.
Allergen-spezifische Antikörper herausfischen
Statt mit einem bestimmten Allergen zu beginnen, verfolgte das Team einen allergen-agnostischen Ansatz. Zunächst suchten sie in den Bulk-Sequenzierungsdaten nach Antikörperfamilien, die IgE-Mitglieder enthielten, und ordneten diese Familien dann kompletten schweren–leichten Kettenpaaren aus den Einzelzell-Daten zu. Mithilfe rekombinanter DNA-Techniken stellten sie diese Antikörper im Labor wieder her, meist in der stabileren IgG-Form und teilweise auch als IgE. Danach folgte die Detektivarbeit: eine Reihe von Bindungstests mit gereinigten Allergenen und komplexen Pollenauszügen sowie Immunpräzipitation gefolgt von Massenspektrometrie, um zu bestimmen, welche Polleneiweiße jeder Antikörper herausziehen und erkennen konnte. 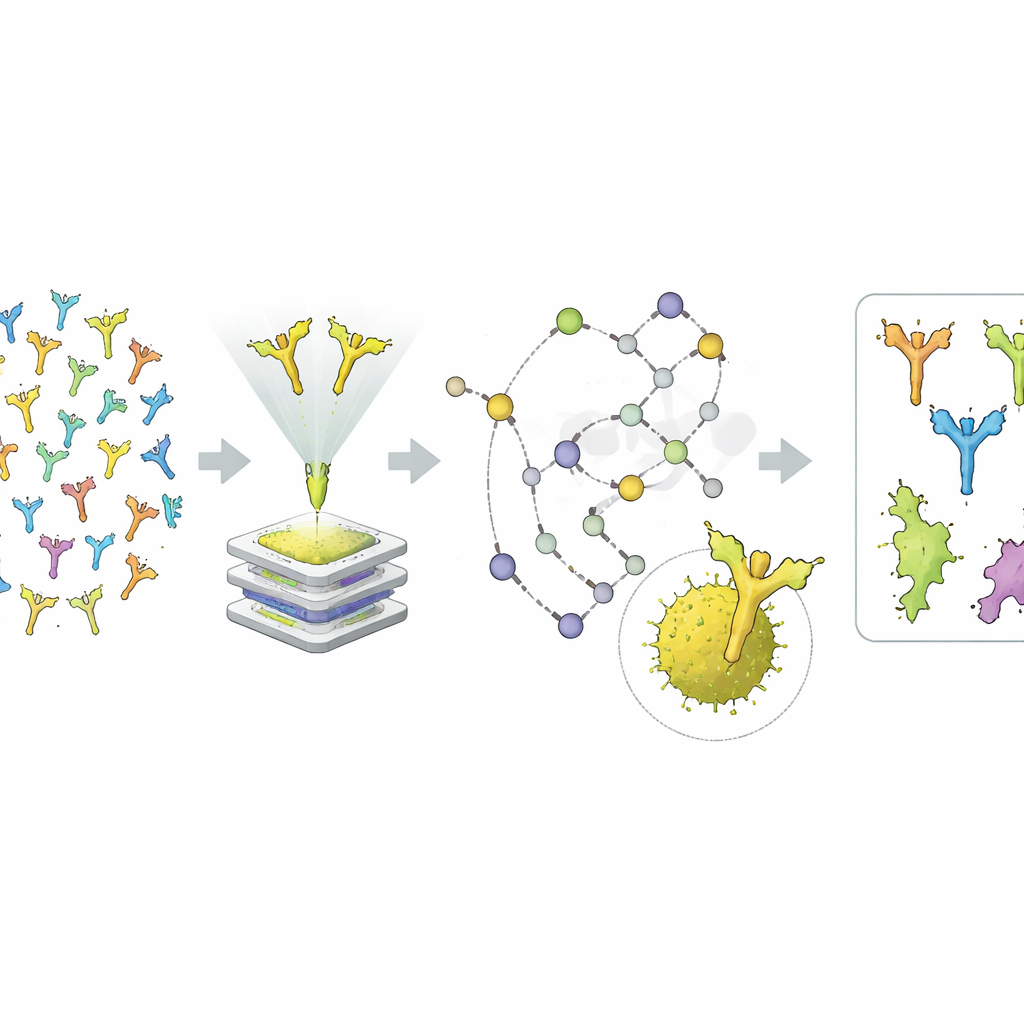
Vier zentrale Gräserpollen-Ziele identifiziert
Aus vielen Kandidaten lieferte die Pipeline vier vollständig humane Antikörper, die eindeutig verschiedene Komponenten des Gräserpollens erkannten. Ein Antikörper richtete sich gegen Gruppe-5-Allergene des Timotheusgrases, ein anderer gegen Gruppe 11, ein dritter gegen Gruppe 3 und ein vierter gegen Gruppe 4. Alle vier banden ihre Ziele mit bemerkenswert hoher Affinität im sub-nanomolaren Bereich, was bedeutet, dass sie sehr fest an ihre Allergene binden und nur sehr langsam dissoziieren. Der Gruppe-3-Antikörper erwies sich als besonders aufschlussreich: Er band Pollenauszüge von Gräsern aus einem großen botanischen Zweig (dem BOP-Kladus), jedoch nicht aus einem anderen (dem PACMAD-Kladus), was zeigt, dass dieses Allergen ungleichmäßig über Gräserarten verteilt ist. Der Gruppe-4-Antikörper zeigte, dass einige klinisch wichtige Allergenkomponenten in standardisierten Extrakt-basierten Diagnosetests unterrepräsentiert sein können.
Wie sich Allergieantikörper im Körper entwickeln
Da jede Antikörperfamilie mehrere Sequenzvarianten enthielt, konnte das Team „Stammbäume“ rekonstruieren, die nachzeichneten, wie sich diese Antikörper im Laufe der Zeit veränderten. Für den Gruppe-5-spezifischen Antikörper fanden sie sowohl IgG1- als auch IgE-Varianten aus derselben Linie. Auffällig war, dass die IgG1-Variante nur geringfügig mutiert war, aber bereits sehr hohe Affinität zeigte, was darauf hindeutet, dass potente Allergieantikörper aus nahezu naiven Zellen mit minimaler Bearbeitung entstehen können. Die IgE-Variante trug mehr Veränderungen, gewann jedoch nicht dramatisch an Affinität, was nahelegt, dass ein Klassenwechsel zu IgE nach der Etablierung eines starken Binders erfolgen kann. Andere Antikörperfamilien fanden sich sowohl im Blut als auch im Knochenmark, was mit langlebigen Zellen vereinbar ist, die allergisches Gedächtnis über Jahre hinweg aufrechterhalten.
Von der Laborentdeckung zu künftigen Therapien
Über das grundlegende Verständnis hinaus prüften die Autoren, ob sich diese nativen humanen Antikörper als Ausgangspunkte für Arzneimittel eignen. Ein rechnerisches „Developability“-Screening ergab, dass die meisten günstige Eigenschaften aufwiesen, mit nur geringfügigen Sequenzmerkmalen, die eventuell angepasst werden müssten. Insgesamt zeigen die Ergebnisse, dass die Kombination aus Einzelzell-Sequenzierung, Analyse des Bulk-Repertoires und proteinbasierten Tests natürliche, hochaffine humane IgE-verwandte Antikörper zuverlässig isolieren kann, ohne vorher nach einem Allergen auszuwählen. Für Menschen mit Heuschnupfen und verwandten Erkrankungen bedeutet das: Wissenschaftler können jetzt präziser kartieren, welche Pollenmoleküle relevant sind, wie das Immunsystem lernt, sie zu erkennen, und wie man Diagnostika, Impfstoffe oder antikörperbasierte Therapien entwickelt, die Allergien beruhigen, indem sie die Krankheit an ihrer molekularen Wurzel angreifen.
Zitation: Thörnqvist, L., Franciskovic, E., Godzwon, M. et al. Allergen-specific human IgE isolated through an allergen-agnostic pipeline—understanding immune response and allergen recognition. Commun Biol 9, 332 (2026). https://doi.org/10.1038/s42003-026-09600-3
Schlüsselwörter: Gräserpollenallergie, IgE-Antikörper, Einzelzell-Sequenzierung, Allergenspezifische Immuntherapie, monoklonale Antikörper