Clear Sky Science · de
Charakterisierung der Entwickelbarkeit von Nanobodies zur Verbesserung therapeutischer Designs mit dem Therapeutic Nanobody Profiler
Warum winzige Antikörper‑Verwandte für zukünftige Medikamente wichtig sind
Viele der heutigen Blockbuster‑Medikamente sind Antikörper—Proteine, die mit hoher Präzision an Krankheitsziele binden. Eine neuere Klasse noch kleinerer Bindemoleküle, sogenannte Nanobodies, kann in schwer zugängliche Taschen von Viren, Tumoren und anderen Molekülen eindringen. An ein Ziel binden zu können reicht jedoch nicht: Ein Medikamentenkandidat muss außerdem leicht herstellbar, in einer Flasche stabil und im Körper sicher sein. Dieser Artikel stellt den Therapeutic Nanobody Profiler vor, ein rechnergestütztes Werkzeug, das Wissenschaftlern bereits früh und allein anhand der Sequenz dabei hilft zu beurteilen, welche Nanobodies am wahrscheinlichsten praktikable Medikamente werden.
Vom vielversprechenden Konzept zum praktischen Medikament
Aus einem Protein eine reale Therapie zu machen, erfordert zahlreiche praktische Hürden, die unter dem Begriff „Developability“ (Entwickelbarkeit) zusammengefasst werden. Proteine müssen in großen Mengen produziert werden, löslich bleiben, Agglomeration vermeiden und während Versand und Lagerung stabil sein. In den letzten zehn Jahren haben Forscher gelernt, viele dieser Eigenschaften für vollgroße monoklonale Antikörper vorherzusagen—gestützt auf umfangreiche klinische Daten und spezialisierte Labortests. Nanobodies unterscheiden sich jedoch strukturell: Sie bestehen aus einer einzelnen Domäne statt aus einem Kettenpaar, haben oft längere Bindeschleifen und offenbaren Oberflächenbereiche, die bei konventionellen Antikörpern verborgen sind. Daher können auf reguläre Antikörper zugeschnittene Methoden bei Nanobodies irreführende Ergebnisse liefern.
Ein Profiler, gebaut für Nanobody‑Eigenheiten
Um diese Diskrepanz anzugehen, entwickelten die Autoren den Therapeutic Nanobody Profiler (TNP), inspiriert von einem früheren Werkzeug für Standardantikörper, aber um die Biologie von Nanobodies herum neu konstruiert. Sie sammelten Nanobody‑Sequenzen aus vielen Quellen: klinischen Studien, natürlichen Immunrepertoires, Patenten, wissenschaftlichen Publikationen und bekannten Kristallstrukturen. Mit auf Einzel‑Domänen‑Antikörper zugeschnittenen Deep‑Learning‑Strukturvorhersagern erzeugten sie 3D‑Modelle für diese Sequenzen. Aus jedem Modell bestimmten sie die Länge der Bindeschleifen, wie weit eine zentrale Schleife vom Proteinkörper reicht, und wie sich Cluster hydrophober und geladener Reste auf der Oberfläche anordnen—Merkmale, die Löslichkeit, Aggregation und unspezifische Anhaftung stark beeinflussen.
Zwei strukturelle Varianten, beide brauchbar
Eines der auffälligsten Ergebnisse betrifft die Hauptbindeschleife, bekannt als CDR3. Als das Team quantifizierte, wie „kompakt“ diese Schleife ist—indem sie ihre Länge mit ihrer Ausstülpung vom Protein verglichen—zeigte sich eine deutliche Aufspaltung in zwei Strukturtypen. In einem Subtyp ist die Schleife länger und klappt über die Seite des Proteins zurück, wobei sie viele stabilisierende Kontakte zu einer charakteristischen Residuen‑Gruppe bildet. Im anderen ragt die Schleife stärker heraus, ähnlich wie bei einem konventionellen Antikörperfragment. Klinische Nanobodies finden sich in beiden Subtypen, und beim Vergleich zahlreicher praktischer Labormessungen—etwa zu Aggregation, Selbstassoziation und thermischer Stabilität—zeige sich kein systematischer Nachteil für einen der beiden Stile. Das bedeutet, dass Arzneimitteldesigner keinen generellen Favoriten für eine bestimmte Schleifenform bevorzugen müssen, sofern andere Eigenschaften akzeptabel sind.
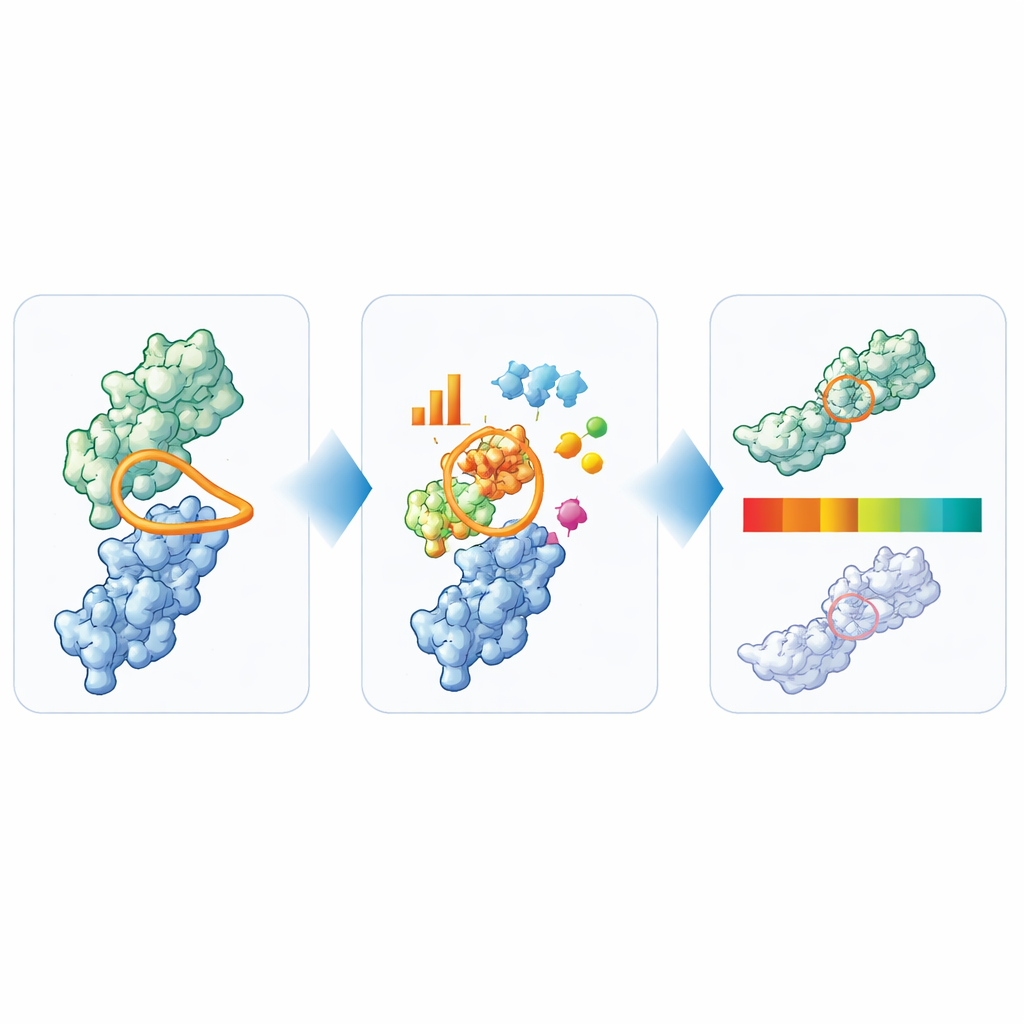
Struktur in einfache Ampelfarben übersetzen
Aus ihrer breiten Analyse destillierten die Autoren sechs Schlüsselfunktionen, die zusammen die wichtigsten Entwickelbarkeitsbedenken für Nanobodies erfassen: Gesamtlänge der Schleifen, die spezifische Länge und Kompaktheit von CDR3 sowie die Größe hydrophober, positiv geladener und negativ geladener Oberflächenpats rund um das Bindungsgebiet. Anschließend nutzten sie die 36 Nanobodies, die klinische Prüfungen erreicht haben, um praktische Grenzen für jede Messgröße festzulegen. Werte im zentralen, häufig belegten Bereich werden als „grün“ gekennzeichnet, Randwerte als „gelb“ und deutliche Ausreißer als „rot“. Um zu prüfen, wie aussagekräftig diese Signale sind, wandten sie TNP auf 72 zusätzliche proprietäre Nanobodies an und verglichen die Markierungen mit einem umfassenden Panel von Labortests. Nanobodies, die TNP als eindeutige Ausreißer markierte, zeigten meist auch mehrere experimentelle Warnsignale, während diejenigen, die rechnerisch sauber erschienen, im Labor häufiger gutartig waren.
Was das für die Therapien von morgen bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die Form und das Oberflächenmuster eines Nanobodies lassen sich inzwischen in ein leicht verständliches Entwickelbarkeitsprofil überführen, noch bevor teure Laborexperimente begonnen werden. Der Therapeutic Nanobody Profiler ersetzt keine Experimente, und Abweichungen zwischen Vorhersagen und Tests kommen weiterhin vor, unter anderem weil Labortests an Nanobodies durchgeführt wurden, die an größere Antikörperfragmente fusioniert waren. Indem TNP jedoch Kandidaten mit ungewöhnlich langen oder eng gefalteten Schleifen oder mit problematischen Oberflächenpats schnell markiert, lenkt es die Aufmerksamkeit auf Nanobodies, die mit höherer Wahrscheinlichkeit verlässliche Medikamente werden. Mit dem Eintritt weiterer Nanobodies in klinische Studien und der Erweiterung des Referenzsatzes sollte dieses Werkzeug noch genauer werden und die Entwicklung kleiner, robuster, antikörperähnlicher Therapeutika für ein breites Spektrum von Krankheiten beschleunigen.
Zitation: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Schlüsselwörter: Nanobodies, Entwickelbarkeit biologischer Arzneimittel, computationales Profiling, Antikörper‑Engineering, Protein‑Stabilität