Clear Sky Science · de
DTX1-vermittelte Degradation von TUBB3 in Kupffer-Zellen mildert das Fortschreiten des hepatozellulären Karzinoms durch Regulierung der M1/M2-Polarisation
Warum die immunologischen „Nachbarn“ von Leberkrebs wichtig sind
Die meisten Menschen denken bei Krebs an entartete Zellen, die unkontrolliert wachsen. Tumoren leben jedoch in einer lebhaften Nachbarschaft aus Immunzellen, Blutgefäßen und Stützgewebe, die entweder gegen den Krebs kämpfen oder ihm stillschweigend beim Wachsen helfen können. Diese Studie untersucht Leberkrebs – konkret das hepatozelluläre Karzinom – und zeigt, wie ein Protein in spezialisierten Leber-Immunzellen das Gleichgewicht zwischen einer krebsbekämpfenden Reaktion und einer tumorfördernden Umgebung verschieben kann. Das Verständnis dieses verborgenen Schalters könnte neue Wege eröffnen, bestehende Immuntherapien zu verbessern.
Ein Leberkrebs, der von seiner Umgebung angetrieben wird
Die Leber ist reich an Immunzellen, darunter eine ortsansässige Population, die als Kupffer-Zellen bezeichnet wird und normalerweise zur Organhomöostase beiträgt. Bei Leberkrebs verwandeln sich viele dieser Zellen in tumorassoziierte Makrophagen, die entweder den Krebs angreifen (ein M1-ähnlicher Zustand) oder ihn schützen (ein M2-ähnlicher Zustand). Patientinnen und Patienten, deren Tumoren von M2-typischen Makrophagen durchsetzt sind, haben meist eine ungünstigere Prognose und sprechen oft schlecht auf Wirkstoffe an, die die Immunbremsen lösen, wie PD-1-Inhibitoren. Die Autorinnen und Autoren begannen damit, öffentliche Gen-Datenbanken und Patientenproben nach Molekülen zu durchsuchen, die sowohl mit Leberkrebs als auch mit diesen Makrophagen in Verbindung stehen, und konzentrierten sich auf ein Strukturprotein namens TUBB3, das in Tumorgewebe überraschend reichlich vorkam.
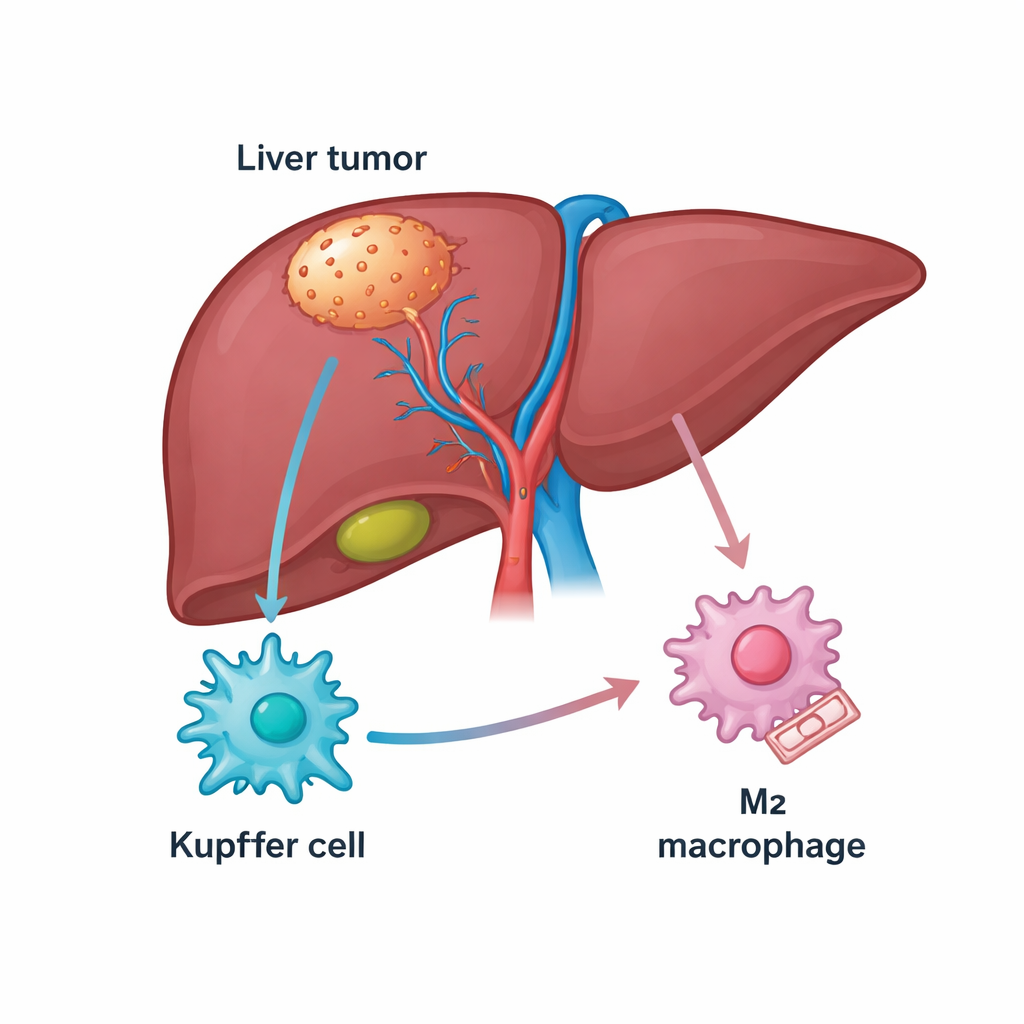
Ein überraschendes Protein, das Immunzellen dazu bringt, Tumoren zu unterstützen
TUBB3 ist vor allem als Baustein der mikroskopischen "Schienen" innerhalb von Zellen bekannt, wurde aber auch mit aggressivem Verhalten und Arzneimittelresistenz in mehreren Krebsarten in Verbindung gebracht. Die Forschenden fanden hier, dass die TUBB3-Spiegel in Lebertumoren deutlich höher waren als im angrenzenden gesunden Gewebe und dass Patienten mit höherer TUBB3-Expression tendenziell eine kürzere Überlebenszeit hatten. Mit Färbetechniken zeigten sie, dass TUBB3 besonders in Kupffer-Zellen innerhalb der Tumoren angereichert war und stark mit Markern des tumorfördernden M2-Zustands korrelierte. Anders gesagt: Kupffer-Zellen, die viel TUBB3 enthalten, neigen eher dazu, Immunangriffe abzuschwächen und das Tumorwachstum zu unterstützen.
Makrophagen umprogrammieren, um Lebertumoren einzudämmen
Um Ursache und Wirkung zu testen, reduzierten die Forschenden in Laborversuchen TUBB3 in Kupffer-Zellen. Nach TUBB3-Downregulation produzierten diese Zellen weniger M2-typische Signale, mehr M1-typische Signale und sezernierten weniger Moleküle, die normalerweise die Immunaktivität unterdrücken. Leberkrebszellen, die diesen umprogrammierten Makrophagen ausgesetzt wurden, wuchsen langsamer, teilten sich weniger und hatten eine geringere Fähigkeit zu migrieren und zu invasieren. In Mäusen führten Gemische aus Leberkrebszellen und TUBB3-defizienten Kupffer-Zellen zu kleineren Tumoren, mehr Tumorzellsterben und einem stärkeren Zustrom von zytotoxischen CD8-T-Zellen, die mit destruktiven Proteinen ausgerüstet waren. Wurden die Makrophagen den Tieren ganz entzogen, verschwand der Nutzen der TUBB3-Blockade größtenteils, was unterstreicht, dass der Effekt über diese Immunzellen und nicht allein über die Krebszellen vermittelt wird.
Aufdeckung einer internen Bremse auf einem wichtigen Signalweg
Die Studie untersuchte außerdem, wie TUBB3 diesen Einfluss ausübt. Die Autorinnen und Autoren fokussierten sich auf einen bekannten Wachstums- und Überlebensweg, der durch die Proteine PTEN und AKT gesteuert wird und ebenfalls beeinflusst, ob Makrophagen eine M1- oder M2-Identität annehmen. Sie fanden, dass die Reduktion von TUBB3 PTEN erhöhte, was wiederum die aktivierenden "Phosphat-Tags" auf AKT verringerte und die Makrophagen in Richtung des tumorbekämpfenden Zustands schob. Als sie AKT künstlich reaktivierten, kehrten die Makrophagen zum M2-Muster zurück und die Krebszellen gewannen ihr aggressives Verhalten zurück, selbst ohne TUBB3. Das ordnet TUBB3 stromaufwärts von PTEN und AKT ein und beschreibt es als eine Art internen Regler für das Verhalten von Makrophagen.
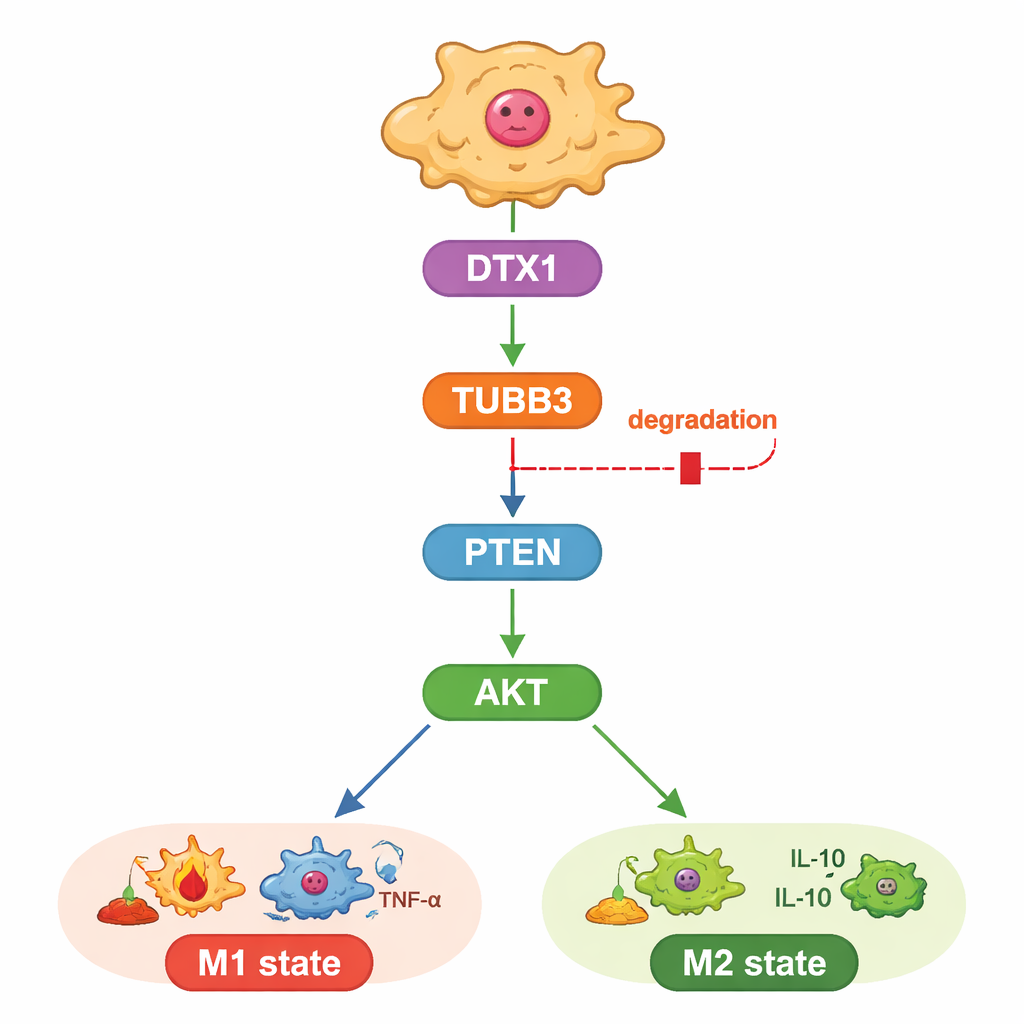
Ein eingebautes Müll-Label, das wieder eingeschaltet werden könnte
Schließlich fragten die Forschenden, warum TUBB3 in Lebertumoren so reichlich vorhanden ist. Durch die Kombination bioinformatischer Vorhersagen mit Expressionsdaten identifizierten sie ein Enzym namens DTX1, das zur Familie jener Proteine gehört, die andere Proteine für den Abbau markieren, als wahrscheinlichen Regulator. DTX1-Spiegel waren in Lebertumoren niedriger als im gesunden Gewebe und korrelierten mit besseren Patientenverläufen und einer stärkeren Präsenz von M1-typischen Makrophagen. In Zellen beschleunigte eine Erhöhung von DTX1 den Abbau von TUBB3, dämpfte die AKT-Aktivität und drängte Makrophagen in den tumorbekämpfenden Zustand, wodurch das Krebszellwachstum gehemmt wurde. Die Wiedereinführung zusätzlicher TUBB3-Mengen hob die Vorteile von DTX1 sowohl in Zellkulturen als auch in Maus-Tumoren auf. Zusammengenommen ziehen diese Ergebnisse eine klare Linie von DTX1 über TUBB3 und PTEN/AKT bis hin zum immunologischen Ton des Tumors.
Was das für die künftige Behandlung von Leberkrebs bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft, dass diese Arbeit ein bislang verborgenes Kontrollsystem in leberansässigen Immunzellen identifiziert, das darüber entscheidet, ob sie Krebs helfen oder ihn behindern. Wenn das Müll-Markierungsenzym DTX1 gering ist, akkumuliert TUBB3, ein Wachstumsweg wird aktiviert und Kupffer-Zellen gleiten in einen tumorfördernden Modus, der die Wirkung von Immuntherapien abschwächt. Die Wiederherstellung dieses Weges — durch Senkung von TUBB3, Erhöhung von DTX1 oder gezielte Feinabstimmung des PTEN/AKT-Signals — könnte lokale Immunabwehr reaktivieren und Behandlungen wie PD-1-Blocker wirksamer machen. Obwohl solche Strategien noch experimentell sind, unterstreichen sie das Potenzial, nicht nur die Tumorzellen, sondern auch die umgebenden immunologischen "Nachbarn" zu behandeln, die das Verhalten von Leberkrebs stark beeinflussen.
Zitation: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Schlüsselwörter: hepatozelluläres Karzinom, tumorassoziierte Makrophagen, Kupffer-Zellen, Immuntherapie, AKT-Signalweg