Clear Sky Science · de
Verdünnung und Entkoppelung der Aktivität von Körnerzellen im Gyrus dentatus durch Noradrenalin
Warum ein Moment der Erregung Erinnerungen schärfen kann
Augenblick, die uns aufrütteln — eine knappe Verkehrssituation, ein unerwarteter Kommentar, eine überraschende Wendung in einem Film — bleiben oft deutlich besser im Gedächtnis haften als ein ganz normaler Tag. Diese Studie untersucht einen zentralen Grund dafür: ein mit Erregung verbundenes Hirnchemikalium, Noradrenalin, verändert still und effizient, wie ein kritisches Gedächtnistor im Hippocampus Informationen filtert und trennt, sodass ähnliche Ereignisse später leichter voneinander zu unterscheiden sind.
Der Wächter für ähnliche Erfahrungen
Im Hippocampus liegt der Gyrus dentatus, eine Region, die wie ein Torwächter für neue Erinnerungen wirkt. Er empfängt umfangreiche Informationen vom entorhinalen Kortex — Signale darüber, wo wir uns befinden und was um uns geschieht — und wandelt diese in Aktivitätsmuster in den Körnerzellen um, seinen Hauptneuronen. Theorie und Experimente legen nahe, dass diese Muster „sparsam“ (nur wenige Zellen gleichzeitig aktiv) und „entkoppelt“ (unterschiedliche Erfahrungen aktivieren unterschiedliche Zellgruppen) sein müssen, damit sich Erinnerungen nicht vermischen. Wie diese Transformation auf Ebene spezifischer Zellen und Schaltkreise zustande kommt, war jedoch lange unklar.
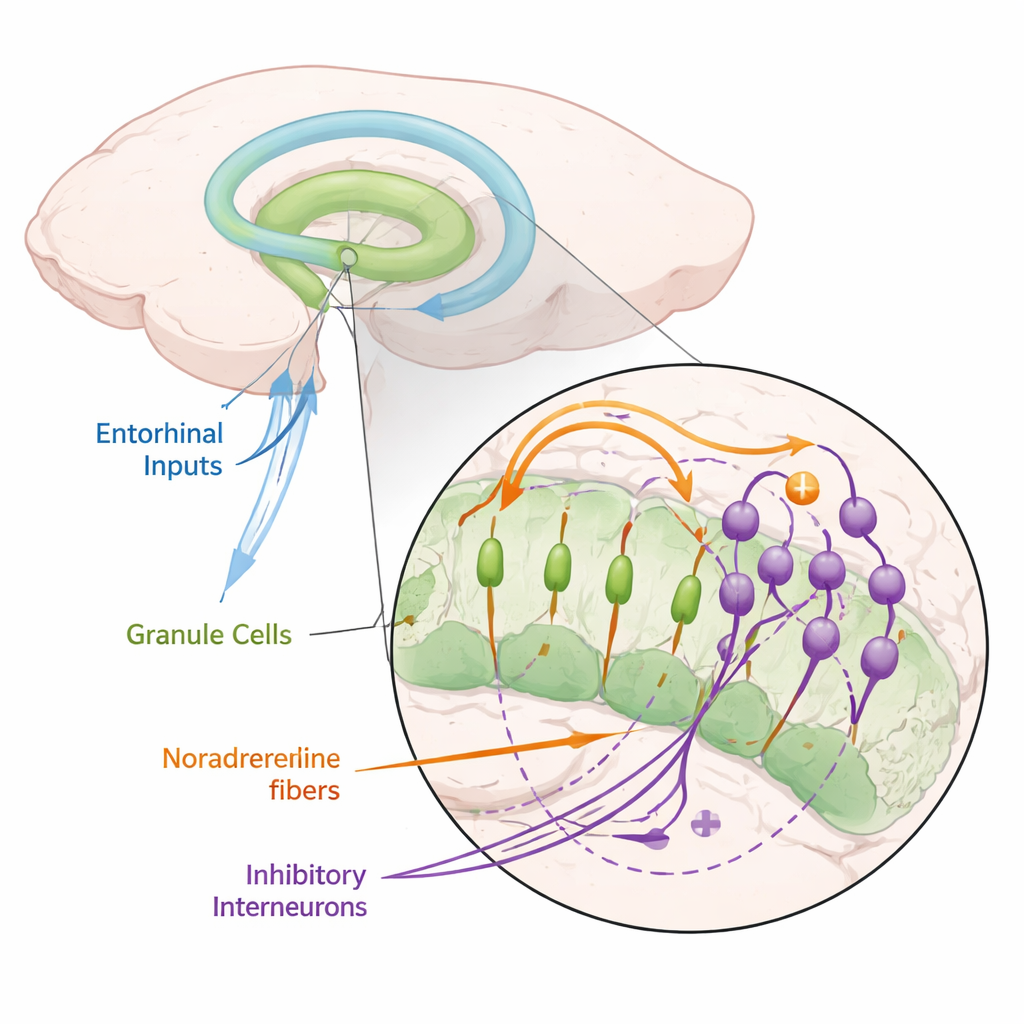
Ein Erregungsbotenstoff, der wichtige Gedächtniszellen dämpft
Die Autoren richteten ihren Fokus auf Noradrenalin, einen Neuromodulator, der von Neuronen in einem kleinen Hirnstammgebiet, dem Locus coeruleus, freigesetzt wird und bei Aufmerksamkeit, Neuheit und Stress aktiv wird. An Mäusen setzten sie lichtempfindliche Proteine in diesen noradrenergen Neuronen ein, sodass sich Noradrenalin auf Knopfdruck mit Lichtblitzen freisetzen ließ. Als sie den Hauptzuflussweg zum Gyrus dentatus stimulierten und von Körnerzellen aufzeichneten, stellten sie fest, dass Noradrenalin die Neigung dieser Zellen zu feuern stark verringerte. Diese Unterdrückung zeigte sich sowohl auf Ebene einzelner Neurone als auch in Populationssignalen und ließ sich reproduzieren, indem man Schnitte einfach in Noradrenalin badete. Das Blockieren von Noradrenalinrezeptoren hob den Effekt auf und zeigte damit, dass er wirklich von diesem chemischen Botenstoff abhängt.
Nicht schwächere Erregung, sondern stärkere Bremsen
Um zu verstehen, wie Noradrenalin Körnerzellen stumm schaltete, prüfte das Team naheliegende Möglichkeiten. Es veränderte weder signifikant das Ruhepotenzial noch den Eingangswiderstand der Körnerzellen, was bedeutet, dass ihre grundlegende Erregbarkeit weitgehend gleich blieb. Auch schwächte es nicht die exzitatorischen Ströme, die diese Zellen vom entorhinalen Kortex erhalten. Stattdessen konnte Noradrenalin die Körnerzellfeuerung nicht mehr unterdrücken, wenn GABAA-Rezeptoren blockiert waren, die die Hemmung vermitteln. Detaillierte Strommessungen zeigten, dass Noradrenalin gezielt eine schnelle, vorwärtsgerichtete Form der Inhibition verstärkte: eintreffende exzitatorische Signale trieben zunächst eine Gruppe von Interneuronen an, die dann die Körnerzellen rasch hemmten, bevor diese spiken konnten. Timing-Analysen ergaben, dass dieser noradrenalinsensitive hemmende Strom kurz nach der direkten Erregung, aber vor dem Feuern der Hauptpopulation der Körnerzellen ankam — ein Kennzeichen feedforward wirkender Bremsen.
Spezialisierte Hemmzellen, die das Timing durchsetzen
Welche Interneurone lieferten diese entscheidende Hemmung? Überraschenderweise waren Parvalbumin-exprimierende Zellen, denen lange eine dominante Rolle bei schneller feedforward-Kontrolle zugeschrieben wurde, nicht verantwortlich — Noradrenalin machte sie tatsächlich weniger aktiv. Stattdessen spielten Cholecystokinin-exprimierende Interneurone (CCK-Zellen) die Hauptrolle. Diese Zellen erhalten direkte Eingänge von denselben kortikalen Fasern, die Körnerzellen erregen, und feuern kurz bevor Körnerzellen aktiv werden, was auf eine feedforward-Funktion hinweist. Noradrenalin depolarisierte CCK-Zellen, machte sie leichter rekrutierbar und erhöhte die Wahrscheinlichkeit, dass Eingangssignale sie auslösten, ohne die Stärke jeder einzelnen hemmenden Verbindung zu verändern. Als die Forscher pharmakologisch die Ausgabe von CCK-Zellen blockierten, konnte Noradrenalin die Aktivität der Körnerzellen nicht mehr unterdrücken. Effektiv schaltet Noradrenalin einen Schaltkreis aus CCK-Interneuronen hoch, der ein sehr schmales Zeitfenster erzwingt, in dem eintreffende exzitatorische Spikes Körnerzellen erfolgreich antreiben können.
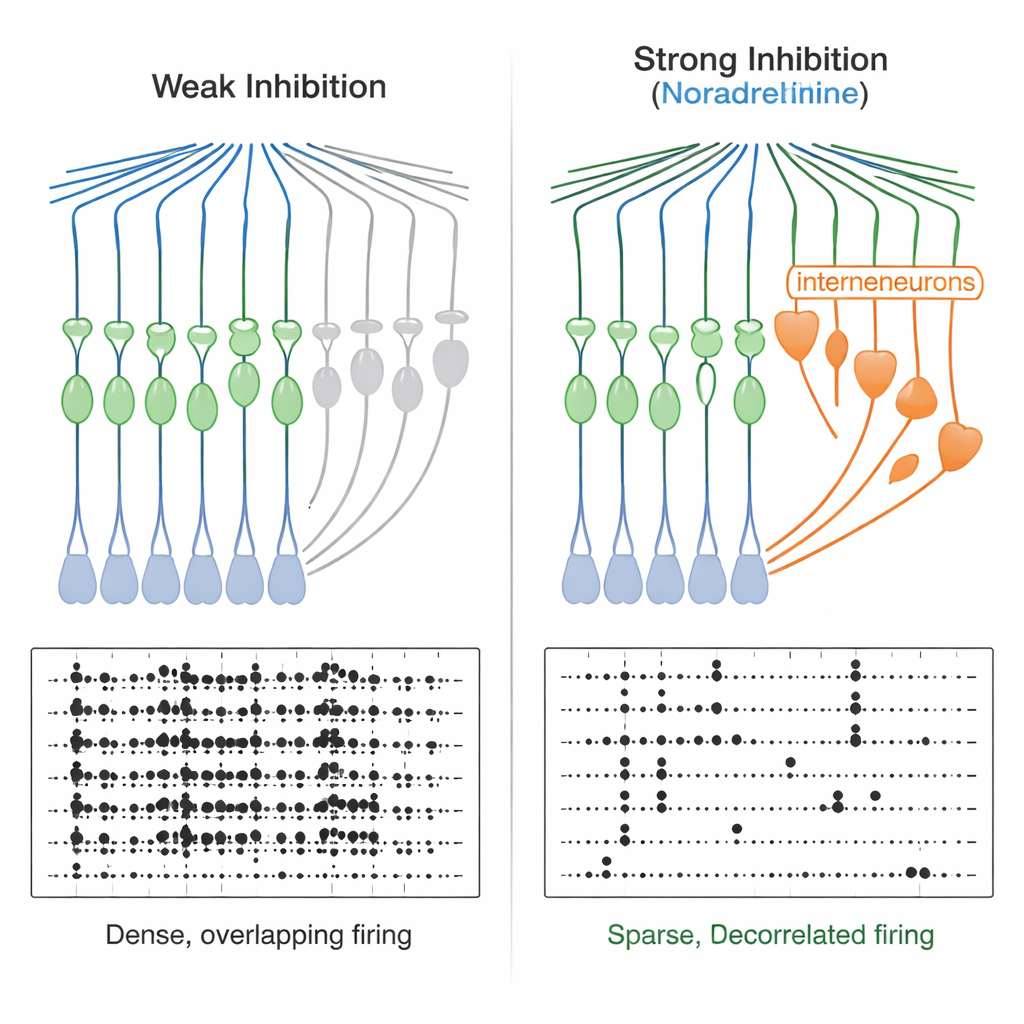
Von engen Zeitfenstern zu saubereren Gedächtniscodes
Dieses geschärfte Timing hat weitreichende Folgen. Als das Team Paare kurzer exzitatorischer Eingänge abgab, zeigte sich, dass Körnerzellen unter normalen Bedingungen Inputs, die um einige zehn Millisekunden auseinanderlagen, zu einem Spike integrieren konnten. Unter Noradrenalin schrumpfte dieses Fenster auf nur wenige Millisekunden — Körnerzellen reagierten nun nahezu ausschließlich auf hoch synchronisierte Eingänge. Computermodelle von Netzwerken bestätigten, dass eine stärkere und schnellere feedforward-Inhibition zu sparsamerer Ausgabe und geringeren Überlappungen zwischen Aktivitätsmustern führt und so die „Entkoppelung“ verbessert. Experimentell reagierten Körnerzellen bei zwei ähnlichen, aber nicht identischen Eingangsmustern mit deutlich unterscheidbareren Feuermustern in Gegenwart von Noradrenalin, sowohl in Einzelzellableitungen als auch in Calcium-Imaging über viele Zellen. Gleichzeitig wurde die Gesamtaktivität der Körnerzellen sparsamer.
Wie Erregung uns helfen kann, ähnliche Erinnerungen zu trennen
Für die nichtfachliche Leserschaft lautet die Schlussfolgerung: Noradrenalin, das freigesetzt wird, wenn wir aufmerksam oder emotional engagiert sind, macht ein zentrales Gedächtnisfilter im Hippocampus selektiver. Indem es eine spezifische Klasse inhibitorischer Nervenzellen aktiviert, verengt es das Zeitfenster, in dem Eingänge Körnerzellen auslösen können, sodass nur eng synchronisierte, bedeutsame Signale durchkommen. Das reduziert das Gesamtfeuerverhalten, verringert die Überlappung von Aktivitätsmustern und hilft dem Gehirn, ähnliche Erfahrungen — etwa zwei Klassenzimmer oder zwei Gespräche — als getrennte Erinnerungen statt als verschwommene Masse zu speichern. Die Arbeit enthüllt einen konkreten Schaltkreismechanismus, der momentane Erregung mit präziseren, weniger verwechselbaren Erinnerungen verbindet.
Zitation: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Schlüsselwörter: Noradrenalin, Gyrus dentatus, inhibitorische Interneurone, Mustertrennung, episodisches Gedächtnis