Clear Sky Science · de
Vorübergehende Proliferation durch reversible YAP- und Mitogensteuerung des Cyclin D1/p27-Verhältnisses
Wie Gewebe wissen, wann sie wachsen sollen
Wenn Sie Ihre Haut schneiden oder ein Organ verletzen, schalten benachbarte Zellen kurzzeitig vom Ruhezustand in einen Reparaturmodus und vermehren sich gerade genug, um die Wunde zu schließen, bevor sie wieder aufhören. Dieses Paper stellt eine auf den ersten Blick einfache Frage: Wie wissen Zellen, wann sie mit der Teilung beginnen und – ebenso wichtig – wann sie wieder aufhören, sodass die Heilung erfolgt, ohne in ein krebsähnliches Überwachstum umzuschlagen? Die Forscherinnen und Forscher entdecken einen eingebauten Balanceakt in den Zellen, der ein kräftiges Wachstumssignal nur vorübergehend einschaltet und dann zuverlässig wieder ausschaltet.
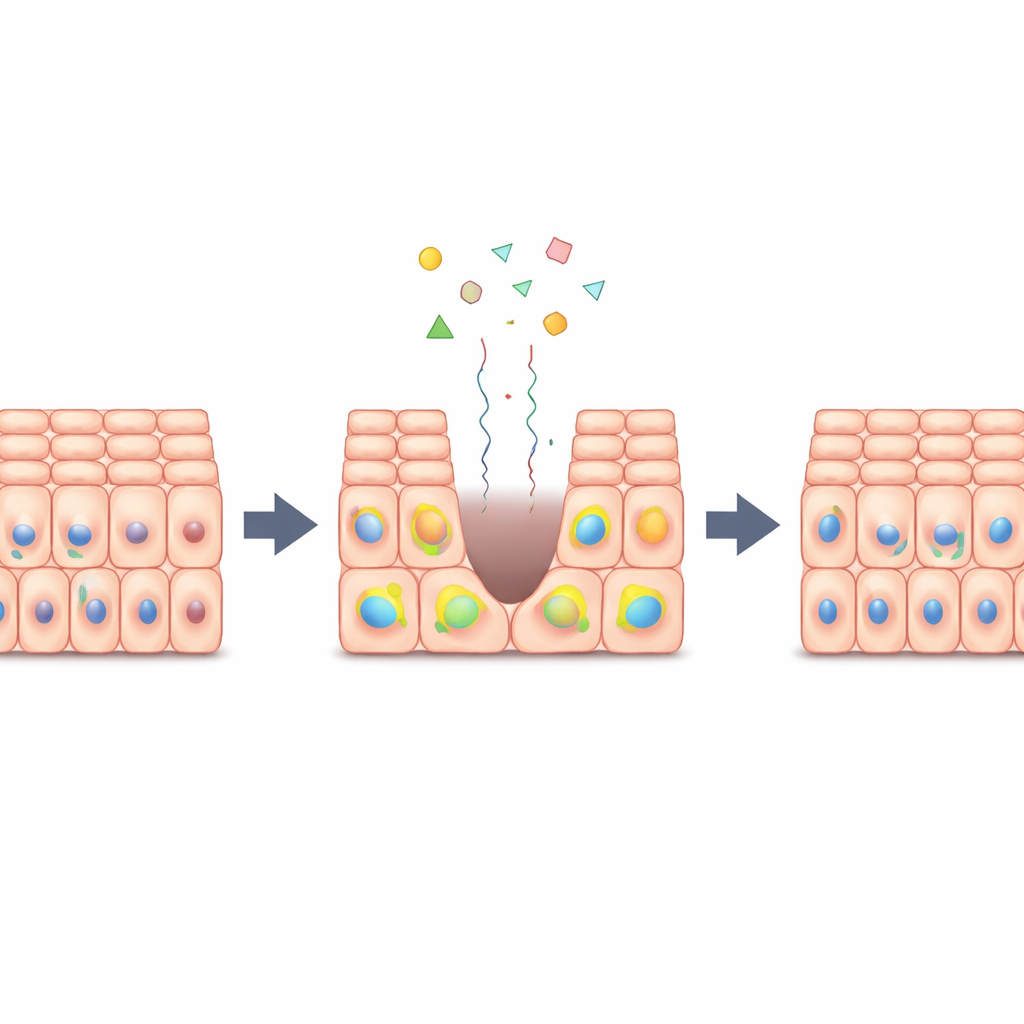
Eine Ampel für die Zellteilung
In vielen Geweben wirkt ein molekulares System namens Hippo–YAP wie ein Verkehrsregler für Zellwachstum. Wenn Gewebe dicht und intakt sind, hält Hippo ein Protein namens YAP aus dem Zellkern, und die Zellen bleiben ruhig. Bei Verletzung oder Dehnung des Gewebes wird Hippo gelockert, YAP wandert in den Zellkern und die Zellen werden zum Teilen angestupst. Die Autorinnen und Autoren untersuchten Tausende einzelner Epithelzellen, die als flache Schichten kultiviert wurden, und setzten sie verschiedenen Kombinationen aus Wachstumsfaktoren (Mitogenen), Medikamenten und Zelldichten aus. Sie fanden heraus, dass Wachstumsfaktor-Signale, physische Dichte und YAP-Aktivität nicht isoliert wirken; stattdessen laufen sie an einem einzigen internen Entscheidungspunkt zusammen, der bestimmt, ob jede Zelle wieder in den Zellzyklus eintritt.
Das entscheidende Verhältnis innerhalb der Zelle
Die zentrale Erkenntnis ist, dass Zellen ihre Teilung anhand eines Verhältnisses zweier Proteine im Zellkern während der frühen Wachstumsphase G1 entscheiden. Ein Protein, Cyclin D1, treibt die Zelle zur Teilung; das andere, p27, wirkt als Bremse. Nicht die absolute Menge eines der beiden Proteine ist entscheidend, sondern das Cyclin D1/p27-Verhältnis. Überschreitet dieses Verhältnis eine kritische Schwelle, wird ein Torwächterprotein namens Rb phosphoryliert und setzt die für die DNA-Replikation nötige Maschinerie frei, sodass die Zelle voranschreiten kann. Liegt das Verhältnis darunter, bleibt die Zelle im Ruhezustand. Das Team zeigte, dass künstliche Aktivierung von YAP oder das Blockieren von upstream-Bremsen im Hippo-Weg das Cyclin D1/p27-Verhältnis beständig erhöhte und Zellen über diese Schwelle trieb, selbst unter Bedingungen, die Zellen normalerweise ruhig halten würden.
Wie Signale von außen verstärkt und dann abgeschwächt werden
YAP wirkt nicht allein: Es erhöht die Empfindlichkeit der Zelle gegenüber von außen kommenden Wachstumssignalen. Die Forschenden nutzten RNA-Sequenzierung und Proteinanalyse und zeigten, dass YAP die Anzahl und Aktivität von Rezeptorproteinen an der Zelloberfläche erhöht, darunter Mitglieder der EGFR-Familie und andere Rezeptor-Tyrosinkinasen. Diese Rezeptoren speisen klassische Wachstumswege wie MEK–ERK und in geringerem Maße mTOR, die Cyclin D1 erhöhen und p27 senken, sodass das interne Verhältnis zugunsten der Teilung verschoben wird. Wichtig ist, dass diese Verstärkung kein schneller Ein-/Ausschalter ist. Selbst nachdem die YAP-Aktivität blockiert wurde, klingen die verstärkte Rezeptorsignalisierung und das erhöhte Cyclin D1/p27-Verhältnis nur allmählich über viele Stunden ab, sodass die Zellen Zeit haben, eine begrenzte Runde der Teilung zu vollenden, bevor die Bremsen wieder vollständig greifen.
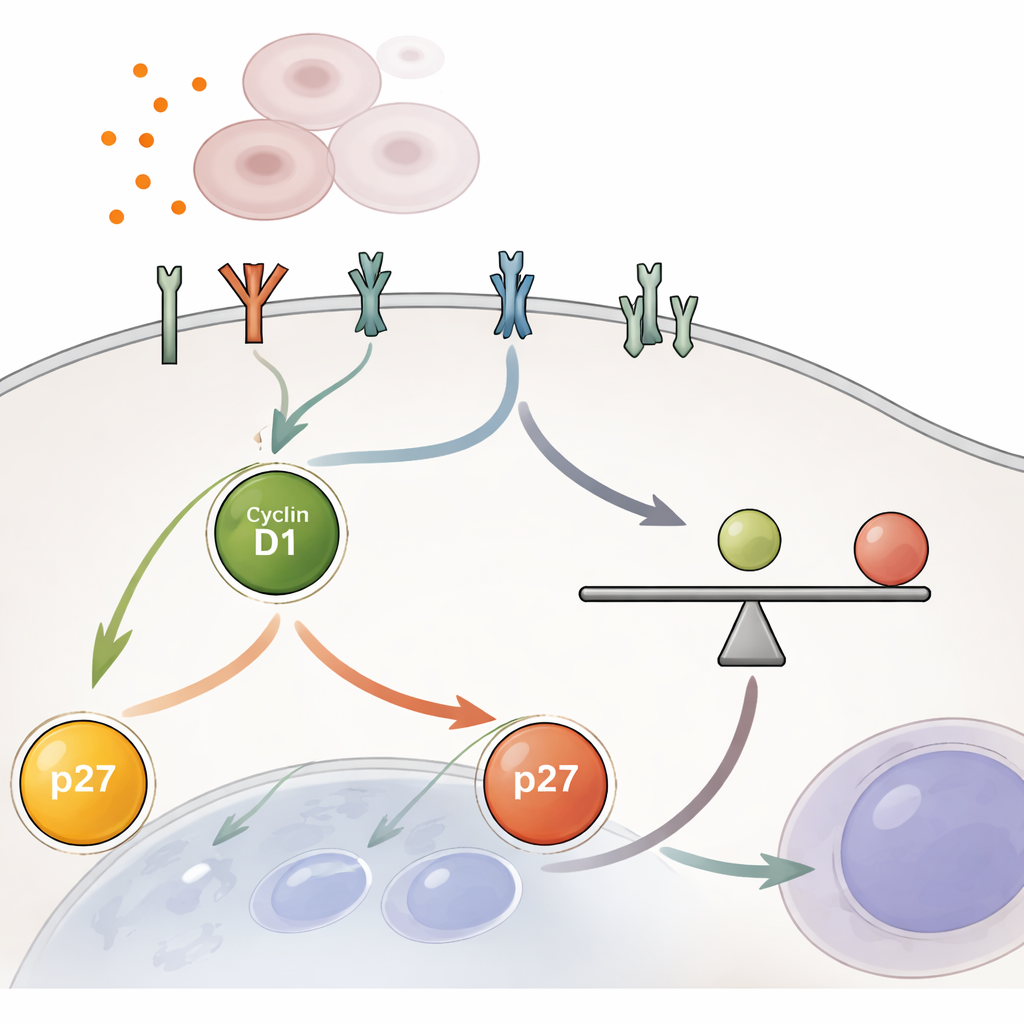
Eingebaute Schutzmechanismen gegen unkontrolliertes Wachstum
Die Studie untersucht außerdem, was passiert, wenn natürliche Bremsen auf YAP geschwächt sind, wie es in manchen Tumoren vorkommt. Das Entfernen eines Junction-Proteins namens Merlin, das normalerweise zur Aktivierung von Hippo beiträgt, entfaltete YAP teilweise und machte die Zellen empfindlicher gegenüber Wachstumsfaktoren. Doch selbst diese Zellen konnten durch sehr hohe lokale Zelldichte noch abgeschaltet werden, was die Kontaktinhibition wiederherstellte und das Cyclin D1/p27-Verhältnis senkte. Das zeigt, dass das System mehrere Kontrollebenen hat: Oberflächenrezeptoren, Hippo–YAP und das Cyclin D1/p27-Verhältnis tragen alle dazu bei, zu entscheiden, ob Zellen mit der Teilung fortfahren.
Warum das für Heilung und Krebs wichtig ist
Für eine allgemeine Leserschaft ist die zentrale Botschaft, dass Gewebereparatur von einem vorübergehenden, sich selbst begrenzenden Wachstumsprogramm gesteuert wird. YAP-Aktivierung und verstärkte Rezeptorsignalisierung heben das Cyclin D1/p27-Verhältnis über eine Schwelle, sodass Zellen sich teilen und Schäden reparieren können. Wenn sich die Zellen teilen und das Gewebe wieder dichter wird, schalten Kontaktinhibition, YAP und Rezeptorsignale allmählich ab, das Verhältnis sinkt und die Teilung stoppt. Wenn dieser Zeitgebermechanismus gestört ist – zum Beispiel durch anhaltende YAP-Aktivierung oder Verlust upstreamer Bremsen – können Zellen unempfindlich gegenüber Dichte werden und weiter teilen, ein Schritt in Richtung Krebs. Das Verständnis dieses verhältnisbasierten Entscheidungssystems könnte helfen, regenerative Therapien zu entwickeln, die die Reparatur sicher fördern, ohne unkontrolliertes Wachstum auszulösen.
Zitation: Ferrick, K.R., Upadhya, S.W., Fan, Y. et al. Transient proliferation by reversible YAP and mitogen control of the cyclin D1/p27 ratio. Commun Biol 9, 340 (2026). https://doi.org/10.1038/s42003-026-09590-2
Schlüsselwörter: YAP-Signalgebung, Kontrolle des Zellzyklus, Geweberegeneration, Kontaktinhibition, Gleichgewicht Cyclin D1 p27