Clear Sky Science · de
Mehrfach-organoidale Schleifen: zerebrale Connectoide zeigen verbesserte neuronale Netzwerkdynamik und sequenzspezifische Entrainment
Kleine verbundene Gehirnschaltkreise bauen
Unsere Gehirne funktionieren nicht als isolierte Zellinseln. Gedanken, Erinnerungen und Bewegungen entstehen aus Signalen, die entlang weitreichender Verbindungsstraßen rasen und viele Hirnregionen miteinander koppeln. Diese Studie zeigt, wie Forschende solche Verdrahtungsmuster jetzt im Labor nachbilden können, indem sie mehrere miniaturisierte, gehirnähnliche Gewebe — sogenannte Organoide — physisch zu geschlossenen Schleifen verbinden. Diese „Loop-Connectoide" beginnen, reichere und lebensechtere Aktivitätsmuster zu zeigen, und bieten damit eine neue Möglichkeit, zu untersuchen, wie komplexe Gehirnschaltkreise funktionieren und wie sie bei Erkrankungen fehlregulieren können.
Von Mini-Gehirnen zu Mini-Netzwerken
Gehirn-Organoide sind winzige Gewebekugeln, die aus menschlichen Stammzellen gezüchtet werden und sich selbst in Strukturen organisieren, die Teilen des sich entwickelnden Gehirns ähneln. Sie enthalten viele Arten von Neuronen und Stützzellen und können eigenständig elektrische Signale erzeugen. Bislang konzentrierten sich die meisten Organoid-Experimente auf einzelne Organoide oder einfache Fusionen von zwei Regionen, was vor allem lokale Verschaltungen abbildet. Die Autorinnen und Autoren wollten darüber hinausgehen und Labormodelle schaffen, die Fernverbindungen zwischen mehreren „Regionen“ enthalten — näher an den Kommunikationslinien des echten Gehirns, die Denken, Wahrnehmung und Verhalten tragen.
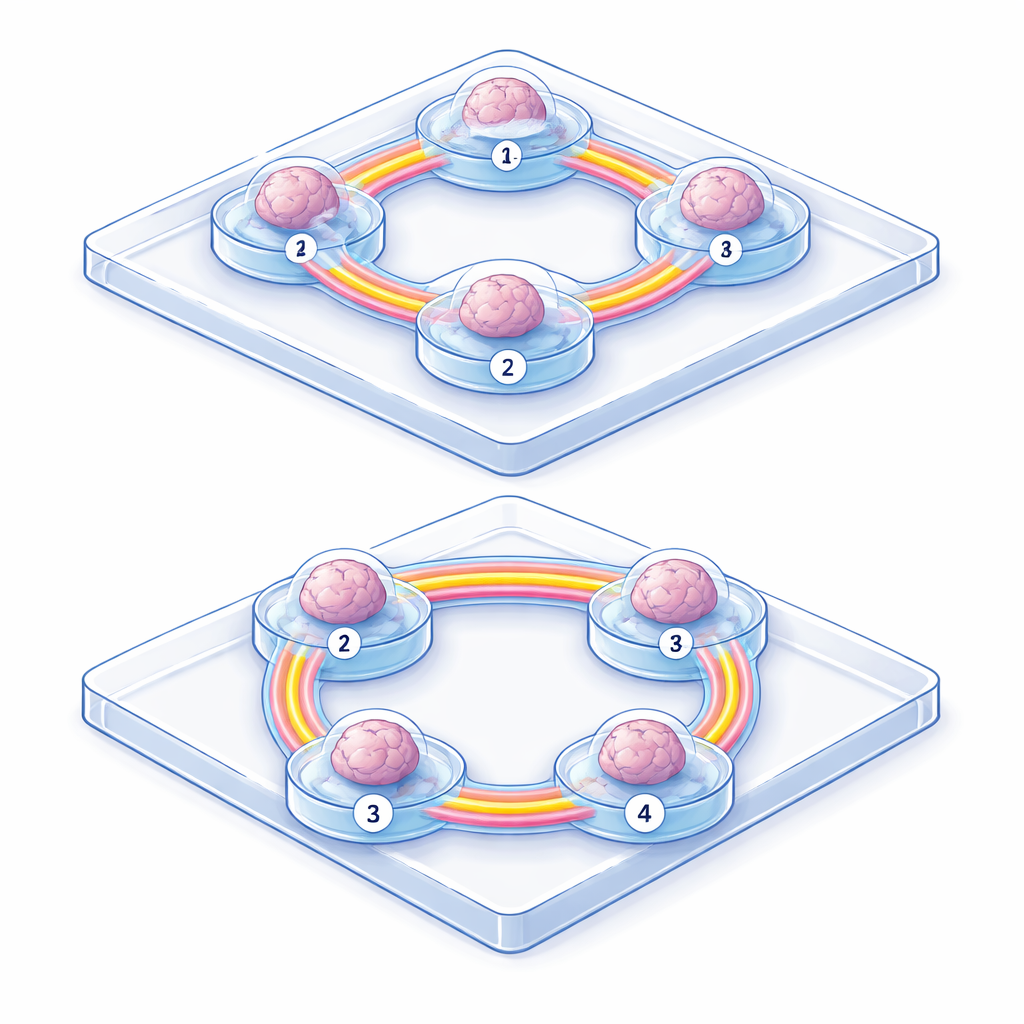
Eine Ringstruktur sprechender Organoide konstruieren
Um diese Netzwerke zu erzeugen, züchtete das Team zerebrale Organoide aus humanen induzierten pluripotenten Stammzellen und setzte sie dann in maßgeschneiderte mikrofluidische Chips. Jeder Chip enthielt zwei, drei oder vier runde Kammern, die durch schmale Kanäle verbunden waren. Sobald ein Organoid in einer Kammer ruhte, konnten seine Nervenfasern (Axone) nur entlang der Kanäle wachsen, wo sie sich natürlich zu Bündeln zusammenfügten und innerhalb von etwa zwei Wochen Nachbarorganoide überbrückten. Bei drei oder vier Organoiden in einem Gerät bildeten diese Bündel einen geschlossenen Ring bzw. eine Schleife. Unter dem Mikroskop blieben die Bündel intakt, selbst wenn das Kunststoffgehäuse entfernt wurde — ein Nachweis dafür, dass die Organoide sich physisch zu einem stabilen Schaltkreis verbunden hatten.
Reichere, längere und stärker strukturierte Gehirnaktivität
Als Nächstes zeichneten die Forschenden elektrische Signale von jedem Organoid mit einem Raster winziger Elektroden auf. Mit fortschreitenden Wochen wurden die Feuermuster der Organoide zunehmend synchronisiert, besonders zwischen solchen, die direkt durch Axonbündel verbunden waren. Netzwerke mit mehreren Organoiden hatten mehr aktive Aufnahmepunkte und insgesamt mehr Verbindungen, wodurch sich eine modulare Struktur ergab: Jedes Organoid fungierte wie ein „lokaler Knoten“, der mit seinen Nachbarn verbunden ist. Diese Mehrfach-Organoid-Schleifen zeigten häufigere Aktivitätsausbrüche und längere Phasen anhaltender Feuertätigkeit als einzelne Organoide. Zeitpunkt und Größe dieser Ausbrüche wurden variabler, wenn drei oder vier Organoide verbunden waren — ein Hinweis auf ein reichhaltigeres Repertoire an Aktivitätsmustern, das echten Gehirnnetzwerken näherkommt.
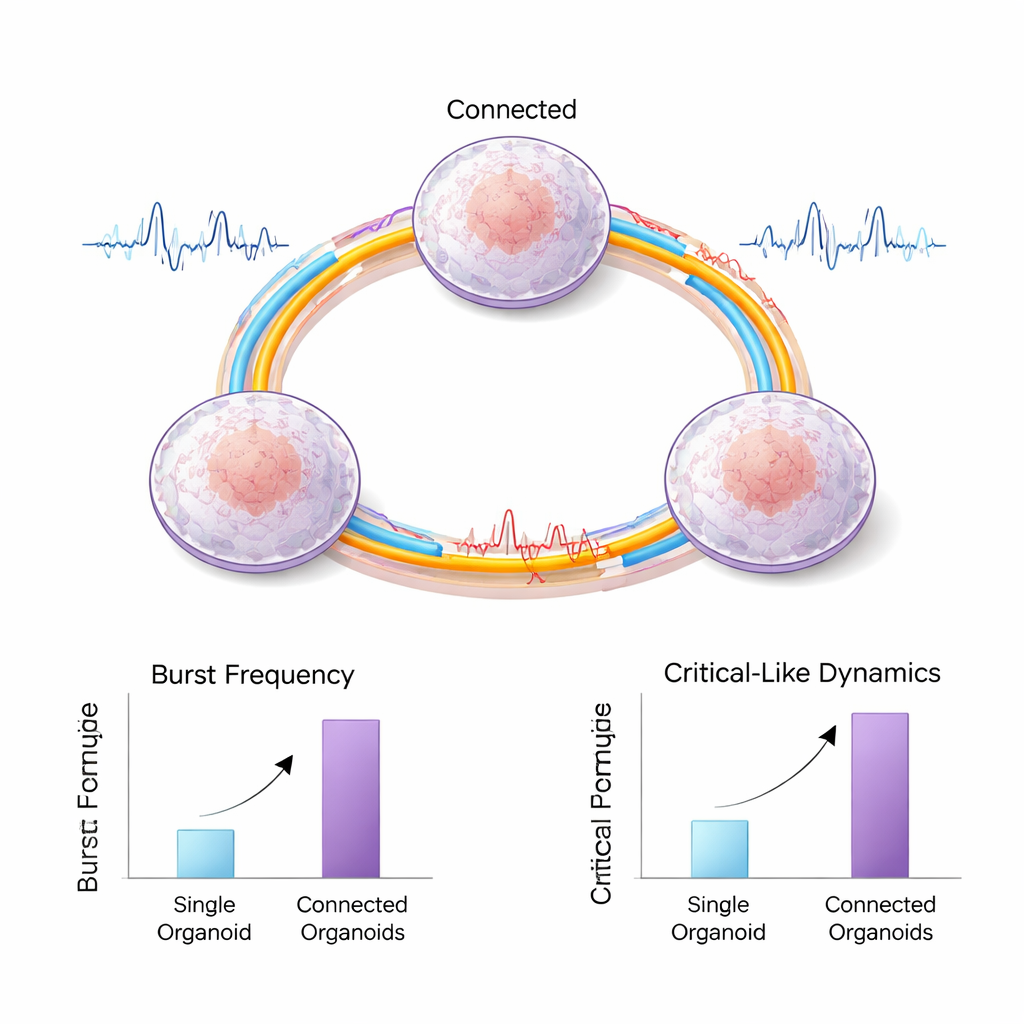
Auf eine optimale Balance gehirnähnlichen Verhaltens zusteuern
Das Team untersuchte außerdem, ob diese Netzwerke nahe der sogenannten „Kritikalität“ operieren — einem Sweet Spot zwischen zu wenig und zu viel Aktivität, der als förderlich für flexible Informationsverarbeitung im Gehirn gilt. Durch die Analyse von Aktivierungskaskaden, sogenannten „neuronal avalanches", fanden sie heraus, dass verbundene Organoide eher wie Systeme an diesem kritischen Punkt agierten als einzelne Organoide. Wirkstoffe, die wesentliche exzitatorische oder inhibitorische chemische Signale blockieren, verschoben die Ausbruchsmuster und bestätigten damit, dass ein Gleichgewicht aus Stimulation und Hemmung entscheidend für die komplexe Dynamik ist. Schließlich führten die Wissenschaftlerinnen und Wissenschaftler eine optogenetische Stimulation durch, bei der drei verbundene Organoide über viele Stunden in einer wiederholten Sequenz beleuchtet wurden; später tendierte die spontane Netzwerkaktivität dazu, diese Sequenz nachzuspielen. Dieses sequenzspezifische Entrainment verschwand, als ein Hemmstoff für plastikitätsrelevante Enzyme hinzugefügt wurde — ein Hinweis darauf, dass die Loop-Connectoide erfahrungsabhängige Veränderungen durchlaufen können, ein grundlegendes Merkmal von Lernen.
Warum diese kleinen Schleifen wichtig sind
Vereinfacht gesagt zeigt die Studie, dass wenn mehrere Mini-Gehirne in einer kontrollierten Schleife verschaltet werden, das Gesamtnetzwerk eher wie ein echtes Gehirn agiert als jedes einzelne Teil für sich. Die verbundenen Organoide feuern in längeren, variableren Ausbrüchen, befinden sich näher an einem effizienten Betriebszustand und lassen sich auf das Wiederholen gelernter Aktivitätsmuster einschwören. Da das System modular und justierbar ist, lässt es sich erweitern, umverdrahten und schließlich mit Zellen von Patientinnen und Patienten bestücken. Damit sind Loop-Connectoide eine vielversprechende Plattform, um zu erforschen, wie großskalige Gehirnschaltkreise sich entwickeln, wie sie bei Erkrankungen wie Autismus oder Demenz versagen und wie neue Medikamente oder Stimulationsverfahren gesunde Aktivitätsmuster wiederherstellen könnten.
Zitation: Duenki, T., Ikeuchi, Y. Multi-organoid loop cerebral connectoids exhibit enhanced neuronal network dynamics and sequence-specific entrainment. Commun Biol 9, 302 (2026). https://doi.org/10.1038/s42003-026-09589-9
Schlüsselwörter: Gehirn-Organoide, neuronale Netzwerke, mikrofluidische Schleifen, neuronale Dynamik, optogenetische Stimulation