Clear Sky Science · de
Epitheliale–mesenchymale Plastizität und Immunsuppression bei Hundekarzinomen zeigen artsübergreifende Hochregulierung von CD109
Krebs-Hinweise, versteckt in Hunden
Viele Haushunde entwickeln Mammatumoren, die den menschlichen Brustkrebserkrankungen auffallend ähneln. Diese Studie nutzt diese natürlich entstandenen canine Tumoren, um eine drängende Frage der Onkologie zu beantworten: Warum schaffen es manche Tumoren, die Immunantwort zu unterdrücken, während andere weiterhin verwundbar bleiben. Indem die Forschenden beobachten, wie sich Zellform und -verhalten von Hundetumoren verändern und wie Immunzellen darauf reagieren, enthüllen sie einen gemeinsamen, artsübergreifenden Mechanismus der Tumor-Immunevasion mit direkten Implikationen für menschliche Patientinnen und Patienten.
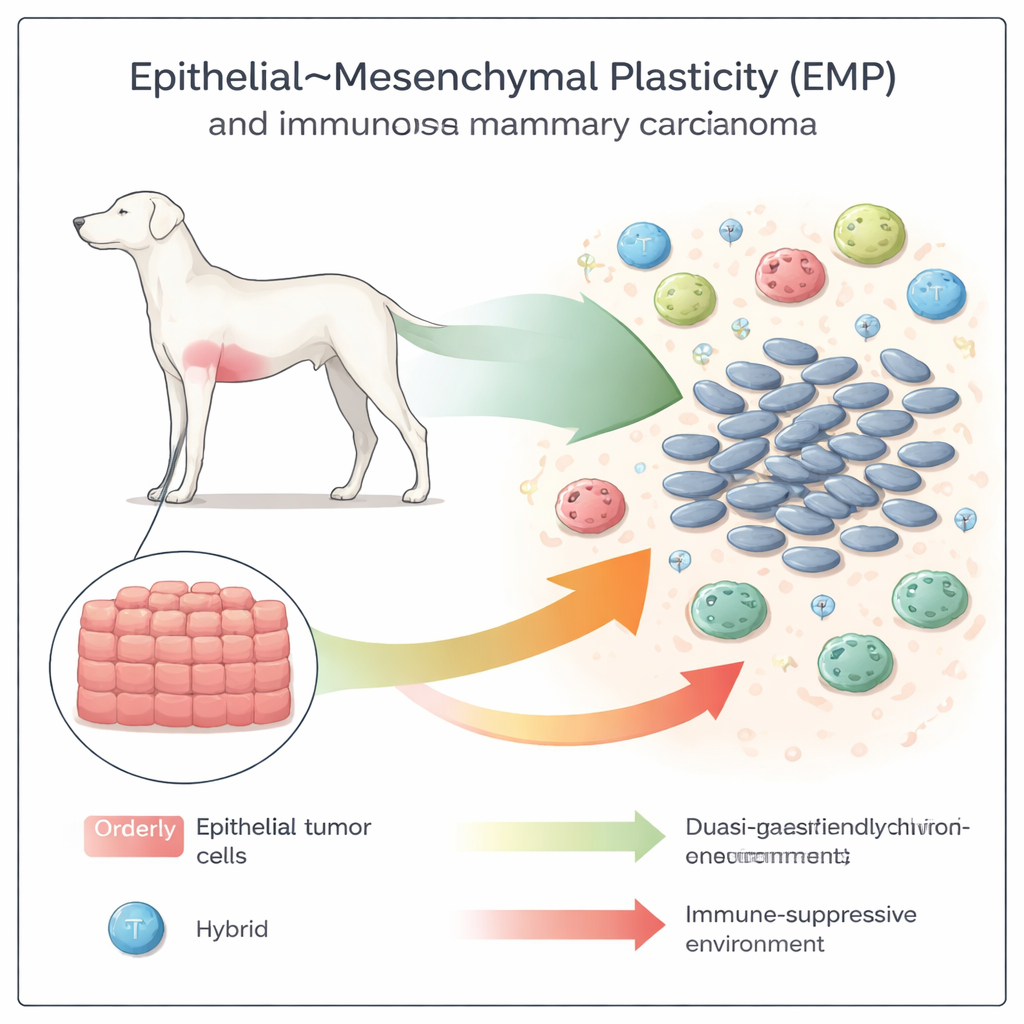
Gestaltwandelnde Tumorzellen
Krebszellen sind nicht auf eine Identität festgelegt. Sie können von einer ordentlichen, ziegelsteinartigen „epithelialen“ Form zu einer lockereren, beweglicheren „mesenchymalen“ Form wechseln und sich oft irgendwo dazwischen einpendeln. Dieses flexible Spektrum, epithelial–mesenchymale Plastizität (EMP) genannt, ist bereits dafür bekannt, Tumoren beim Eindringen und Ausbreiten zu helfen. In caninen Mammakarzinomen untersuchte das Team über 50 Tumoren und fand, dass hochgradige, gefährlichere Krebserkrankungen stärkere Anzeichen dieses Gestaltwandels zeigten: sie verloren geordnete Strukturen, gewannen spindelförmige Zellen und veränderten Schlüsseloberflächenproteine, die Zellen normalerweise zusammenhalten.
Wie Tumoren die Immunabwehr ausschalten
Die Forschenden fragten dann, ob dieser zelluläre Umbau mit Veränderungen in der immunologischen „Nachbarschaft“ des Tumors einhergeht. In niedriggradigen, eher epithelialen Tumoren waren T‑Zellen — insbesondere die zytotoxischen Typen, die Krebs zerstören können — relativ zahlreich. Mit einer Verschiebung der Tumoren in Richtung quasi‑mesenchymaler Zustände und höherer histologischer Grade gingen die Gesamtzahlen an T‑Zellen zurück, während der Anteil regulatorischer T‑Zellen und pro‑tumoraler M2‑ähnlicher Makrophagen zunahm. Anders gesagt: Je plastischer und invasiver die Zellen wurden, desto mehr wandelte sich das umgebende Mikroumfeld von immunfreundlich zu immunsuppressiv, was Muster widerspiegelt, die zuvor nur in Mausmodellen beobachtet wurden.
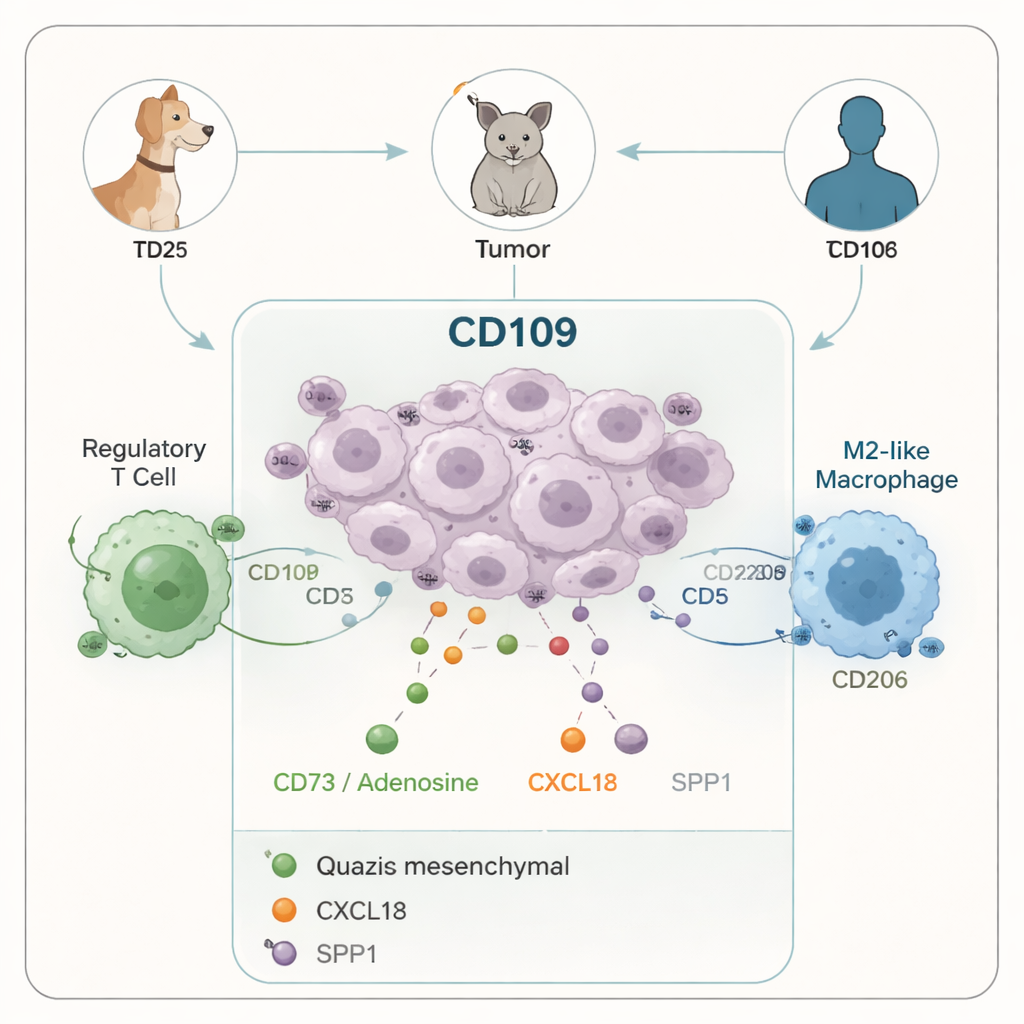
Signale, die die falsche Hilfe anziehen
Um aufzudecken, wie diese Tumoren ihre Umgebung umprogrammieren, sequenzierten die Forschenden RNA aus einer gezielten Auswahl caniner Tumoren, die epitheliale, gemischte und quasi‑mesenchymale Zustände abdeckten. Heterogene und quasi‑mesenchymale Tumoren schalteten eine Reihe sekretierter Faktoren ein, die dafür bekannt sind, Immunantworten zu dämpfen und suppressive Zellen anzuziehen. Dazu gehörten Moleküle wie CD73, das Adenosin erzeugt und Immunzellen «beruhigen» kann, sowie Chemokine wie CXCL12 und SPP1, die helfen, Makrophagen und andere Unterstützer zu rekrutieren, die letztlich das Tumorwachstum fördern. Bemerkenswert war, dass selbst Tumoren mit nur einem Bruchteil quasi‑mesenchymaler Zellen starke immunsuppressive Signaturen zeigten, was darauf hindeutet, dass eine kleine, aggressive Subpopulation das Verhalten des gesamten Tumors bestimmen kann.
Ein neuer Akteur: CD109 bei Hunden, Mäusen und Menschen
Unter den vielen Molekülen, die mit EMP anstiegen, stach eines hervor: ein Oberflächen‑Glykoprotein namens CD109. In caninen Mammatumoren waren CD109‑Spiegel in stärker mesenchymalen, höhergradigen und basalähnlichen Karzinomen erhöht und korrelierten tendenziell mit schlechteren Prognosen. Beim Durchsuchen vorhandener Maus‑ und Menschendatensätze zeigten die Autorinnen und Autoren, dass CD109 auch in quasi‑mesenchymalen Maus‑Brusttumoren und in aggressiven, basalähnlichen menschlichen Brustkrebszellen erhöht ist. Ein wichtiger Regulator des Zellzustandswechsels, der Transkriptionsfaktor Snail, bindet direkt in der Nähe des CD109‑Gens und verknüpft es damit mechanistisch mit dem EMP‑Programm. Einzelzellanalysen bestätigten, dass die CD109‑Expression in den am stärksten mesenchymal‑artigen Krebszellen konzentriert ist und mit anderen immunsuppressiven Signalen koauftritt.
Geteilte Strategien zur Immunflucht in vielen Tumoren
Um zu prüfen, wie allgemein diese Muster sind, analysierte das Team RNA‑Daten aus mehreren anderen caninen Tumoren epithelialen Ursprungs neu, darunter orale Plattenepithelkarzinome, invasive Urothelkarzinome und pulmonale Karzinome. In diesen Tumortypen korrelierten EMP‑Marker konsequent mit höherer Expression immunsuppressiver parakriner Faktoren — insbesondere CD73, SPP1 und CXCL12 — wobei die Verbindung von CD109 mit EMP in Mammakarzinomen am stärksten und spezifischsten erschien. Das deutet auf ein gemeinsames „Spielbuch“ hin: Wenn Tumoren plastischere, invasivere Zustände annehmen, schalten sie zugleich chemische Signale an, die das immunologische Umfeld zu ihren Gunsten umgestalten.
Was das für Hunde und Menschen bedeutet
Für nichtfachliche Leserinnen und Leser ist die Kernaussage: Wenn Krebszellen bei Hunden lernen, Gestalt und Identität zu wechseln, lernen sie auch, das Immunsystem zu beruhigen und modernen Immuntherapien zu widerstehen. Da canine Tumoren die menschliche Erkrankung eng nachbilden, weisen diese Befunde auf gemeinsame Zielstrukturen — wie CD73 und das neu hervorgehobene CD109 — hin, die blockiert werden könnten, um die Immunantwort in beiden Spezies wieder zu wecken. Künftig könnte die Messung dieser Moleküle helfen, Hochrisikotumoren zu identifizieren und Kombinationsbehandlungen zu steuern, die nicht nur die Krebszellen selbst angreifen, sondern auch den von ihnen aufgebauten Schutzschild auflösen.
Zitation: Bakhle, K., Nelissen, S., Li, L. et al. Epithelial-mesenchymal plasticity and immunosuppression in canine carcinomas reveals cross-species upregulation of CD109. Commun Biol 9, 303 (2026). https://doi.org/10.1038/s42003-026-09587-x
Schlüsselwörter: kanine Mammakarzinome, epitheliale mesenchymale Plastizität, tumorales immunes Mikroumfeld, CD109, Resistenz gegen Krebsimmuntherapie