Clear Sky Science · de
Sex- und ätiologiespezifische Effekte auf prädiktive Verarbeitung im Colliculus inferior bei zwei Rattenmodellen des Autismus
Warum unser Gehirn sich für überraschende Geräusche interessiert
Stellen Sie sich vor, Sie gehen eine belebte Straße entlang und plötzlich hupt ein Auto. Ihr Gehirn markiert dieses Geräusch sofort als wichtig gegenüber dem Hintergrundlärm. Viele autistische Menschen erleben akustische Welten anders – manchmal empfinden sie Alltagsgeräusche als überwältigend, manchmal nehmen sie sie kaum wahr. Diese Studie stellt eine einfache, aber grundlegende Frage: Verarbeiten Männchen und Weibchen mit autismusähnlichen Merkmalen bereits auf einer sehr frühen Hörstufe im Mittelhirn Klangüberraschungen unterschiedlich, und spielt es eine Rolle, ob diese Merkmale genetisch oder durch die pränatale Umgebung verursacht sind?
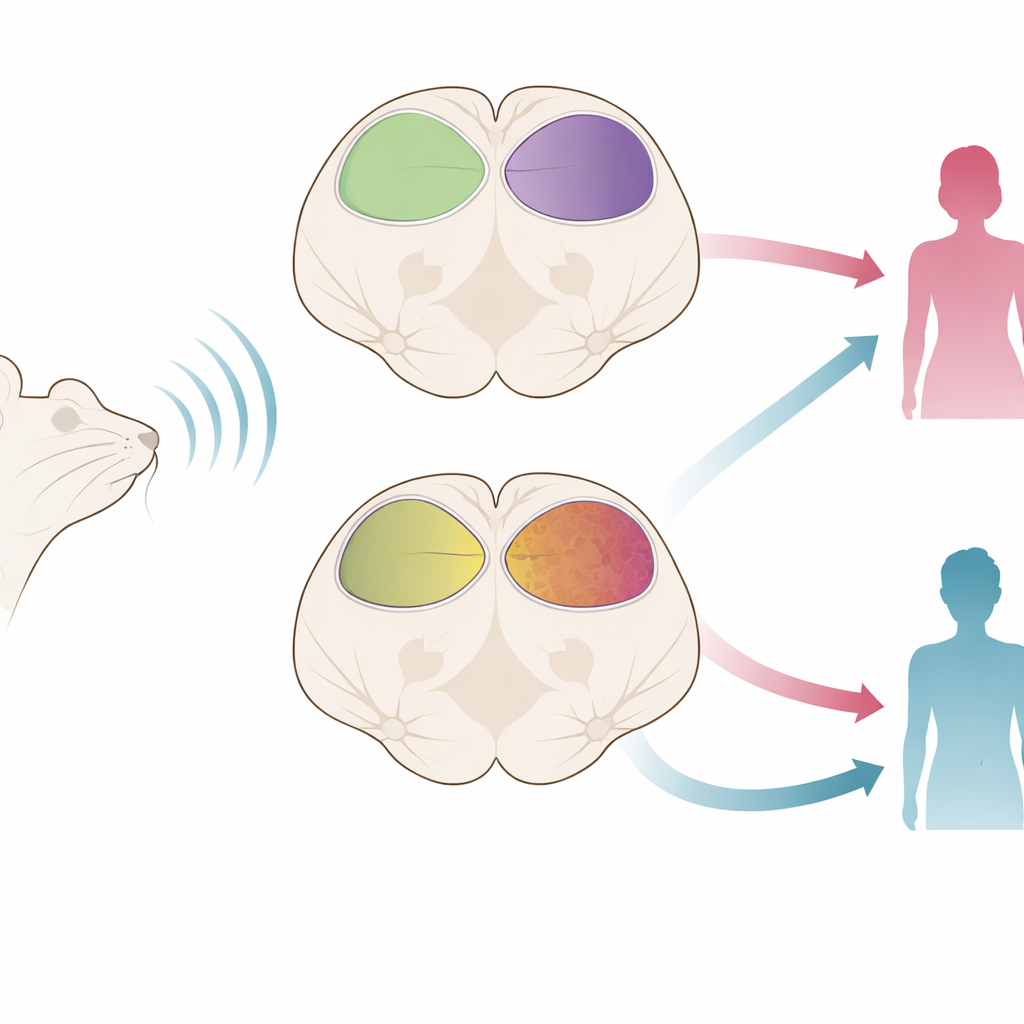
Ein schallaufnehmender Knoten tief im Gehirn
Die Arbeit konzentriert sich auf eine kleine Struktur im Mittelhirn, den Colliculus inferior, ein wichtiges Kreuzungspunkt, an dem Schallinformationen aus den Ohren erstmals mit Signalen aus höheren Hirnarealen zusammenlaufen. Bei Ratten wie beim Menschen enthält dieses Zentrum zwei Hauptwege: einen „klassischen“ Pfad, der Klangdetails wie Tonhöhe und Lautstärke treu überträgt, und einen flexibleren Pfad, der Kontext, Neuheit und Relevanz gewichtet. Die Forschenden verwendeten zwei etablierte Rattenmodelle, die unterschiedliche Ursachen von Autismus nachahmen: eines mit einer Mutation in einem Gen, das mit Synapsenfunktion verknüpft ist (Grin2b), und ein anderes, bei dem sich Embryonen während der Entwicklung dem Medikament Valproinsäure aussetzten, einem bekannten umweltbedingten Risikofaktor.
Untersuchung, wie Neuronen auf regelmäßige und abweichende Töne reagieren
Um zu testen, wie diese Hirnschaltkreise Muster verfolgen, zeichneten die Forschenden die Aktivität einzelner Neuronen auf, während sie einfache Tonsequenzen über einen winzigen Lautsprecher in ein Ohr abspielten. In einer Sequenz wurde ein einzelner Ton immer wiederholt, mit einem seltenen abweichenden Ton dazwischen – ähnlich wie wenn ein Trommelschlag plötzlich anders klingt. In einer anderen Sequenz stiegen oder fielen die Töne in perfekter Vorhersehbarkeit wie eine Treppe ohne Wiederholungen. Durch den Vergleich der Reaktionen jedes Neurons auf wiederholte, geordnete und seltene Töne konnten die Forschenden drei Bestandteile prädiktiven Hörens trennen: wie stark ein Neuron sich an Wiederholung „gewöhnt“, wie stark es reagiert, wenn ein Muster gebrochen wird, und die Gesamthöhe seiner Mismatch-Antwort auf Überraschung.
Verschiedene Ausgangspunkte für Männchen und Weibchen
Sogar bevor Geräusche eintrafen, zeigten weibliche Kontrollratten eine höhere spontane Feuerrate in diesem Mittelhirnknoten als Männchen, was auf einen von Natur aus aktiveren Basiszustand hindeutet. Bei abgespielten Tönen reagierten Kontrollweibchen weniger stark auf wiederholte Töne und auf geordnete Sequenzen als Männchen, erzeugten aber stärkere Signale, die speziell mit Verletzungen erwarteter Muster verknüpft waren. Einfach ausgedrückt betonten männliche Gehirne in dieser Region die stabile Verfolgung regelmäßiger Klangstrukturen, während weibliche Gehirne stärker darauf fokussierten, wenn diese Struktur gebrochen wurde. Diese geschlechtsgebundenen Stile traten sowohl im klassischen als auch im kontextsensitiven Pfad des Colliculus inferior auf.
Wie autismusähnliche Veränderungen frühe Klangvorhersage umgestalten
Das Einführen autismusverknüpfter Risikofaktoren verschob diese Muster, und die Verschiebungen hingen stark von Geschlecht und Pfad ab. Bei Weibchen verstärkten sowohl die Grin2b-Mutation als auch die pränatale Valproinsäureexposition die gesamte Mismatch-Antwort auf überraschende Töne, vor allem durch eine verstärkte Anpassung an Wiederholung, während in einigen Fällen das reine „Fehler“-Signal bei Musterverletzungen abgeschwächt wurde. Pränatale Valproinsäure senkte außerdem die ohnehin hohe Basisaktivität der Weibchen, besonders im kontextsensitiven Pfad. Bei Männchen waren die Effekte begrenzter: Pränatale Valproinsäure verringerte ihre Mismatch-Antworten im kontextsensitiven Pfad, während die Grin2b-Mutation nur geringen Einfluss auf frühe Vorhersagesignale hatte. Diese Befunde deuten auf eine besondere Verwundbarkeit – und Plastizität – des nicht-klassischen, kontextorientierten Pfads hin, insbesondere bei Weibchen.
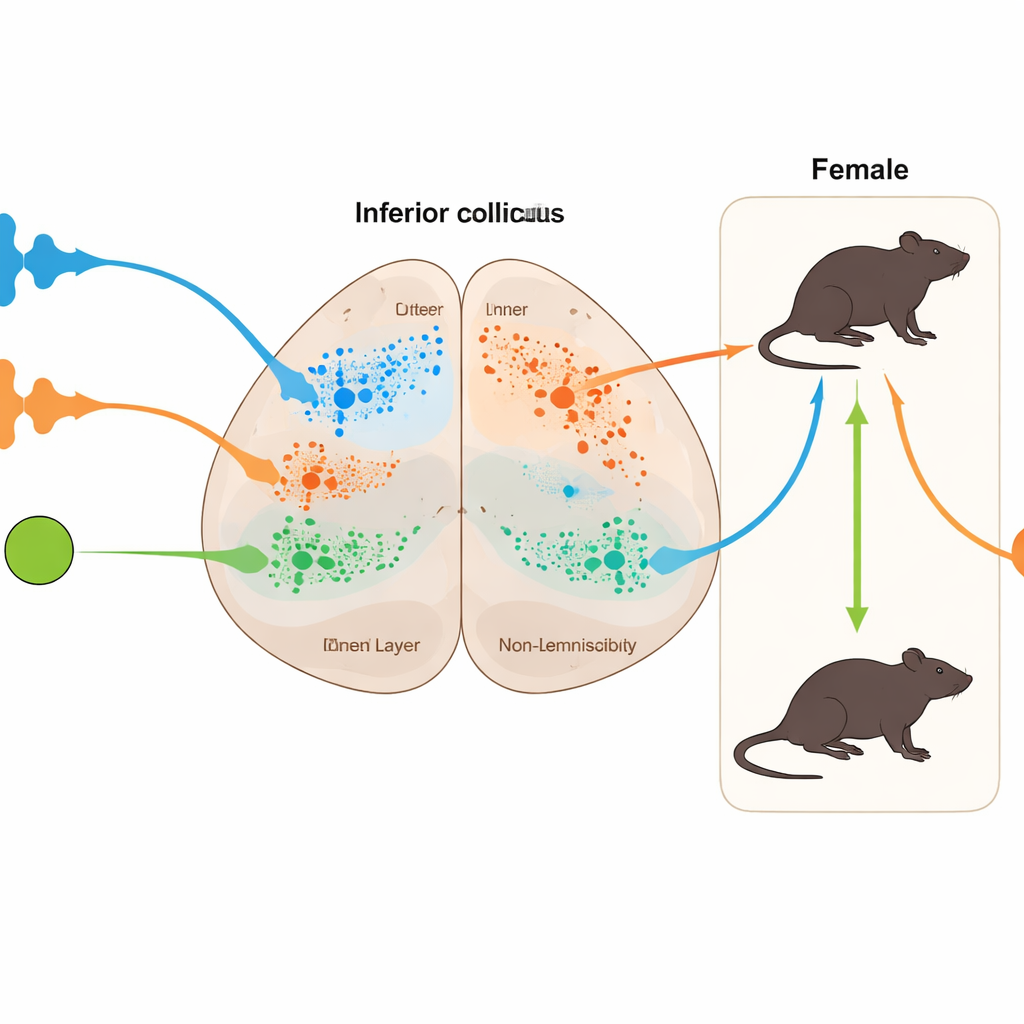
Was das für das Verständnis des autistischen Hörens bedeutet
Für Laien ist die Kernaussage, dass die frühe Klangverarbeitung im Gehirn nicht einheitlich ist: Männchen und Weibchen starten mit unterschiedlichen „Hörstilen“, und genetische versus umweltbedingte Risikofaktoren für Autismus lenken diese Stile in unterschiedliche Richtungen. Es geht nicht um eine einzige, einfache Veränderung in der Lautstärke der Gehirnantwort auf Geräusche, sondern autismusähnliche Zustände verändern das Gleichgewicht zwischen Gewöhnung an sich wiederholende Töne und Reaktion auf Unerwartetes, insbesondere in Schaltkreisen, die Kontext und emotionale Relevanz gewichten. Diese Arbeit an Ratten kann menschliche Hörerfahrungen nicht allein erklären, aber sie stützt die Vorstellung, dass Autismus mehrere biologische Subtypen umfasst – und dass Geschlecht und Ursache beide beeinflussen, wie das Gehirn die laute Welt vorhersagt und darauf reagiert.
Zitation: Cacciato-Salcedo, S., Lao-Rodríguez, A.B. & Malmierca, M.S. Sex- and etiology-specific effects on predictive processing in the inferior colliculus of two rat models of autism. Commun Biol 9, 356 (2026). https://doi.org/10.1038/s42003-026-09585-z
Schlüsselwörter: auditorische Verarbeitung, prädiktive Kodierung, Autismus-Modelle, Geschlechtsunterschiede, Colliculus inferior