Clear Sky Science · de
Strukturelle Einblicke in die WRN-Helikase zeigen Konformationszustände und Chancen für die Wirkstoffforschung bei MSI‑H-Krebs
Warum das für die Krebsbehandlung wichtig ist
Bestimmte Krebsarten haben eine eingebaute Schwäche: Sie können Fehler in ihrer DNA nur schlecht reparieren. Ein Protein namens WRN-Helikase wirkt wie ein molekulares Reparaturwerkzeug, das diese empfindlichen Tumoren am Leben erhält. Diese Studie zeigt in atomarer Detailtiefe, wie WRN sich entlang der DNA bewegt und wie experimentelle Wirkstoffe seine Bewegung blockieren können — und liefert damit eine Landkarte für neue Therapien, die diese verwundbaren Krebszellen selektiv abtöten, während gesundes Gewebe verschont bleibt.
Der DNA-Handwerker unter dem Mikroskop
Die WRN-Helikase ist Teil der zellulären Instandhaltungscrew und hilft, DNA zu entwinden, damit Schäden erkannt und repariert werden können. Menschen, die ohne funktionierendes WRN geboren werden, entwickeln das Werner-Syndrom, eine seltene Erkrankung mit vorzeitiger Alterung, was zeigt, wie wichtig dieses Protein für den Erhalt des Genoms ist. Tumoren mit „mikrosatelliteninstabilität‑hoch“ (MSI‑H) — ein häufiges Defizit bei Darmkrebs und einigen anderen Tumoren — sind besonders von WRN abhängig. Wird WRN in diesen Zellen ausgeschaltet, bricht die ohnehin fragile DNA rasch auseinander und die Krebszellen sterben. Das macht WRN zu einem attraktiven Arzneimittelziel, doch bislang fehlte ein klares Bild davon, wie das Protein seine Form verändert, während es DNA greift, chemische Energie verbraucht und sich entlang des Erbguts bewegt.
Beobachtung von WRN beim Flexen und Atmen
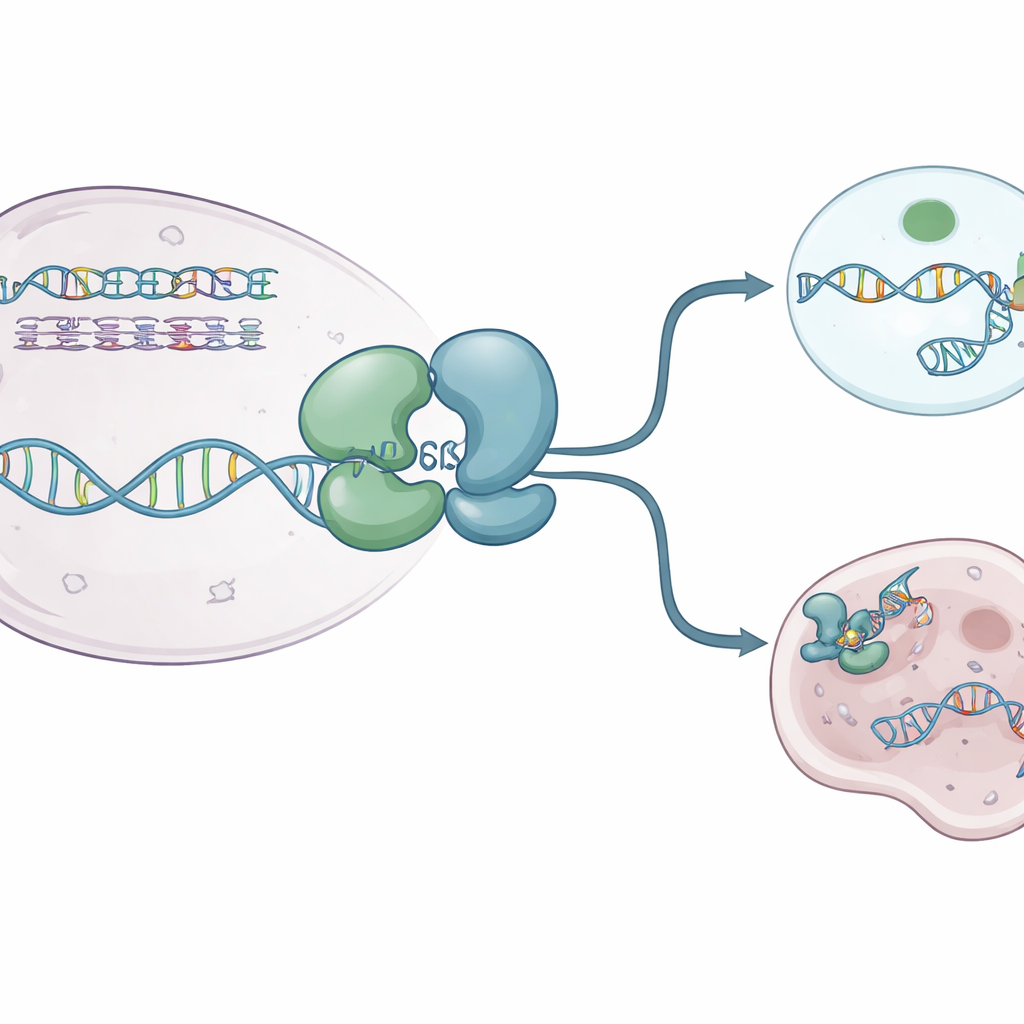
Die Autoren nutzten Röntgenkristallographie, um mehrere hochaufgelöste »Momentaufnahmen« des menschlichen WRN-Helikasekerns einzufangen. Sie lösten Strukturen von WRN allein sowie von WRN, gebunden an einzelsträngige DNA und an ein nicht spaltbares ATP‑ähnliches Brennstoffmolekül. Diese Ansichten zeigten, dass das Protein aus zwei Hauptlappen besteht, die über ein flexibles Scharnier verbunden sind und wie ein atmendes Gelenk funktionieren. Im ruhenden, kraftstofffreien Zustand nimmt WRN eine kompakte »geschlossene« Form an, in der die Lappen eng beieinanderliegen. Wenn ATP‑ähnlicher Brennstoff und DNA vorhanden sind, schwingen die Lappen auseinander in eine offenere Konfiguration, die die DNA in einer positiv geladenen Rinne aufnehmen kann. Eine kleine aromatische Schleife innerhalb von WRN formt sich zu einer kurzen Helix um und klemmt sich zwischen DNA-Basen — sie wirkt wie ein Ratschensystem, das dem Protein hilft, vorwärts zu treten, ohne zurückzurutschen.
Wie aktuelle Wirkstoffe WRN abschalten
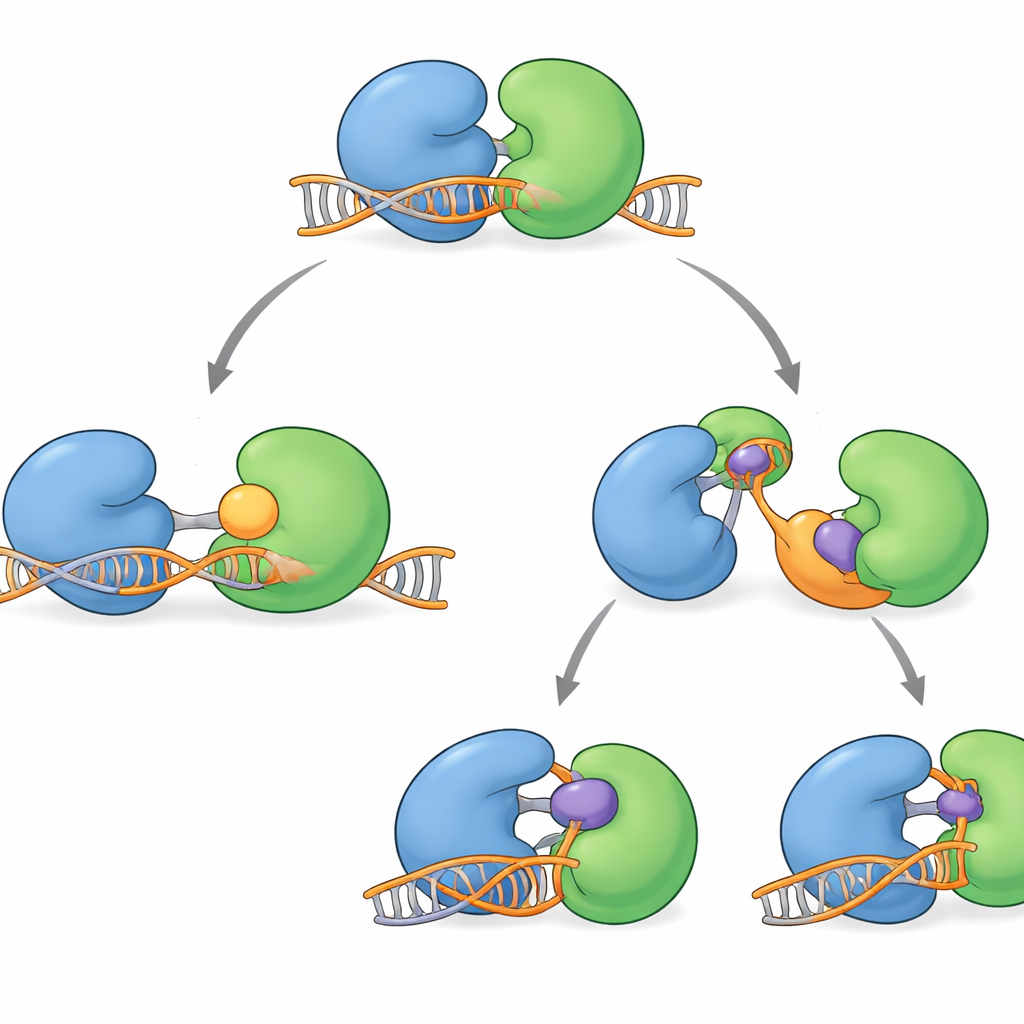
Mehrere WRN-blockierende Verbindungen sind kürzlich in klinische Prüfungen gegangen. Sie verstopfen die aktive Rinne des Proteins nicht direkt. Stattdessen wirken sie aus der Distanz, indem sie den Scharnierbereich umgreifen und WRN in Formen verriegeln, die die DNA nicht richtig erfassen können. Einige Moleküle, wie HRO761 und ein verwandter klinischer Kandidat von GSK, drehen einen Lappen um etwa 180 Grad relativ zum anderen und erzeugen eine dramatische »verdrehte« Form, die neben der DNA sitzt. Andere, darunter VVD‑133214 und eine hier untersuchte eng verwandte Verbindung, fixieren WRN in einer fest »geschlossenen« Anordnung, die wichtige DNA-fassende Oberflächen nicht freilegt. Biophysikalische Experimente bestätigten, dass WRN, wenn diese Wirkstoffe gebunden sind, keinen stabilen Komplex mehr mit einzelsträngiger DNA bilden kann und damit die Verbindung zwischen ATP-Verbrauch und DNA-Entwindung effektiv unterbricht.
Wie Krebszellen lernen, zu entkommen
Um zu sehen, wie Tumoren diesen Wirkstoffen entgehen könnten, kultivierte das Team MSI‑H-Darmkrebszellen über Wochen bis Monate hinweg in Gegenwart von WRN-Inhibitoren. Resistente Populationen traten schnell auf. Genetische Analysen zeigten, dass die Zellen jeweils eine einzelne, präzise Veränderung im WRN-Gen in der Nähe der Wirkstoffbindungsstelle am Scharnier erworben hatten. Eine Mutation schwächte die Wirkung des »verdrehten Zustands«-Inhibitors HRO761 ab, während eine andere Mutation die Empfindlichkeit gegenüber VVD‑133214 verringerte, das den geschlossenen Zustand bevorzugt. Außerdem steigerten viele resistente Zellen die WRN-Produktion, wodurch sie sich mehr Kopien des Ziels verschafften und die Wirkung des Wirkstoffs teilweise verdünnten. Diese Befunde spiegeln Resistenzmuster wider, die auch bei anderen zielgerichteten Krebsmedikamenten beobachtet werden, wo kleine strukturelle Veränderungen im Zielprotein oder Überexpression die Behandlung abschwächen können.
Blick nach vorn: klügere WRN-Blocker
Insgesamt kartieren die neuen Strukturen einen vollständigen Arbeitszyklus von WRN, wie es die DNA ergreift, sich entlangbewegt und sich dann zurücksetzt. Sie zeigen auch, dass die derzeitigen klinischen Verbindungen hauptsächlich »off‑DNA«-Formen des Proteins stabilisieren. Für eine allgemeine Leserschaft ist der Kernpunkt, dass wir nun verstehen, wo WRN verwundbar ist und wie Tumoren sich anpassen können. Das legt eine nächste Welle von Inhibitoren nahe, die WRN binden, wenn es an die DNA gebunden ist, und es möglicherweise in einem toxischen Zustand festhalten — ähnlich erfolgreichen Wirkstoffen, die andere DNA-Reparaturenzyme einklemmen. Solche »on‑DNA«-WRN-Blocker könnten allein oder in Kombination mit bestehenden Mitteln haltbarere Wege bieten, die verborgene Schwäche von MSI‑H-Tumoren auszunutzen.
Zitation: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Schlüsselwörter: WRN-Helikase, mikrosatelliteninstabilität, DNA-Reparatur, allosterische Inhibitoren, Arzneimittelresistenz