Clear Sky Science · de
PiR48444 hemmt die osteogene Differenzierung von MSCs und die Knochenregeneration durch Zielrichtung auf METTL7A/eIF4E-vermittelte BMP2 m6A-Methylierung
Warum winzige Moleküle für gebrochene Knochen wichtig sind
Gebrochene Knochen und altersbedingter Knochenverlust sind weit verbreitete Probleme, und Ärztinnen und Ärzte möchten Stammzellen nutzen, um dem Körper beim Wiederaufbau des beschädigten Skeletts zu helfen. Diese Stammzellen bilden jedoch nicht immer so effizient neuen Knochen, wie man es sich wünscht, insbesondere bei älteren Menschen oder in entzündetem Gewebe. Diese Studie entdeckt ein kleines RNA-Molekül, genannt piR48444, das wie eine molekulare Bremse auf knochenbildenden Stammzellen wirkt. Indem man diese Bremse löst, zeigen die Forschenden, dass es möglich sein könnte, die Knochenreparatur zu verbessern und Knochenverlust vorzubeugen.
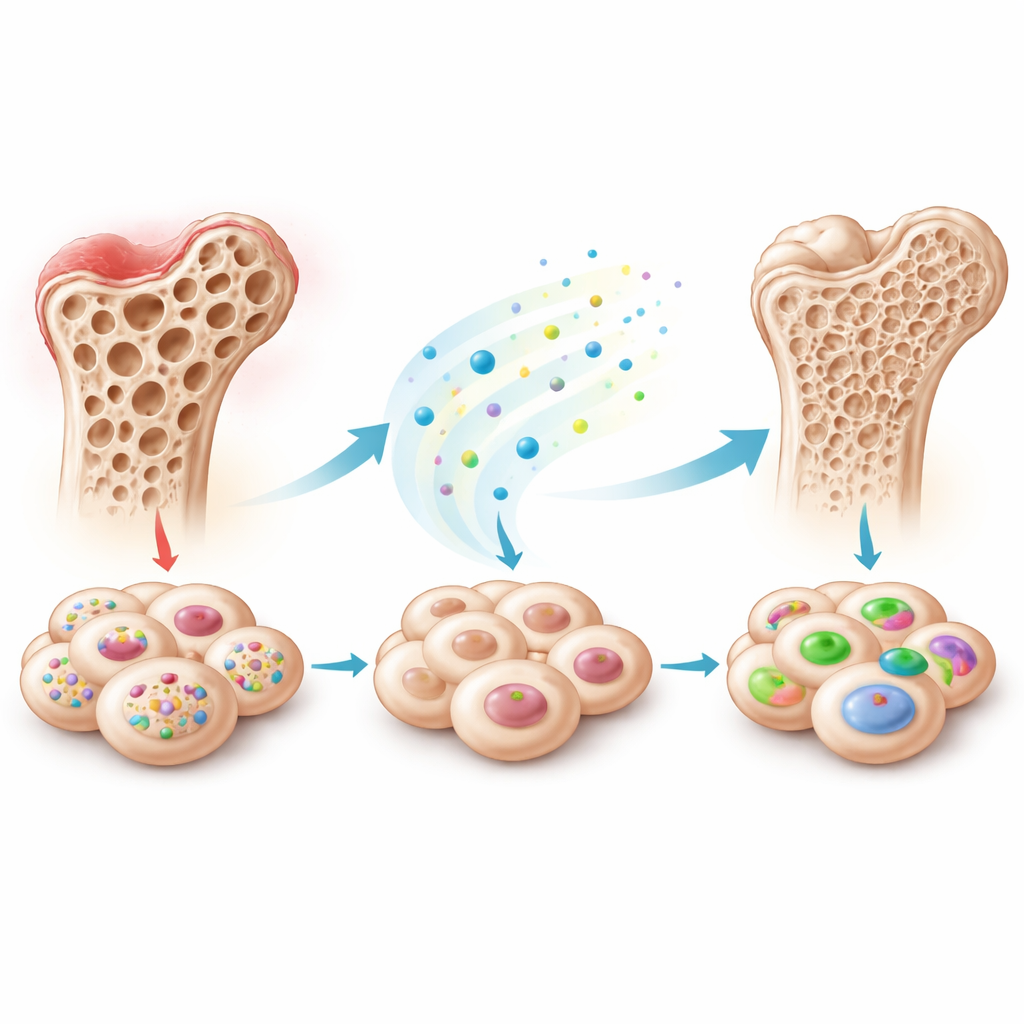
Eine verborgene Bremse in vielen Stammzelltypen
Das Team konzentrierte sich auf mesenchymale Stammzellen, vielseitige Zellen, die zu Knochen, Knorpel, Fett und mehr werden können und die aus vielen Geweben wie Knochenmark, Milchzähnen und Fett isoliert werden. Wenn diese Zellen im Labor zur Knochenbildung angeregt werden, ändern Tausende von Genen und kleinen RNAs ihre Aktivität. Durch Sequenzierung dieser Moleküle in Stammzellen aus exfoliierten Milchzähnen fanden die Forschenden, dass eine bestimmte kleine RNA, piR48444, kontinuierlich abnahm, als sich die Zellen in Richtung Knochen entwickelten. Sie überprüften anschließend andere Stammzelltypen und sahen dasselbe Muster: Zellen, die mehr Knochen bildeten, hatten weniger piR48444, was darauf hindeutet, dass dieses Molekül ihre knochenbildende Fähigkeit normalerweise bremst.
Von der Laborplatte zu lebenden Knochen
Um diese Idee zu testen, veränderten die Wissenschaftler die piR48444-Spiegel in mehreren Stammzelltypen. Als sie piR48444 reduzierten, depositierten die Zellen mehr Calcium, schalteten Gene an, die mit Knochenbildung verbunden sind, und sahen unter dem Mikroskop mehr wie unreifes Knochengewebe aus. Als sie die Zellen zwangen, zusätzliches piR48444 zu produzieren, geschah das Gegenteil: knochenbezogene Aktivität nahm ab. Das Team ging dann zu Tiermodellen über. Stammzellen mit ausgeschaltetem piR48444 wurden verwendet, um kleine Schädeldefekte bei Mäusen zu füllen. Diese modifizierten Zellen erzeugten deutlich mehr neuen Knochen als Kontrollzellen, wie 3D-Röntgenscans und Gewebefärbungen zeigten, was darauf hindeutet, dass das Blockieren von piR48444 die Knochenreparatur in lebenden Organismen wesentlich verbessern kann.
Schutz fragiler Knochen bei Krankheit und Alter
Knochenverlust wird nicht nur durch Verletzungen verursacht, sondern auch durch Entzündung und Alterung. In Knochenmarkstammzellen, die bakteriellen Toxinen ausgesetzt waren, und in Stammzellen aus älteren Tieren waren die piR48444-Spiegel ungewöhnlich hoch, während knochenaufbauende Marker niedrig waren. Die Forschenden entwickelten ein „Antagomir“ – ein kurzes Molekül, das dazu bestimmt ist, piR48444 im Blutkreislauf zu neutralisieren – und injizierten es in Mäuse mit entzündungsbedingtem Knochenverlust sowie in natürlich gealterte Mäuse. In beiden Modellen behielten die behandelten Tiere deutlich mehr ihres schwammigen Innenknochens, mit dichteren und zahlreicheren feinen Knochenbälkchen, während die harte Außenschale des Knochens unverändert blieb. Dies deutet darauf hin, dass das Blockieren von piR48444 selektiv den fragilen, stoffwechselaktiven Teil des Skeletts schützt, der beim Altern und bei chronischen Entzündungen am stärksten gefährdet ist.
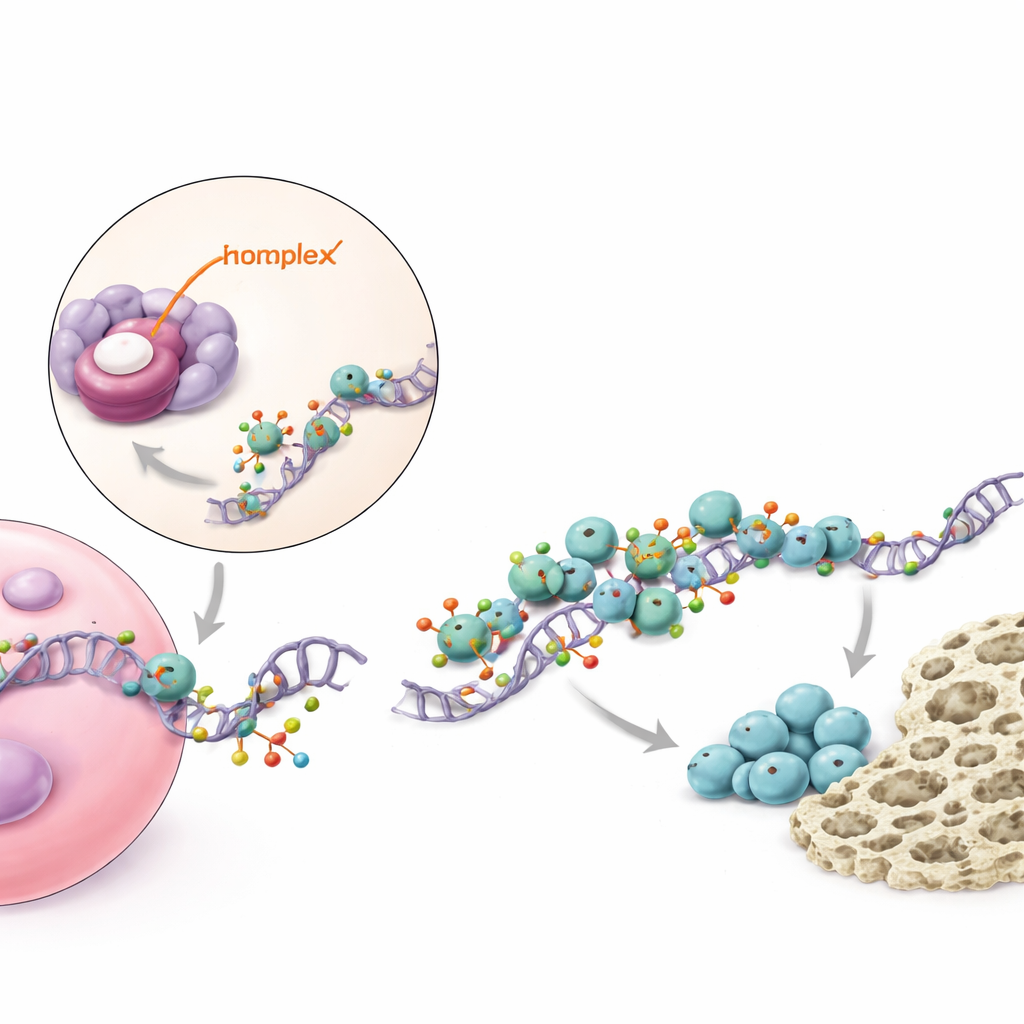
Eine molekulare Staffel, die ein wichtiges Knochensignal verstärkt
Bei tieferer Analyse kartierte die Studie, wie piR48444 seine Effekte innerhalb der Zellen ausübt. Die kleine RNA bindet an und unterdrückt ein Protein namens METTL7A, das als Enzym wirkt und Botenmoleküle modifiziert, die den Bauplan für BMP2 tragen, einen bekannten Wachstumsfaktor, der die Knochenbildung stark fördert. METTL7A fügt den BMP2-Botschaften kleine chemische Markierungen hinzu, die sie stabiler machen und es dem zellulären Proteinsyntheseapparat erleichtern, sie abzulesen. METTL7A arbeitet außerdem mit einem anderen Protein, eIF4E, zusammen, das die Initiation der Proteinfertigung unterstützt. Wenn piR48444 reichlich vorhanden ist, wird METTL7A unterdrückt, weniger BMP2-Nachrichten werden markiert und übersetzt, und es wird weniger BMP2-Protein produziert, sodass Stammzellen weniger wahrscheinlich Knochen bilden. Wenn piR48444 blockiert wird, steigen METTL7A und BMP2 an und treiben die Zellen in Richtung Knochenbildung.
Was das für die zukünftige Knochenreparatur bedeutet
Kurz gesagt zeigen die Autorinnen und Autoren eine Kontrollkette, in der eine winzige RNA (piR48444) ein Helferenzym (METTL7A) dämpft, das seinerseits ein starkes knochenbildendes Signal (BMP2) begrenzt. Indem man diese Kette auf der Ebene von piR48444 unterbricht, können verschiedene Stammzellen besser Knochen bilden und der Knochenverlust bei Mäusen verringert werden. Während Sicherheit, Off-Target-Effekte und Langzeitergebnisse noch sorgfältig geprüft werden müssen, weist die Arbeit auf piR48444 sowohl als potenziellen Blutmarker für das Osteoporoserisiko als auch als vielversprechendes Ziel für Medikamente hin, die die stammzellbasierte Knochenregeneration in der Klinik verbessern sollen.
Zitation: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Schlüsselwörter: Knochenregeneration, mesenchymale Stammzellen, Osteoporose, nicht-kodierende RNA, BMP2-Signalgebung