Clear Sky Science · de
Qualitätsbewertung von RNA-3D-Strukturmodellen mittels Deep Learning und Zwischen-2D-Karten
Warum die Beurteilung von RNA-Formen wichtig ist
In jeder Zelle falten und verdrehen sich RNA-Moleküle zu komplexen dreidimensionalen Formen, die dabei helfen, welche Gene aktiviert werden, chemische Reaktionen steuern und sogar Viren abwehren. Heutige leistungsfähige Computerprogramme können viele dieser Formen vorhersagen, doch Wissenschaftler stehen weiterhin vor einem grundlegenden Problem: Wenn der Computer Dutzende oder Hunderte Kandidatenformen für dieselbe RNA liefert, welche davon entspricht der Realität? Dieses Papier stellt RNArank vor, ein KI-Werkzeug, das genau diese Frage angeht, indem es RNA-3D-Modelle bewertet — ähnlich einem strukturellen Qualitätsprüfer — sodass Forscher sich auf die vertrauenswürdigsten Vorhersagen konzentrieren können.
Ein neuer Prüfer für RNA-Modelle
RNArank ist darauf ausgelegt, die Qualität einer vorgeschlagenen RNA-Form zu beurteilen, ohne zu wissen, wie diese Form erzeugt wurde. Ob das Modell aus einem Deep-Learning-System, einer physikbasierten Simulation oder von einem menschlichen Experten stammt — RNArank betrachtet nur die finalen 3D-Koordinaten. Es fragt im Grunde: „Sieht diese Struktur wie eine realistische RNA aus?“ Solch eine unabhängige Qualitätsbewertung ist wichtig, denn anders als in der Proteinwelt, wo Werkzeuge wie AlphaFold oft von vornherein sehr verlässliche Ergebnisse liefern, profitieren RNA-Vorhersagen weiterhin von der Kombination mehrerer Methoden und menschlicher Expertise — und von einer intelligenten Methode zur Rangordnung der resultierenden Modelle.
Der KI beibringen, wie gute RNA aussieht
Zum Trainieren von RNArank stellten die Autoren rund 200.000 RNA-Strukturen zusammen, die ein breites Spektrum von eindeutig fehlerhaften bis hin zu nahezu perfekten Modellen abdecken. Diese wurden aus bekannten experimentellen Strukturen unter Verwendung verschiedenster Ansätze erzeugt, darunter moderne Deep-Learning-Prädiktoren, Molekulardynamik-Simulationen, die atomare Bewegungen nachahmen, und gezielte Verzerrungen korrekter Strukturen zur Erzeugung von „Decoys“. Für jedes Modell berechnete das Team, wie eng es der tatsächlich experimentell bestimmten RNA entsprach, mithilfe einer verfeinerten Genauigkeitsmetrik, die auf RNA zugeschnitten ist und lDDT_RNA genannt wird. Diese Metrik konzentriert sich darauf, wie gut die Abstände zwischen Nukleotidpaaren reproduziert werden, und erfasst sowohl die Gesamtfaltung als auch lokale Details, ohne übermäßig empfindlich gegenüber der Molekülgröße zu sein.
Wie RNArank eine RNA liest und bewertet
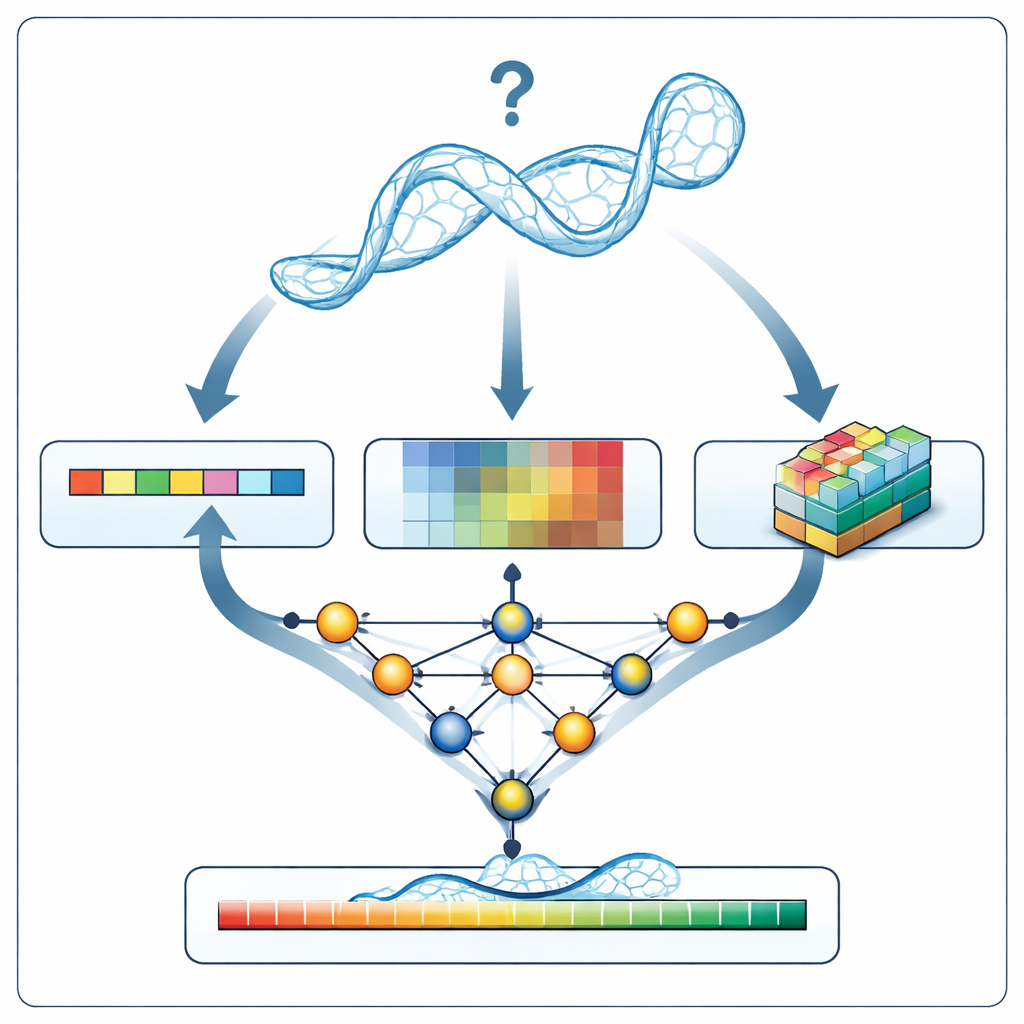
Wenn RNArank ein neues RNA-Modell untersucht, übersetzt es die Struktur zunächst in drei Arten von Informationen: eine 1D-Beschreibung der Sequenz und der Rückgratgeometrie entlang der Kette, 2D-Beschreibungen dazu, wie jedes Nukleotidpaar zueinander steht (deren Abstände, geschätzte Wechselwirkungsenergien und mögliche atomare Kollisionen), sowie 3D-„Voxel“-Schnappschüsse, kleine Gitter, die die lokale Atomwolke um jedes Nukleotid erfassen. Ein mehrteiliges neuronales Netzwerk verknüpft diese Hinweise zu einem einheitlichen Bild und sagt dann zwei Zwischen-2D-Karten voraus: welche Nukleotide wahrscheinlich in Kontakt stehen und um wieviel sich jede modellierte Distanz wahrscheinlich von der unbekannten wahren Struktur abweicht. Aus diesen Karten rekonstruiert RNArank sowohl einen pro-Nukleotid-Vertrauenswert als auch einen Gesamtscore für das gesamte RNA-Modell.
Das Verfahren auf die Probe gestellt
Das Team testete RNArank an drei anspruchsvollen Datensätzen: einer Gruppe von 24 neu aufgeklärten RNAs aus der Protein Data Bank sowie an den RNA-Zielen zweier internationaler Blindvorhersage-Wettbewerbe, CASP15 und CASP16, bei denen viele Gruppen Modelle einreichen, ohne die Lösungen zu kennen. Über Tausende von Kandidatenstrukturen hinweg korrelierten die RNArank-Werte näher mit der tatsächlichen Modellqualität als mehrere etablierte energiesbasierte Bewertungsmethoden und andere Deep-Learning-Ansätze. RNArank war besonders gut darin, das beste oder nahe am besten liegende Modell aus einer großen Menge auszuwählen und zu erkennen, welche Teile einer Struktur wahrscheinlich unzuverlässig sind. Die Autoren zeigten außerdem, dass RNArank seine Leistung selbst bei RNAs beibehielt, die sich sequenzseitig deutlich von den während des Trainings gesehenen unterschieden — ein Hinweis auf echte Generalisierung statt bloßem Auswendiglernen.
Heutige Grenzen und Aussichten
RNArank ist nicht perfekt: Es hat weiterhin Schwierigkeiten mit besonders flexiblen RNAs, die viele Konformationen einnehmen, und mit RNAs, die ihre Form ändern, wenn sie von Proteinen in große molekulare Maschinen eingespannt werden. Dennoch ist es schnell genug, um viele Modelle für RNAs mit einigen hundert Nukleotiden in nur Sekunden zu bearbeiten, und es hilft bereits automatisierten Servern, in gemeinschaftlichen Tests qualitativ hochwertigere Vorhersagen auszuwählen. Indem es eine methodenunabhängige, rein strukturbasierte Bewertungsinstanz für RNA-Modelle bereitstellt, liefert RNArank Biologen einen schärferen Filter, um rohe Computerergebnisse in verlässliche strukturelle Hypothesen zu verwandeln — ein Schritt näher an routinemäßig vertrauenswürdigen Vorhersagen von RNA-Formen und damit an tieferen Einsichten in die Funktionsweisen dieser vielseitigen Moleküle.
Zitation: Liu, X., Wang, W., Du, Z. et al. Quality assessment of RNA 3D structure models using deep learning and intermediate 2D maps. Commun Biol 9, 293 (2026). https://doi.org/10.1038/s42003-026-09582-2
Schlüsselwörter: RNA-3D-Struktur, Deep Learning, Modellqualitätsbewertung, strukturelle Bioinformatik, RNArank