Clear Sky Science · de
Ein Einzelzell-Atlas enthüllt zelluläre Heterogenität und BMP5-vermittelte Regulierung der adipogenen Differenzierung im Schaffettgewebe
Warum Schaffett uns etwas über Gesundheit lehren kann
Fett ist mehr als Polster; es ist ein aktives Organ, das Tieren hilft, Kälte, Hunger und Krankheit zu überstehen. Schafe sind besonders interessant, weil einige Rassen enorme Fettreserven im Schwanz anlegen – ein natürliches „Energie-Rucksack“ für schlechte Zeiten. Diese Studie nutzte moderne Einzelzell-Genetik, um die verschiedenen Zelltypen, aus denen Schaffett besteht, fein aufzulösen und herauszufinden, wie ein zentrales Signal, ein Molekül namens BMP5, mitbestimmt, ob Schwanzfettzellen wachsen und Energie speichern. Das Verständnis dieser Prozesse könnte zu schlankeren Nutztierrassen führen und Aufschluss über menschliche Adipositas und Stoffwechselkrankheiten geben.
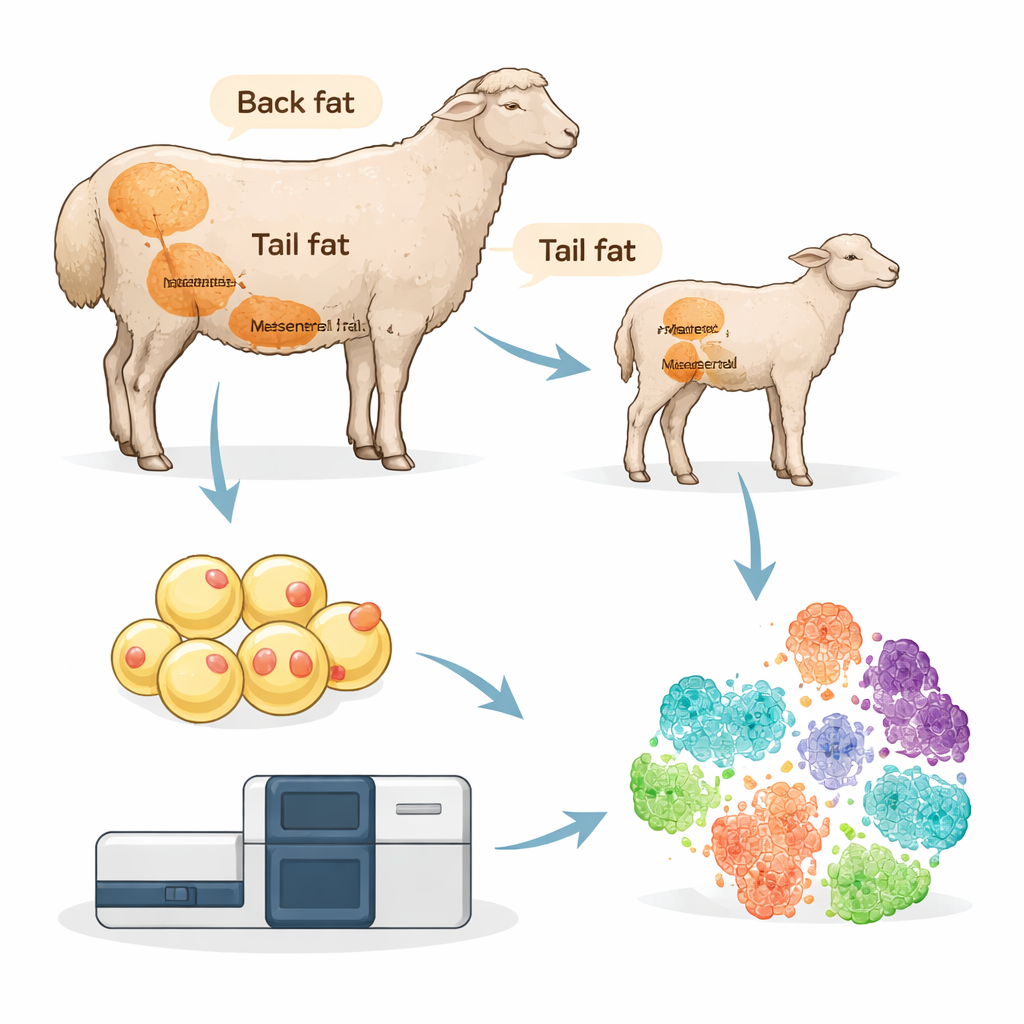
Verschiedene Fettarten, verschiedene Aufgaben
Fett im Körper ist nicht einheitlich. Die Forscher konzentrierten sich auf vier wichtige Fettdepots beim Hu-Schaf: subkutanes Fett am Rücken, Schwanzfett und zwei Arten von tief liegendem Viszeralfett um innere Organe. Durch die Analyse von mehr als 64.000 einzelnen Zellkernen erstellten sie einen zellulären Atlas dieser Depots. Sie identifizierten neun Hauptzellfamilien, darunter ausgereifte Fettzellen, Stamm- und Vorläuferzellen, die zu Fett werden können, Immunzellen und Zellen, die Blutgefäße auskleiden. Jedes Depot hatte eine eigene Zusammensetzung. Rücken- und Schwanzfett waren besonders reich an ausgereiften Fettzellen, die auf Energiespeicherung ausgerichtet sind, während Viszeralfett mehr Immunzellen enthielt, die wahrscheinlich Entzündungen und den gesamten Stoffwechsel mitsteuern.
Die besondere Reserve flexibler Zellen im Schwanzfett
Das Team schaute dann genauer auf das fettreiche Schwanzdepot und entnahm Proben bei der Geburt sowie im Alter von 2, 4 und 6 Monaten. Sie entdeckten, dass Schwanzfett einen hohen Anteil einer speziellen Stammzell-ähnlichen Population, der fibroadipogenen Vorläuferzellen, enthält. Diese Zellen können entweder zu energie-speichernden Fettzellen oder zu fibrösen Stütz-Zellen differenzieren, wodurch das Schwanzdepot sowohl strukturelle Festigkeit als auch die Fähigkeit zur Expansion der Energiereserven erhält. Eine Untergruppe dieser Vorläufer, die kurz nach der Geburt reichlich vorhanden war, zeigte starke Aktivität in Genen, die Zellteilung und frühe Entwicklung steuern, was nahelegt, dass die ersten Lebenswochen ein kritisches Zeitfenster sind, in dem die zukünftige Fettkapazität des Schwanzes festgelegt wird.
Wie ein einzelnes Signal die Fettbildung lenkt
Mithilfe computergestützter Werkzeuge untersuchten die Forscher, wie Zelltypen im Schwanzfett über chemische Signale miteinander „kommunizieren“. Unter Dutzenden Signalwegen stach in Neugeborenen der BMP-Weg hervor. In diesem System sezernierten Stamm- und frühe Fettzellen ein Protein namens BMP5, das an Rezeptoren benachbarter Vor-Fettzellen bindet und offenbar deren Differenzierung zu voll ausgebildeten Fettzellen fördert. Mit dem Älterwerden der Tiere nahm die Stärke dieses BMP5-Signals ab, was mit einer allgemeinen Verlangsamung der Neubildung von Fettzellen übereinstimmte. Im Vergleich der Genaktivität zwischen neugeborenem Schwanzfett und einem Viszeralfettdepot waren BMP5 und verwandte Gene im Schwanz deutlich aktiver, was seine Rolle als Treiber der schwanzspezifischen Fettansammlung unterstreicht.
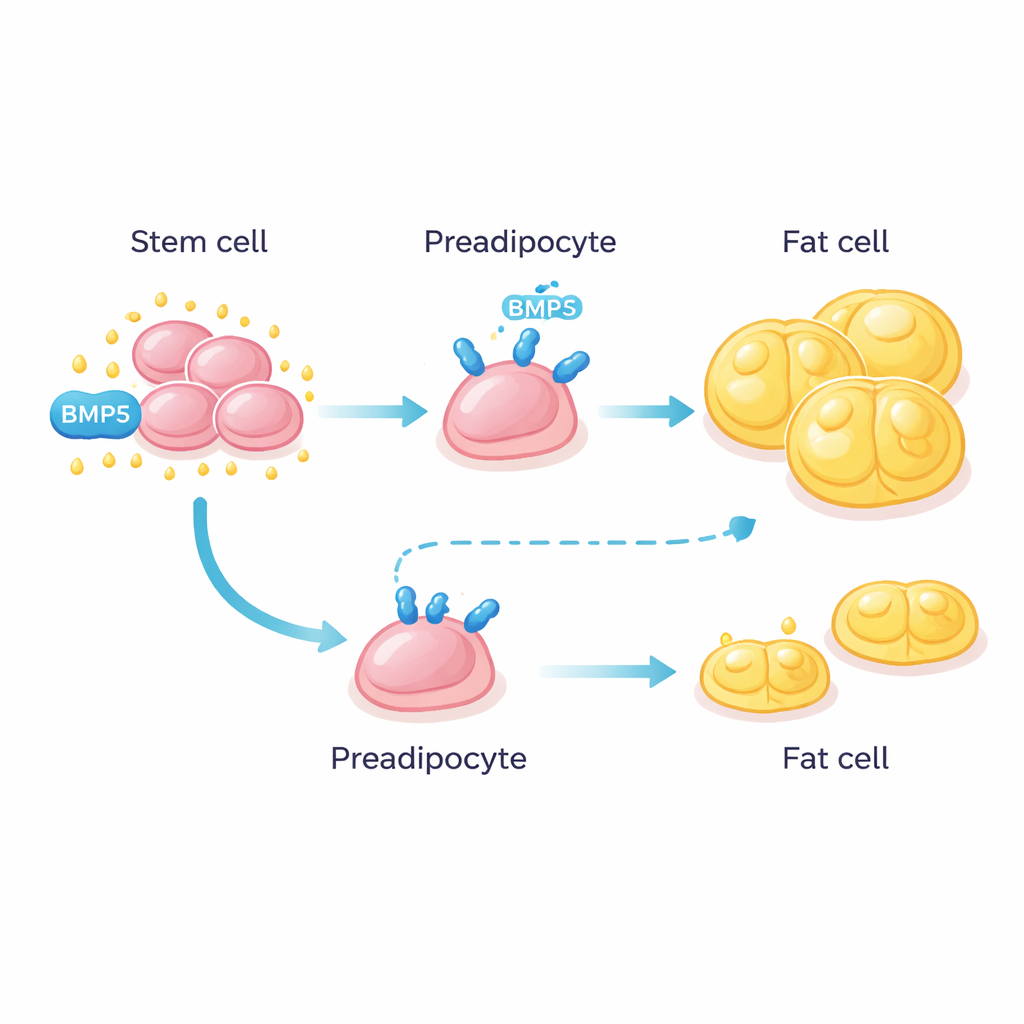
BMP5 ausschalten reduziert Fettspeicherung
Um zu prüfen, ob BMP5 tatsächlich die Fettbildung steuert, züchteten die Wissenschaftler Schwanzfettzellen im Labor und schalteten das BMP5-Gen mithilfe kleiner RNA-Moleküle ab. Das Ergebnis war eindrücklich: Zellen mit reduziertem BMP5 speicherten weniger Triglyzeride, die Hauptform von Fett, und wichtige fettbezogene Gene waren herunterreguliert. Dieses Experiment deutet darauf hin, dass BMP5 wie ein Lautstärkeregler für die Entwicklung von Schwanzfett wirkt. Wird es hochgeregelt, baut der Schwanz große, energiereiche Reserven auf; wird es heruntergeregelt, entsteht schlankeres Gewebe. Da die BMP5-Aktivität offenbar in Schwanz- und anderem subkutanen Fett konzentriert ist, schlagen die Autoren vor, dass es künftig möglich sein könnte, unerwünschtes externes Fett bei Nutztieren zu verringern, ohne das erwünschte intramuskuläre Fett zu schädigen.
Was das für Tiere und Menschen bedeutet
Einfach gesagt zeigt diese Arbeit, dass verschiedene Fettdepots bei Schafen aus unterschiedlichen Zellgemeinschaften bestehen und nach eigenen Wachstumsregeln operieren. Schwanzfett verfügt über flexible, stammzellähnliche Zellen und ein starkes BMP5-Signal, die zusammen eine robuste Energiespeicherung aufbauen. Indem die Studie Zellen einzeln kartiert, identifiziert sie BMP5 als Schlüsselregulator dafür, wann und wo neue Fettzellen entstehen. Für Landwirte könnten solche Erkenntnisse Zucht- oder Geneditierungsstrategien informieren, um schlankere Tiere mit effizienterer Futterverwertung zu erzeugen. Für die menschliche Gesundheit bietet der Schaf-Atlas ein Modell großer Säugetiere, um zu untersuchen, warum manche Fettdepots schädlicher sind als andere und wie Signale in der frühen Lebensphase lebenslange Risiken für Adipositas und Stoffwechselerkrankungen prägen können.
Zitation: Cheng, J., Han, K., Xu, D. et al. Single-cell atlas reveals cellular heterogeneity and BMP5-mediated regulation of adipogenic differentiation in sheep adipose tissue. Commun Biol 9, 292 (2026). https://doi.org/10.1038/s42003-026-09581-3
Schlüsselwörter: Fettgewebe, Einzelzell-Atlas, Schwanzfett von Schafen, BMP5-Signalgebung, Fettstoffwechsel