Clear Sky Science · de
Lokales Kationen-Klemmen verzerrt und erweicht RNA-Duplex
Warum diese winzige Drehung in RNA wichtig ist
Innerhalb jeder Zelle werden DNA und RNA ständig gebogen, gestreckt und verdreht, während sie genetische Informationen speichern und nutzen. Diese Bewegungen sind nicht nur mechanische Details — sie steuern, wie Gene abgelesen werden, wie sich Viren kopieren und wie neue RNA-basierte Medikamente und Nanogeräte funktionieren. Die vorliegende Studie zeigt, dass einfache Salze aus positiv und negativ geladenen Ionen die Steifigkeit oder Flexibilität von RNA drastisch verändern können und dass RNA ganz anders reagiert als DNA. Das Verständnis dieses feinen „Erweichens und Versteifens“ könnte Forschern helfen, RNA-Medikamente, Impfstoffe und molekulare Werkzeuge besser zu entwickeln.
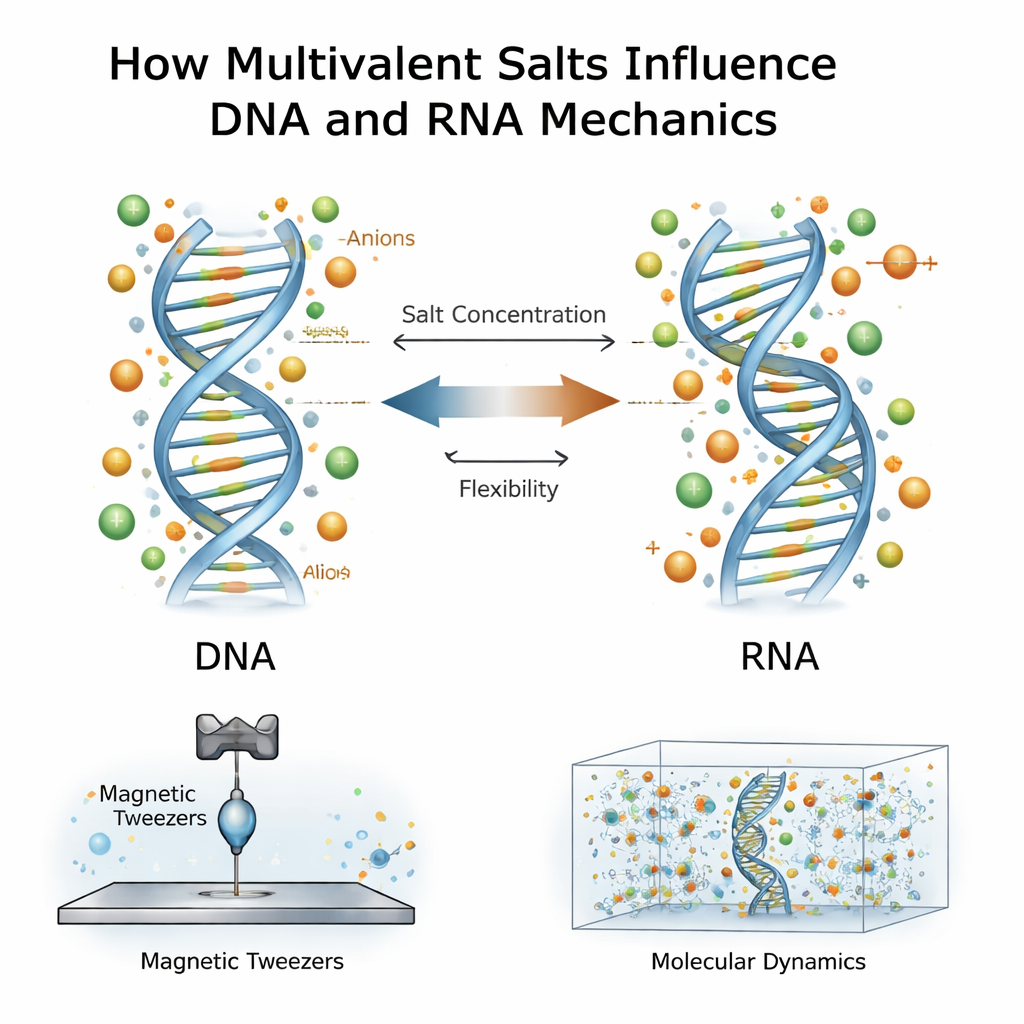
Salzige Umgebung und genetische Moleküle
DNA und RNA tragen eine starke negative elektrische Ladung und sind daher in Wasser von Wolken entgegengesetzt geladener Ionen umgeben. Die meisten früheren Arbeiten konzentrierten sich auf positiv geladene Ionen, insbesondere multivalenten Ionen mit zwei oder drei positiven Ladungen, wie Magnesium oder Spermidin. Diese Ionen sind dafür bekannt, DNA-Stränge zusammenzuhalten, zu kondensieren oder ihre Biegeleichtheit zu verändern. RNA, obwohl chemisch ähnlich wie DNA, verhält sich anders: Sie ist meist schwerer zu biegen, aber leichter zu dehnen. Die neue Arbeit stellt eine tiefere Frage: Was passiert, wenn sowohl die positiven Ionen als auch ihre begleitenden negativen Partner — Anionen — bei sehr hohen Salzkonzentrationen, deutlich höher als in typischen Zellen, mit DNA und RNA wechselwirken?
Einzelmoleküle ziehen, um Steifigkeit zu messen
Die Forschenden verwendeten eine Technik namens magnetische Pinzetten, um einzelne DNA- oder RNA-Doppelhelixe nacheinander zu dehnen. Jedes Molekül war an einem Ende an einer Glasoberfläche und am anderen an einer winzigen magnetischen Kugel verankert. Durch das Bewegen von Magneten über der Probe konnten sie mit kontrollierten Kräften ziehen und aufzeichnen, wie weit sich jedes Molekül ausdehnte und wie es sich unter Spannung verdrehte. Aus diesen Kraft–Dehnungs-Kurven extrahierten sie vier zentrale mechanische Eigenschaften: wie schwer das Molekül zu biegen ist, wie schwer es zu dehnen ist, seine effektive Länge pro Basenpaar und wie Verdrillung seine Länge verändert. Diese Messungen wiederholten sie über einen weiten Bereich multivalenter Salzkonzentrationen für mehrere verschiedene Salze, darunter Spermidin und Calciumchlorid.
DNA wird wieder steifer, aber RNA weicht plötzlich auf
Bei DNA entsprach das Verhalten größtenteils den Erwartungen. Mit zunehmender Konzentration multivalenter positiver Ionen wurde DNA zunächst leichter zu biegen — ihre Steifigkeit nahm ab — weil die Ionen ihre negative Ladung neutralisierten. Bei noch höheren Werten überkompensierten die überschüssigen positiven Ionen effektiv und kehrten die Nettoladung der DNA um. Diese „Ladungsinversion“ machte die DNA wieder schwerer zu biegen, sodass ihre Steifigkeit anstieg. Überraschenderweise zeigte RNA das entgegengesetzte und deutlichere Muster. Bei niedrigen bis moderaten Salzkonzentrationen nahm ihre Biegesteifigkeit zu: der RNA-Duplex wurde geradliniger und steifer. Bei sehr hohen Konzentrationen jedoch fiel die Biegesteifigkeit der RNA um mehr als die Hälfte, und andere Eigenschaften wie ihre Dehnbarkeit und das Wechselspiel von Verdrillung und Dehnung kehrten sich auf unerwartete Weise um.
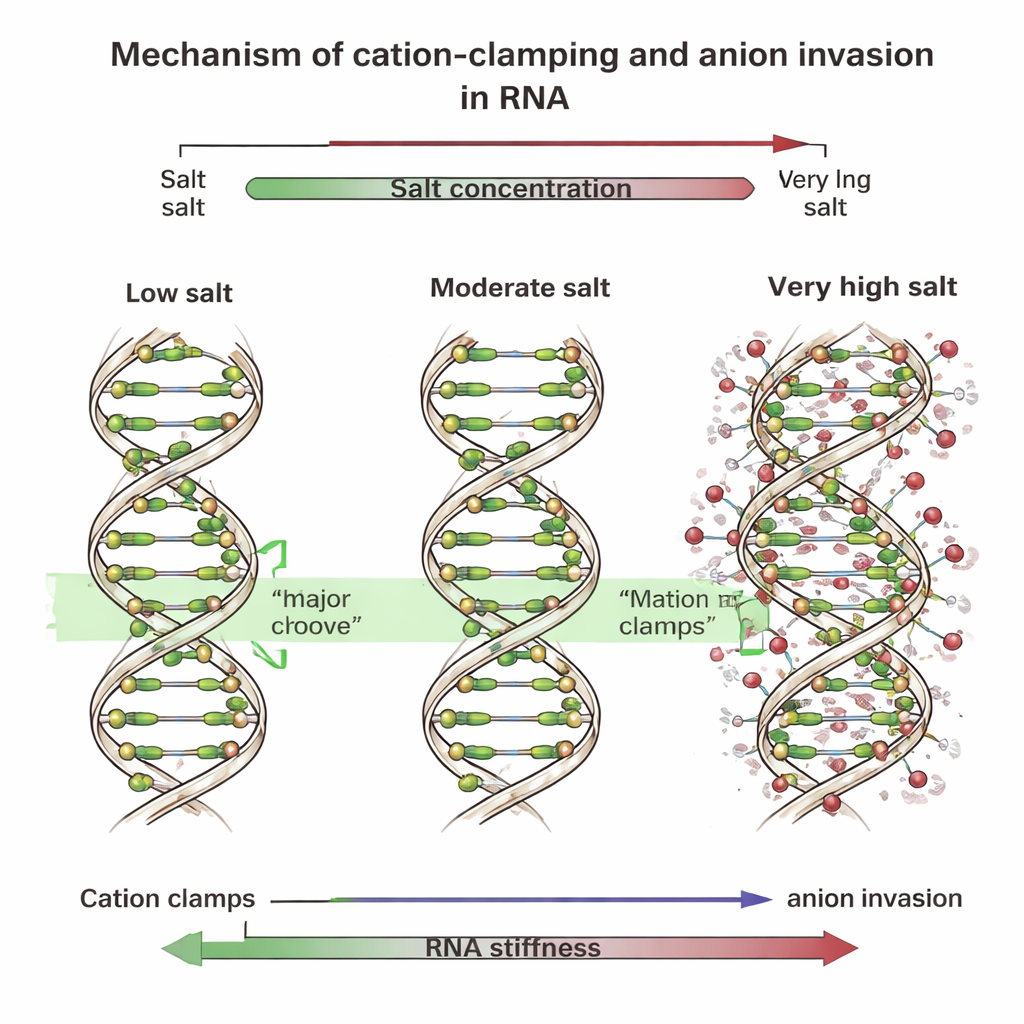
Klemmen, Rillen und eindringende Ionen
Um die Ursache aufzudecken, führten die Forschenden detaillierte Computersimulationen durch, die jedes Atom kurzer DNA- und RNA-Fragmente in salzhaltigem Wasser verfolgten. Diese Simulationen zeigten, dass sich bei niedrigen und moderaten Konzentrationen multivalente positive Ionen in einer weiten Oberfläche der RNA, der sogenannten großen Furche, niederlassen. Dort bilden sie „Kationenklemmen“, die über die Furche schlagen, ihre Seiten zusammenziehen, die Helix strecken und sie steifer machen. Die DNA, deren Furchen anders geformt sind, bindet diese Ionen hauptsächlich entlang ihres äußeren Rückgrats. Bei sehr hohen Salzkonzentrationen drängen jedoch viele negative Ionen — wie Chlorid — dicht an das RNA-Rückgrat heran und sogar in die große Furche. Ihre Anwesenheit stört die geordneten Klemmen und zerlegt sie in unregelmäßige, fleckenhafte „lokale Klemmen“, die die Helix verzerren. Wenn die Forschenden diesen Effekt in Simulationen nachahmten, indem sie künstliche Federn hinzufügten oder zusätzliche negative Ionen nahe der RNA einkapselten, bog sich das RNA-Rückgrat stärker und seine Gesamtsteifigkeit brach zusammen, genau wie in den Experimenten beobachtet.
Was das für zukünftige RNA-Technologien bedeutet
Vereinfacht gesagt zeigt die Studie, dass RNA entweder gerader und steifer oder stärker geknickt und flexibler gemacht werden kann, allein durch Änderung des Typs und der Konzentration der umgebenden Salze. Bei moderaten Konzentrationen multivalenter Ionen klemmen positive Ladungen gleichmäßig die Außenseite der RNA und stützen sie; bei extremen Konzentrationen brechen eindringende negative Ionen diese einheitliche Stütze und erzeugen verzerrte, weichere Bereiche. DNA zeigt dieses starke Erweichen nicht, weil sie Ionen anders bindet und stattdessen eine Nettoladungsumkehr erfährt. Diese Erkenntnisse machen deutlich, dass nicht nur positive Ionen, sondern auch ihre negativen Partner entscheidend für die Kontrolle der RNA-Form sind. Dieses Wissen wird Forschenden helfen, die Mechanik von RNA im Labor gezielt zu steuern — zum Beispiel um RNA-Medikamente zu stabilisieren, die Faltung von RNA in Biosensoren zu kontrollieren oder zuverlässigere RNA-basierte Nanostrukturen zu entwerfen.
Zitation: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Schlüsselwörter: RNA-Mechanik, multivalente Ionen, Kationenklemmen, DNA versus RNA, Salzeffekte