Clear Sky Science · de
CISH, ein wichtiger intrazellulärer Checkpoint, im Vergleich und in Kombination mit bestehenden und aufkommenden Krebs-Immuncheckpoints
Die Bremsen der krebsbekämpfenden Zellen lösen
Krebsimmuntherapien haben die Perspektive für viele Patientinnen und Patienten verändert, doch ein großer Teil profitiert weiterhin kaum oder gar nicht. Diese Studie untersucht einen neuen Weg, die körpereigenen T‑Zellen – die Vollstrecker des Immunsystems – zu verstärken, indem eine interne „Bremse“ namens CISH ausgeschaltet wird. Im Gegensatz zu aktuellen Medikamenten, die an Schaltern an der Zelloberfläche ansetzen, zielt diese Strategie auf ein Steuerungssystem ab, das tief im Zellinneren liegt, mit dem Ziel, gentechnisch veränderte T‑Zellen deutlich besser darin zu machen, Tumore zu finden und zu zerstören, selbst wenn Krebszellen versuchen, sich zu verbergen.
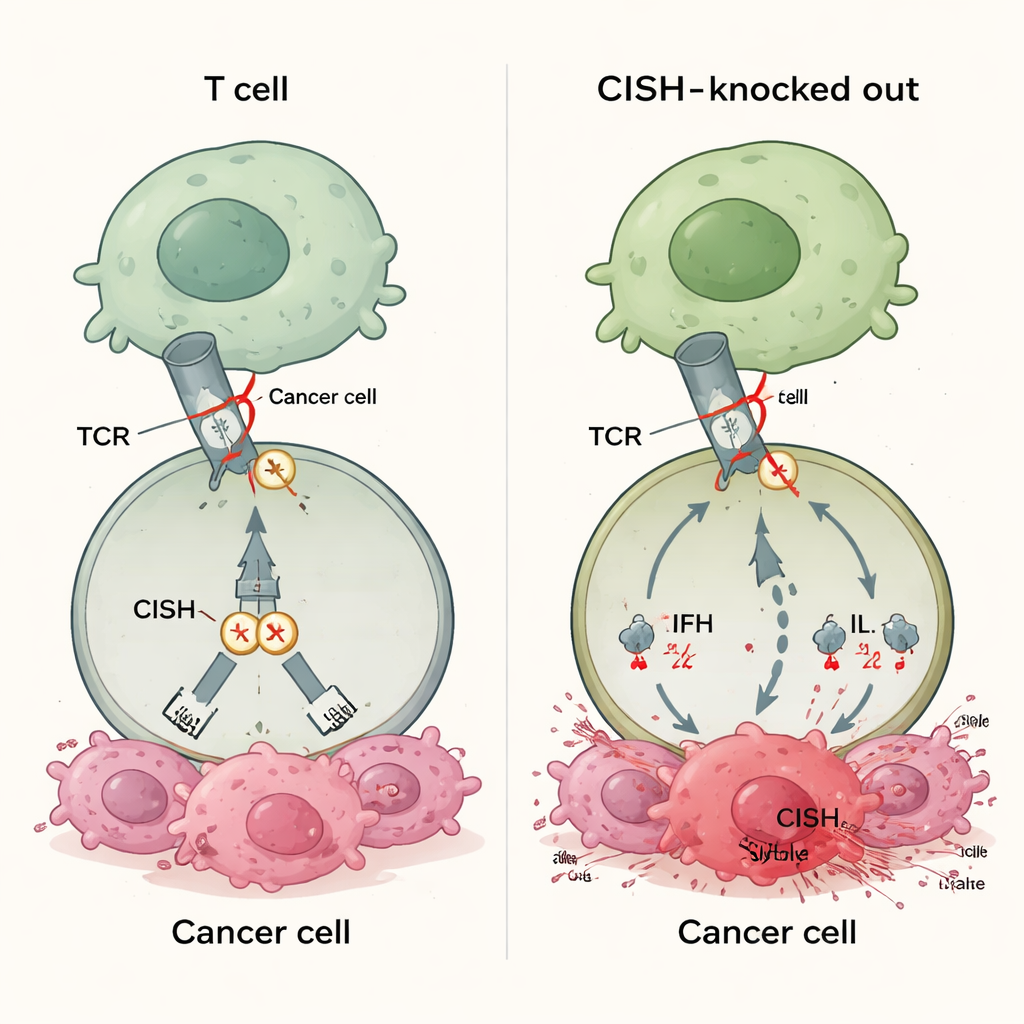
Eine neue Art von Immunbremse
Die meisten zugelassenen Immuntherapie‑Medikamente blockieren Proteine wie PD‑1 an der Oberfläche von T‑Zellen. Diese Medikamente wirken nur, wenn Tumore passende Gegenmoleküle wie PD‑L1 zeigen, und viele Krebsarten exprimieren diese Partner entweder nie in ausreichender Menge oder verlieren sie im Verlauf der Erkrankung. Das trägt dazu bei, dass 30–60 % der Patientinnen und Patienten nicht auf heutige Checkpoint‑Therapien ansprechen. CISH gehört zu einer anderen Klasse von Bremsen, die innerhalb der T‑Zelle sitzen. Es wird eingeschaltet, wenn der T‑Zell‑Rezeptor ein Ziel erkennt, und dämpft dann das Signal, indem es die Zerstörung eines zentralen Signalproteins fördert. Da diese Wirkung nicht von tumorexprimierten Liganden abhängt, könnte das Ausschalten von CISH prinzipiell die T‑Zell‑Antworten bei vielen Krebsarten verstärken, unabhängig vom PD‑L1‑Status oder anderen Biomarkern.
Direkter Vergleich mit bestehenden Checkpoints
Die Forschenden nutzten CRISPR‑Geneditierung, um CISH zu entfernen, und verglichen die resultierenden T‑Zellen mit solchen, denen PD‑1 oder mehrere andere intrazelluläre Bremsen fehlten. Bei schwacher Stimulation – eine Situation, die Tumore nachahmen soll, die nur geringe Antigenmengen zeigen – produzierten CISH‑entfernte Zellen deutlich mehr wichtige Immunbotenstoffe, darunter Interferon‑gamma, TNF‑alpha und IL‑2. Diese Zellen waren außerdem polyfunktionaler, das heißt einzelne T‑Zellen konnten mehrere Aufgaben gleichzeitig erfüllen, ein Kennzeichen starker anti‑tumoraler Aktivität. Im Gegensatz dazu half das alleinige Entfernen von PD‑1 unter diesen Niedrigsignalbedingungen nicht. In zahlreichen Tests steigerte der Verlust von CISH stärker die Aktivierung, die Abtötungskapazität und die Ausbildung langlebiger, gedächtnisähnlicher T‑Zellen als das Ausschalten anderer intrazellulärer Kandidaten wie RASA2, CBLB, SOCS1, REGNASE1, HPK1 oder PTPN1/2.
Zusammenspiel mit anderen internen Schaltern
Da die T‑Zell‑Signalgebung von vielen sich überschneidenden Pfaden gesteuert wird, prüfte das Team, ob die Kombination der CISH‑Entfernung mit dem Entfernen weiterer Bremsen additive Vorteile bringen könnte. Mit multipler CRISPR‑Editierung fanden sie, dass das Entfernen von CISH zusammen mit SOCS1, HPK1 oder RASA2 die Produktion hilfreicher Zytokine bei schwacher Stimulation weiter erhöhte. In einem Tumormodell, das auf einer häufigen KRAS‑Mutation basiert, waren T‑Zellen, die mit einem KRAS‑spezifischen Rezeptor ausgestattet waren, besser im Abtöten von Krebszellen, wenn CISH entfernt war, und dieser Effekt wurde stärker, wenn der CISH‑Verlust mit der Deletion von SOCS1 oder RASA2 kombiniert wurde. Diese Befunde deuten darauf hin, dass CISH einen nicht redundanten Knotenpunkt in der T‑Zell‑Biologie kontrolliert und mit ausgewählten Partnern zusammenarbeiten kann, um tumorspezifisches Töten zu schärfen.
CAR‑T‑Zellen widerstandsfähiger gegen trickreiche Tumore machen
Die Autorinnen und Autoren richteten den Blick dann auf einen klinisch wichtigen Anwendungsfall: CAR‑T‑Zellen, die auf den B‑Zell‑Marker CD19 zielen. Sie erzeugten Leukämiezellen mit unterschiedlichen CD19‑Niveaus, um Tumore zu imitieren, die ihre Ziele abgeben oder reduzieren, um der Therapie zu entkommen. CAR‑T‑Zellen ohne CISH waren deutlich besser darin, Krebszellen zu zerstören, selbst wenn CD19 knapp war, und schütteten mehr aktivierende und rekrutierende Signale aus. Gleichzeitig setzten sie geringere Mengen an Molekülen frei, die dafür bekannt sind, T‑Zellen zu schwächen oder Tumorwachstum zu fördern, wie Galectin‑1, Galectin‑3, lösliches 4‑1BB, IL‑1α und das Glykoprotein EMMPRIN/CD147. Zusammengenommen deuten diese Veränderungen auf eine aggressivere, weniger leicht unterdrückbare CAR‑T‑Zelle hin, die besonders gut für feindliche Tumorumgebungen mit niedrigem Antigengehalt geeignet ist.
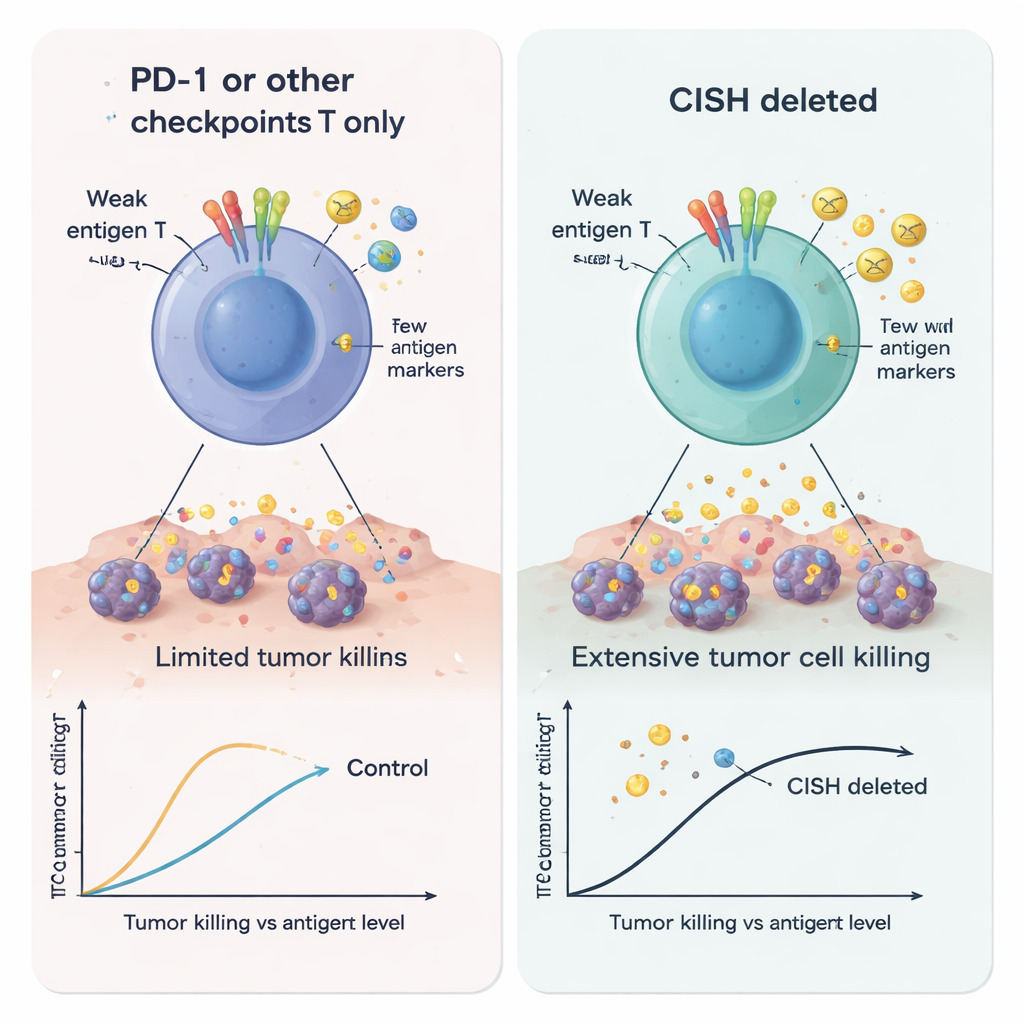
Vom Labortisch zu den Patientinnen und Patienten
Über Reagenzgläser und Kulturschalen hinaus hat die Idee, CISH anzugreifen, bereits Patientinnen und Patienten erreicht. Eine First‑in‑Human‑Studie mit tumorinfiltrierenden Lymphozyten, die so editiert wurden, dass CISH entfernt ist, führte bei einer Person mit fortgeschrittenem kolorektalem Krebs zu einem kompletten Ansprechen, das länger als zwei Jahre anhält, trotz der Resistenz des Tumors gegen mehrere frühere Behandlungen. Indem die Studie zeigt, dass CISH ein mächtiger, zugänglicher interner Checkpoint ist, der die Empfindlichkeit von T‑Zellen gegenüber selbst schwachen Tumorsignalen erhöht, erklärt sie dieses bemerkenswerte klinische Ergebnis und stützt Bemühungen, künftige Therapien zu entwickeln – sei es gentechnisch veränderte Zellen oder Tabletten –, die diese interne Bremse sicher lockern und die Reichweite der Krebsimmuntherapie erweitern.
Zitation: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Schlüsselwörter: Krebsimmuntherapie, T-Zellen, CAR-T-Therapie, Immuncheckpoints, CRISPR-Geneditierung