Clear Sky Science · de
Eine pathogene Mutation in α‑SNAP beeinträchtigt die Bindung an Membranlipide, indem sie eine entscheidende hydrophobe Schleife verschleiert
Wie eine winzige Proteinveränderung die Gehirnentwicklung stören kann
Unsere Gehirnzellen transportieren ständig Fracht in winzigen Bläschen, den Vesikeln, und ein Helferprotein namens alpha‑SNAP ist zentral für das Gelingen dieser Lieferungen. Eine seltene Mutation in alpha‑SNAP, bekannt aus einer Mäuselinie namens „hyh“, führt zu schweren Problemen bei der Gehirnbildung und der Flüssigkeitsregulation. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Verhindert diese Einzelaminosäureänderung, dass alpha‑SNAP an Zellmembranen andockt, und könnte genau das ein Hauptgrund für die Fehlentwicklung des Gehirns sein?
Ein zellulärer Hafenarbeiter mit vielen Aufgaben
Alpha‑SNAP arbeitet normalerweise wie ein Hafenarbeiter für Vesikel und hilft ihnen dabei, mit Zellmembranen zu verschmelzen, damit Fracht freigesetzt oder recycelt werden kann. Es kooperiert mit einer Gruppe von Proteinen, den SNAREs, und einer energieverbrauchenden Maschine namens NSF, um Membranen zusammenzuführen und das System anschließend für die nächste Runde zurückzusetzen. Über diese klassische Rolle hinaus steuert alpha‑SNAP auch Prozesse wie die Zellreinigung (Autophagie), programmierten Zelltod, Kalziumeinstrom und Energiesensorik. All diese Funktionen hängen, in der einen oder anderen Form, von der Fähigkeit von alpha‑SNAP ab, die ölige Membranoberfläche zu berühren und teilweise in sie einzudringen.
Eine verborgene Schleife und eine problematische Mutation
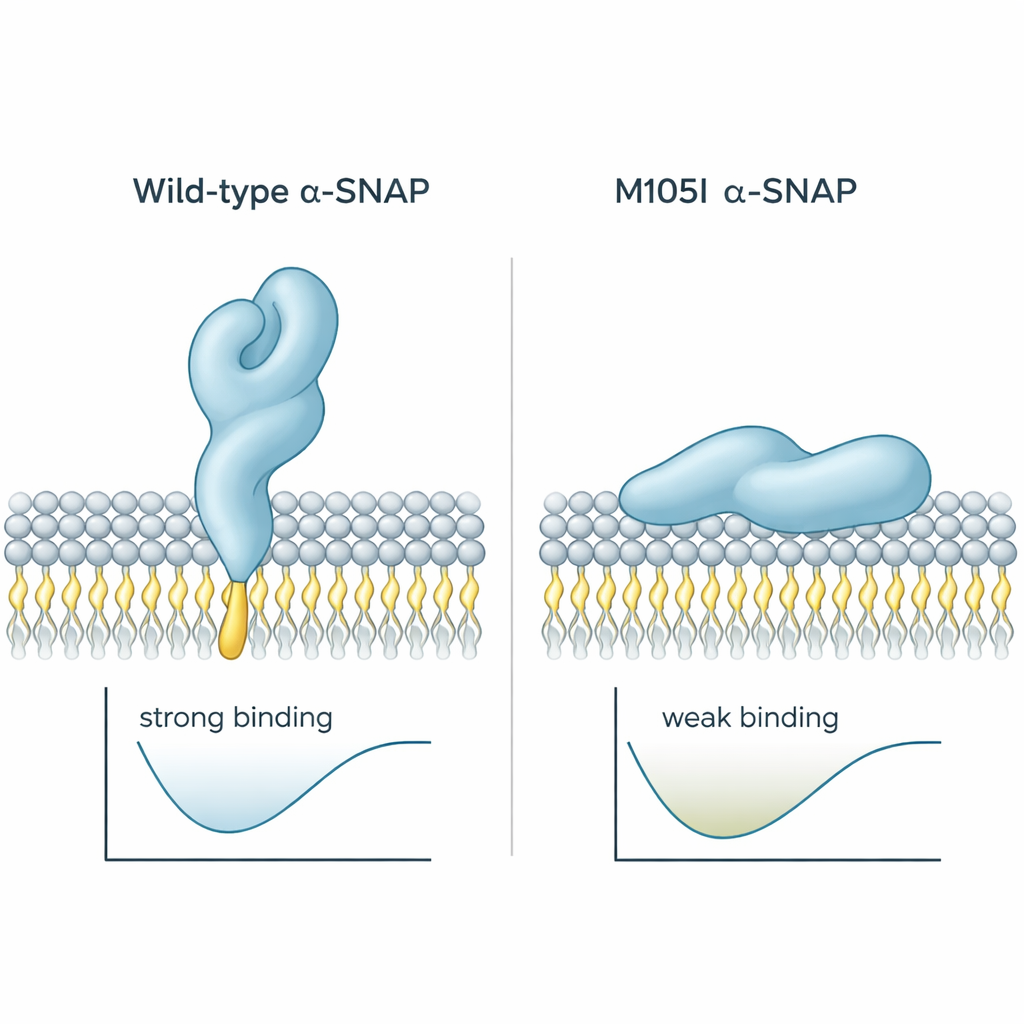
Frühere Arbeiten zeigten, dass alpha‑SNAP eine kurze fettige „Schleife“ nahe einem Ende des Proteins verwendet, um sich an Membranen zu verhaken. Im gesunden Protein ragt diese Schleife heraus und kann in die äußere Schicht der Membran eintauchen. Beim hyh‑Mausmodell wird an Position 105 ein einzelnes Baustein ausgetauscht, was die M105I‑Mutation erzeugt. Die Autoren nutzten Computersimulationen, um zu untersuchen, wie sich diese Änderung auf die Proteinstruktur auswirkt. Sie fanden, dass das mutierte Protein etwas kompakter wird und sich so verdreht, dass die hydrophobe Schleife nach innen geklappt wird, weg vom Wasser und weg von Membranen. Infolgedessen nähert sich das Mutantenprotein Membranen flacher an und drückt eher mit einem weniger klebrigen Bereich gegen sie, wodurch sowohl die Kontaktzeit als auch die Eindringtiefe verringert werden. Berechnungen der Bindungsenergie stützten dies: Das Wildtyp‑Protein fand einen niedrigenergetischen, stark gebundenen Zustand, während das Mutantenprotein schwächere, oberflächlichere Kontakte bevorzugte.
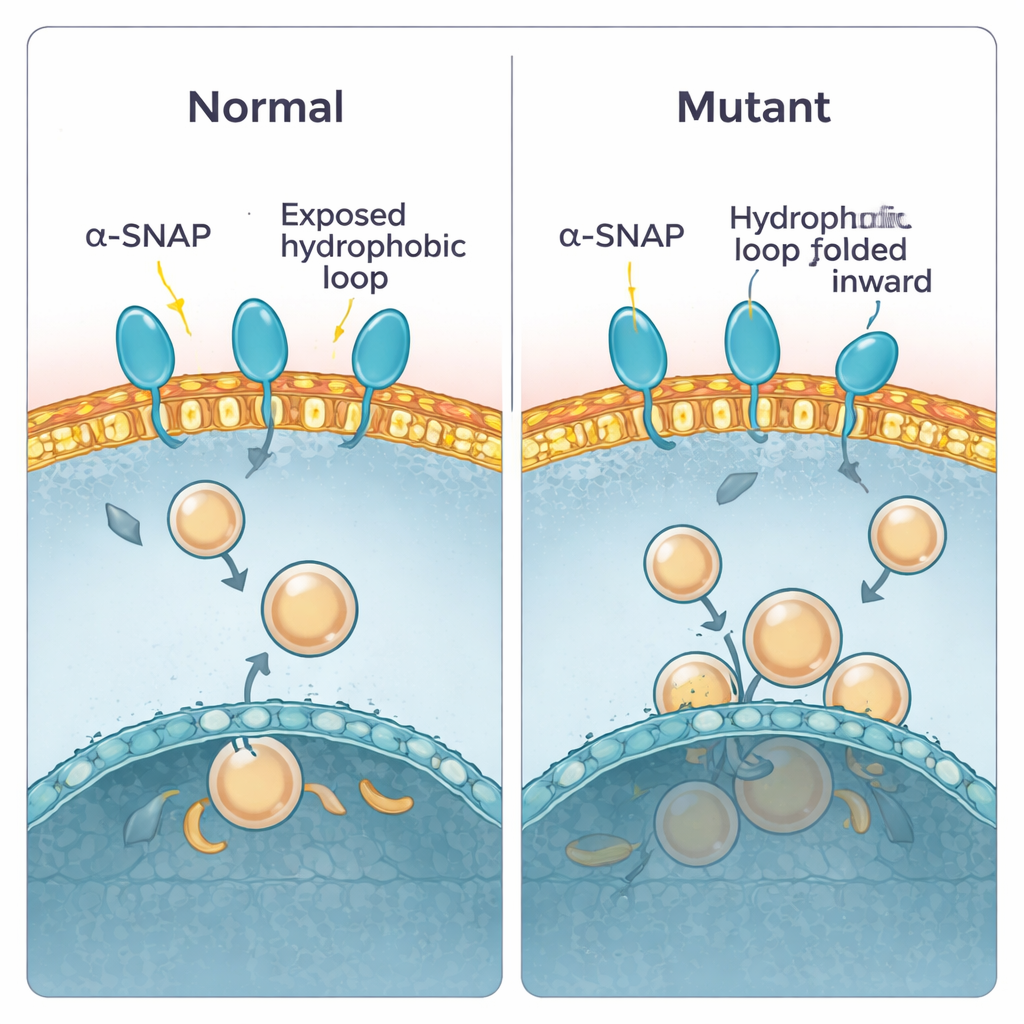
Die Vorhersage im Labor prüfen
Um diese Vorhersagen zu testen, reinigte das Team sowohl das normale als auch das mutierte alpha‑SNAP und untersuchte ihr Verhalten in verschiedenen Experimenten. Zuerst nutzten sie ein Detergens, das sich in eine wässrige und eine ölige Phase trennt, um die Wahl zwischen Wasser und Membran zu simulieren. Normales alpha‑SNAP verteilte sich ausgeglichen, was mit einer ausgeglichenen, teilweise fettigen Oberfläche übereinstimmt. Die mutierte Variante war weniger bereit, in die ölige Phase überzugehen, was darauf hindeutet, dass ihre fettigen Bereiche tatsächlich stärker vergraben sind. Anschließend ließen sie die Proteine mit flachen Plasmamembran‑„Folien“ aus Zellen interagieren und bildeten ab, wie viele Bindungsstellen erschienen. Wiederum punktete das normale alpha‑SNAP die Membran, während das Mutantenprotein deutlich weniger band. Schließlich ließen sie künstliche Membranbläschen (Liposome) aus Gehirnlipiden durch Zuckergradienten schweben. Wildtyp‑alpha‑SNAP stieg mit Vesikeln reich an Plasmamembranlipiden nach oben, während das Mutantenprotein zurückblieb und schlecht band, es sei denn, die Vesikel bestanden aus einer anderen, eher internen Membranmischung.
Folgen im sich entwickelnden Gehirn
Die Forscher richteten ihren Blick anschließend auf die Gehirne sich entwickelnder Mausembryonen, speziell auf eine Phase, in der neue Nervenzellen entstehen. Durch die Trennung zellulärer Inhalte in lösliche und membrangebundene Anteile zeigten sie, dass die Gesamtmengen an alpha‑SNAP in hyh‑Gehirnen bereits reduziert waren, aber noch wichtiger war, dass der Anteil, der an Membranen haftet, im Vergleich zu normalen Mäusen unverhältnismäßig niedrig war. Bei einer weiteren Auftrennung verschiedener Membrantypen stellte sich heraus, dass der größte Verlust an der Plasmamembran, der äußeren Zelloberfläche, zu verzeichnen war, während interne Membranen deutlich weniger betroffen waren. Die Mikroskopie erzählte dieselbe Geschichte: In normalem Gewebe zeichnete alpha‑SNAP Zellen in einem bienenwabenartigen Muster nach, das mit einem bekannten Oberflächenmarker übereinstimmte. In hyh‑Gehirnen verblasste diese klare Randfärbung zu einem diffuseren, internen Leuchten, was darauf hindeutet, dass das mutierte Protein nicht an der Zellkante verankert bleibt, wo Vesikelfusion und Signalübertragung am aktivsten sind.
Warum das für Krankheiten wichtig ist
Zusammengefasst zeigen die Ergebnisse, dass die M105I‑Mutation mehr bewirkt, als nur die Menge an alpha‑SNAP zu verringern; sie verändert die Faltung des Proteins so, dass die entscheidende membranfassende Schleife verborgen wird. Dadurch fällt es alpha‑SNAP schwerer, die Plasmamembran zu erfassen und die richtige Orientierung zur Organisation der Fusionsmaschinerie einzunehmen. In einem sich entwickelnden Gehirn, in dem die präzise Lieferung von Signalen und Baumaterialien an der Zelloberfläche essenziell ist, trägt diesen subtilen Strukturfehlern vermutlich zu Hydrozephalus, fehlgeleiteter Cortexbildung und anderen Defekten bei, die bei hyh‑Mäusen beobachtet werden. Für Nicht‑Spezialisten ist die Botschaft klar: Schon eine winzige Formänderung eines einzelnen Proteins kann verändern, wie Zellen kommunizieren und damit wie ein Gehirn gebaut wird.
Zitation: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Schlüsselwörter: alpha‑SNAP, Membranbindung, Proteinmutation, Gehirnentwicklung, Vesikelfusion