Clear Sky Science · de
Entwicklung von Capsaicin-abgeleiteten Prohibitin-Liganden zur Modulation der Aurora-Kinase A/PHB2-Interaktion und der Mitophagie in Krebszellen
Warum ein Chili-Chemikalie für Krebs wichtig ist
Chilis verdanken ihre Schärfe dem Capsaicin, einem kleinen Molekül, das an Proteine in unseren Zellen bindet. Diese Studie untersucht eine überraschende Wendung dieses vertrauten Gewürzes: Forschende haben Capsaicin neu gestaltet, um neue, arzneimittelähnliche Moleküle zu erzeugen, die gezielt die „Kraftwerke“ von Krebszellen – die Mitochondrien – ansteuern und einen Prozess dämpfen, den diese Zellen nutzen, um ihre Energiemanagementsysteme in Schuss zu halten. Da Krebszellen stark auf effiziente Mitochondrien angewiesen sind, um unkontrolliertes Wachstum zu treiben, könnte die selektive Störung dieses Unterstützungsmechanismus einen neuen Weg für Krebstherapien eröffnen.
Die Zellkraftwerke und ihre interne Aufräumtruppe
Mitochondrien balancieren ständig zwischen dem Aufbau neuer Einheiten und dem Recycling beschädigter Organelle. Die Recycling-Seite, Mitophagie genannt, funktioniert als Qualitätskontrolle: Abgenutzte Mitochondrien werden markiert und abgebaut, während gesündere erhalten bleiben. Viele Krebszellen kapern dieses Gleichgewicht und nutzen Mitophagie, um schwächere Mitochondrien auszusortieren und „Top-Performer“ anzureichern, die große Mengen ATP – die Energiewährung der Zelle – produzieren. Ein Protein namens Aurora-Kinase A (AURKA), das in Tumoren oft überexprimiert ist, wurde kürzlich auch in Mitochondrien nachgewiesen, wo es mit einem weiteren Protein, Prohibitin‑2 (PHB2), und dem Autophagie-Adaper LC3 zusammenarbeitet. Gemeinsam bilden sie einen Komplex, der Mitophagie fördert und die hohe Energieproduktion in Krebszellen unterstützt.
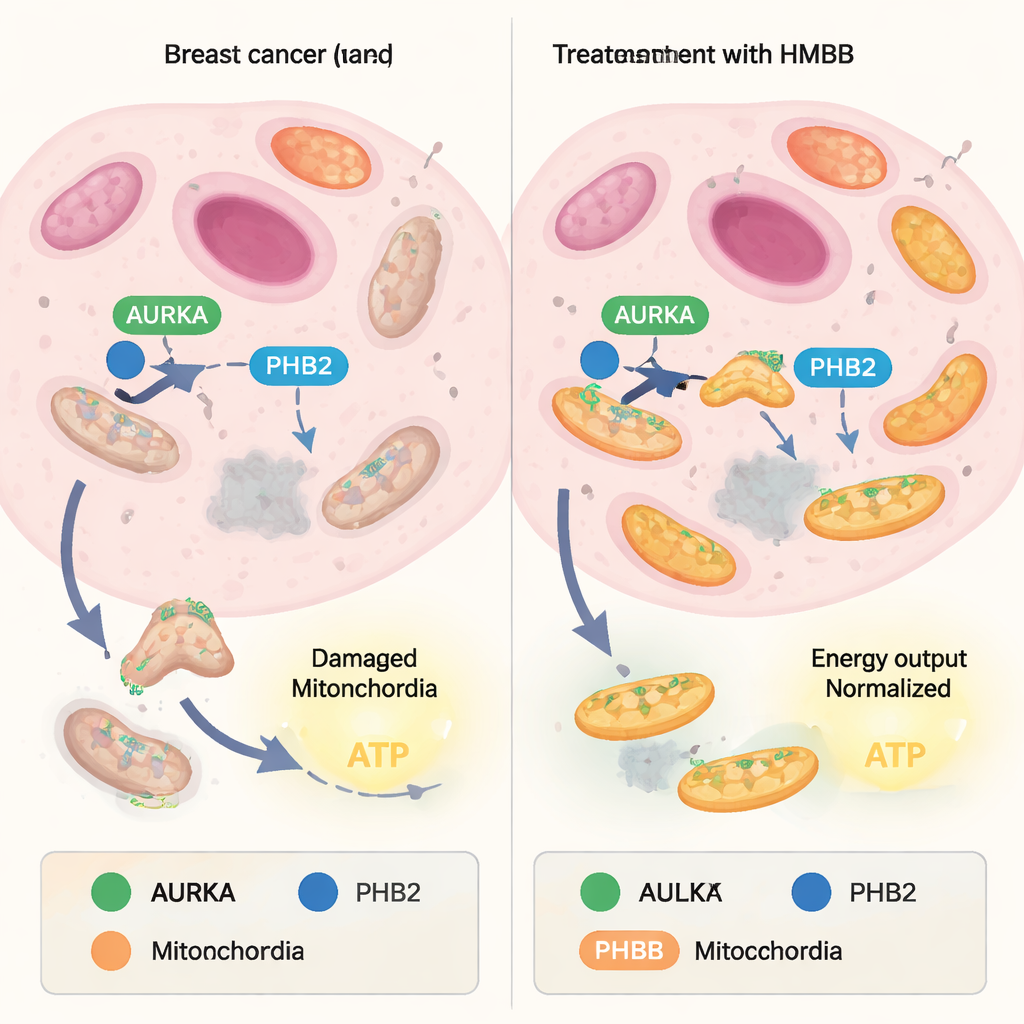
Vom scharfen Capsaicin zu gezielten molekularen Werkzeugen
Frühere Arbeiten hatten gezeigt, dass eine natürliche Verbindung namens Xanthohumol an PHB2 binden und den AURKA–PHB2–LC3-Komplex stören kann, wodurch Mitophagie gehemmt und die mitochondriale ATP-Produktion reduziert wird. Die chemische Struktur von Xanthohumol ist jedoch für die Arzneimittelentwicklung nicht ideal. In dieser Studie wandten sich die Autorinnen und Autoren Capsaicin zu, einem weiteren natürlichen PHB-Liganden, und fragten, ob es sich in praktischere Werkzeuge umformen lässt. Zuerst bestätigten sie, dass Capsaicin die Interaktion zwischen AURKA und PHB2 in lebenden Brustkrebszellen leicht abschwächt, mithilfe einer Bildgebungstechnik (FRET/FLIM), die misst, wie nahe zwei markierte Proteine beieinanderliegen. Anschließend synthetisierten sie 16 Capsaicin-inspirierte Moleküle, indem sie den „Schwanz“ und den aromatischen „Kopf“ der Ausgangsstruktur modifizierten, und testeten systematisch, wie jede Variante die AURKA–PHB2-Partnerschaft innerhalb der Mitochondrien beeinflusste.
Entdeckung eines molekularen „Klebers“, der Proteine zusammenhält
Die modifizierten Moleküle zeigten auffallend unterschiedliche Effekte. Einige, wie Capsaicin selbst oder ein Derivat namens Verbindung 5, ließen AURKA und PHB2 leichter auseinandergehen. Andere taten nahezu nichts. Ein Teil davon – insbesondere ein Molekül namens Verbindung 13, später HMBB genannt – hatte jedoch den gegenteiligen Effekt und verstärkte die Bindung zwischen AURKA und PHB2 deutlich. Computergestützte Docking-Simulationen halfen, dieses Verhalten zu erklären. Capsaicin und Verbindung 5 neigten dazu, in die aktive Stelle von AURKA zu ragen und physische Kollisionen mit PHB2 zu erzeugen, die die Proteine auseinanderdrängten. Im Gegensatz dazu schlüpften Verbindungen 12 und 13 in die AURKA-Aktive Stelle und kontaktierten gleichzeitig eine bekannte hemmende Tasche auf PHB2, ohne eine Kollision zu verursachen. Ihre Form erlaubte es ihnen vielmehr, als „molekularer Kleber“ zu wirken, AURKA und PHB2 zu überbrücken und den Komplex zu stabilisieren.
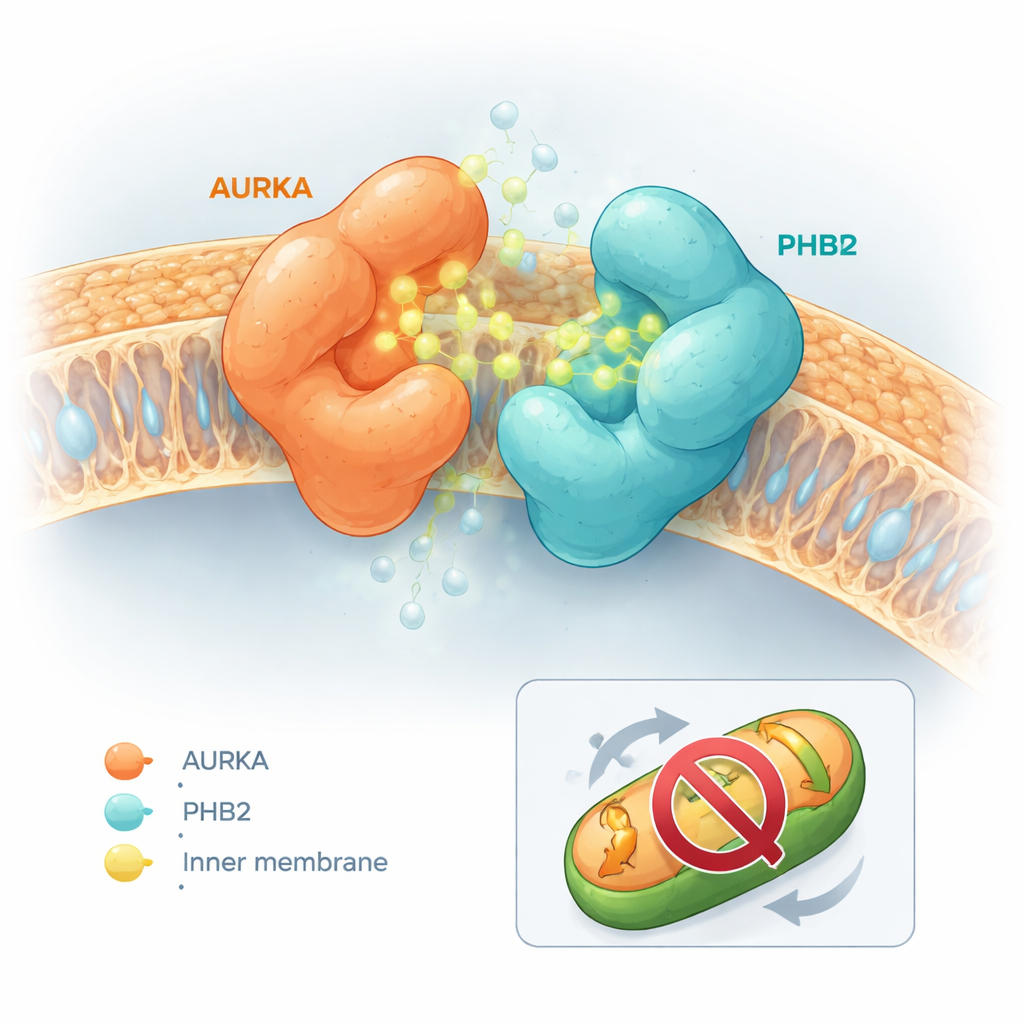
Die mitochondriale Aufräumarbeit blockieren, ohne das Kontrollzentrum der Zelle abzuschalten
Eine entscheidende Frage war, ob dieses Verhalten als molekularer Kleber AURKA im ganzen Zellinneren deaktiviert – was breite Nebenwirkungen verursachen könnte – oder ob es selektiver wirkt. Mit einem separaten fluoreszenten Biosensor, der die AURKA-Aktivierung an Centrosomen meldet – den Strukturen, die die Zellteilungsmaschinerie organisieren – beobachtete das Team, dass HMBB die AURKA-Aktivität an diesen Orten nicht dämpfte. In mitochondrialen Tests jedoch kehrte HMBB den Verlust an mitochondrialer Masse um, der normalerweise durch AURKA-Überexpression in Brustkrebszellen verursacht wird. In Zellen, die natürlicherweise hohe AURKA-Spiegel aufweisen, erhöhte HMBB den mitochondrialen Gehalt, was darauf hindeutet, dass AURKA-getriebene Mitophagie blockiert wurde. In Zellen mit niedrigen AURKA-Leveln hatte HMBB kaum Wirkung, was die Abhängigkeit von dem AURKA–PHB2-Weg unterstreicht.
Was das für zukünftige Krebstherapien bedeuten könnte
Zusammengefasst zeigen die Ergebnisse, dass sorgfältig designte Capsaicin-Derivate die Art und Weise, wie AURKA und PHB2 in Mitochondrien interagieren, fein abstimmen können. Indem sie als molekularer Kleber wirken, fixieren HMBB und verwandte Verbindungen AURKA und PHB2 in einer Konfiguration, die das normale Mitophagie-Programm am Fortgang hindert, ohne AURKAs essentielle Funktionen an anderen Orten der Zelle auszuschalten. Für eine nichtfachliche Leserin oder einen nichtfachlichen Leser ist die Kernaussage, dass die Autorinnen und Autoren Prototypmoleküle entwickelt haben, die selektiv in die Mechanismen eingreifen, mit denen Krebszellen ihre Kraftwerke in Schuss halten, wodurch deren Energieversorgung geschwächt werden könnte, während normale Zellfunktionen verschont bleiben. Obwohl diese Verbindungen noch in einem frühen, laborbasierten Entwicklungsstadium sind, illustrieren sie eine vielversprechende Strategie: kleine, arzneimittelähnliche Moleküle zu nutzen, um spezifische Proteinpartnerschaften innerhalb der Mitochondrien anzuvisieren und dadurch die metabolischen Vorteile vieler Tumore zu untergraben.
Zitation: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Schlüsselwörter: Mitochondrien, Mitophagie, Aurora-Kinase A, Capsaicin-Derivate, Krebsmetabolismus