Clear Sky Science · de
Funktionelle Umprogrammierung von iNKT-Zellen durch sulfatidreaktive Typ‑II‑NKT‑Zellen verwandelt alveoläre Makrophagen und lindert Lungen-Ischämie‑Reperfusions‑Schäden
Warum es wichtig ist, Spenderlungen zu schützen
Wenn Chirurgen eine Lunge transplantieren oder den Blutfluss nach einer Blockade wiederherstellen, kann die plötzliche Rückkehr von Sauerstoff paradoxalerweise das Gewebe schädigen. Dieses Problem, Lungen‑Ischämie–Reperfusions‑Schaden genannt, ist eine bedeutende Ursache für frühe Misserfolge nach Lungentransplantationen und anderen kritischen Eingriffen. Die hier zusammengefasste Studie untersucht, wie eine seltene Gruppe von Immunzellen „umprogrammiert“ werden kann, um Entzündungen zu dämpfen, und damit einen potenziell neuen Ansatz zum Schutz verletzlicher Lungen in kritischen Momenten bietet.
Immunzellen, die heilen oder schaden können
Unsere Lungen werden von alveolären Makrophagen überwacht, Immunzellen, die in den Lungenbläschen sitzen und schnell auf Gefahren reagieren. Diese Zellen können zwischen zwei Hauptmodi wechseln. In einem „Kampf“-Modus (häufig M1 genannt) schütten sie entzündungsfördernde Substanzen aus, die zwar Keime bekämpfen, aber auch Gewebe schädigen können. Im „Reparatur“-Modus (häufig M2 genannt) setzen sie dämpfende Moleküle frei, die Entzündungen begrenzen und die Heilung fördern. Bei Lungen‑Ischämie–Reperfusion verschiebt sich das Gleichgewicht zugunsten des schädlichen Kampfmodus. Die Forscher vermuteten, dass eine gezielte Verschiebung der Makrophagen hin zum Reparaturmodus zum richtigen Zeitpunkt den Schaden abmildern könnte.
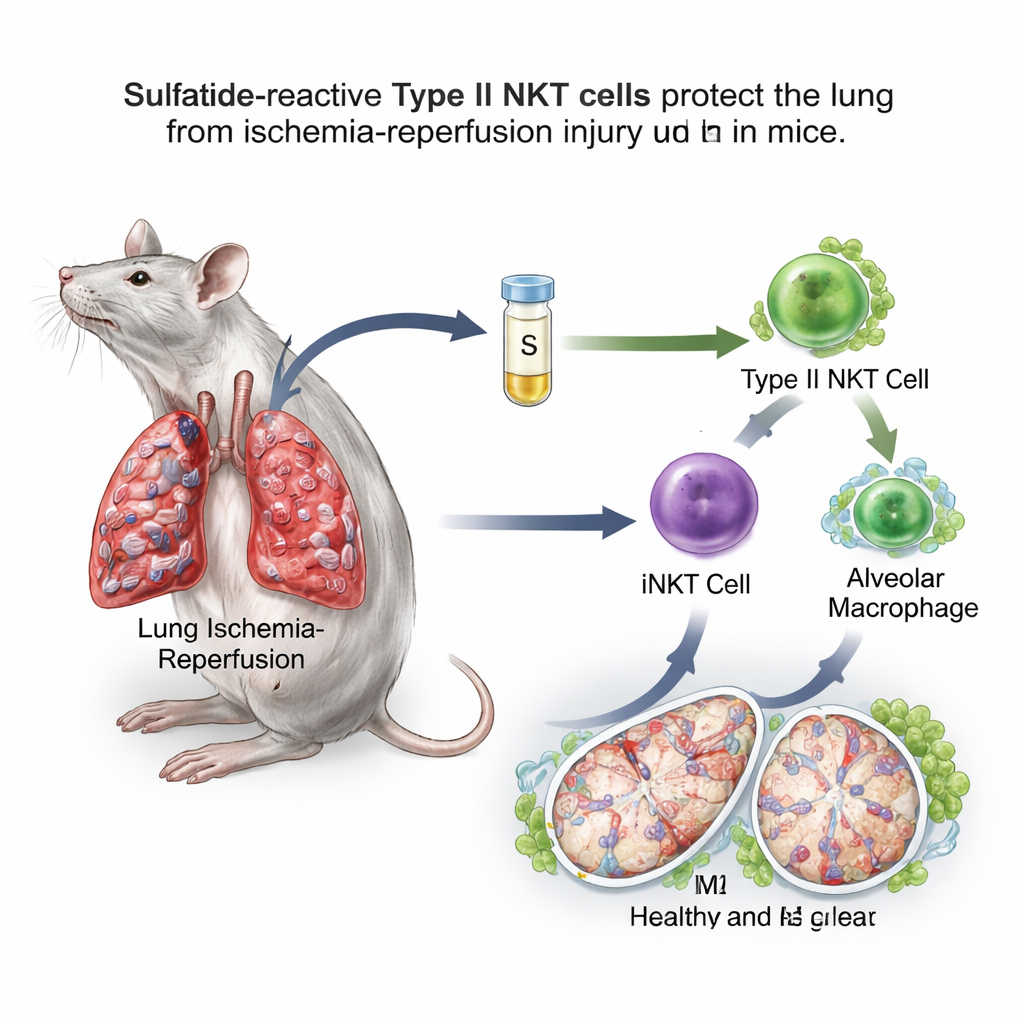
Ein Zucker‑Fett‑Molekül kippt einen Immun‑Schalter
Das Team konzentrierte sich auf natürliche Killer‑T‑Zellen (NKT‑Zellen), ungewöhnliche Immunzellen, die zwischen schnellen angeborenen Abwehrreaktionen und langsameren, zielgerichteten Antworten stehen. NKT‑Zellen gibt es in zwei Haupttypen. Typ I, auch invariante NKT (iNKT)‑Zellen genannt, sind dafür bekannt, Lungen‑Ischämie–Reperfusions‑Schäden bei Mäusen zu verschlimmern. Typ II NKT‑Zellen können hingegen in anderen Organen Immunreaktionen zurückhalten. Ein Fettsäuremolekül namens Sulfatid wird speziell von Typ‑II‑NKT‑Zellen erkannt. In einem Mausmodell, bei dem der Blutfluss zu einer Lunge für eine Stunde unterbrochen und dann wiederhergestellt wurde, verabreichten die Forscher Sulfatid mehrere Stunden vor dem Ereignis. Sie stellten fest, dass sulfatidbehandelte Mäuse im Vergleich zu unbehandelten Tieren weniger Lungenödem, weniger durchlässige Blutgefäße, geringeren oxidativen Stress, bessere Sauerstoffwerte und reduzierte Entzündungsstoffe in der Lungenlavage aufwiesen.
Umprogrammierung von Makrophagen durch eine Signalkette
Genauere Untersuchungen zeigten, dass Sulfatid die alveolären Makrophagen in Richtung des reparaturorientierten M2‑Zustands verschob. Diese Makrophagen zeigten mehr Oberflächenmarker und Gene, die mit Heilung verbunden sind, und waren beim Übertragen in andere Mäuse besser darin, Entzündungen zu dämpfen. Als die Wissenschaftler selektiv alveoläre Makrophagen entfernten, verschlechterte sich der Lungenschaden und der schützende Effekt von Sulfatid ging weitgehend verloren, was zeigt, dass diese Zellen eine zentrale Rolle in der Signalachse spielen. Bedeutend ist, dass der Nutzen von Sulfatid in Mäusen, denen entweder Typ‑II‑NKT‑Zellen oder Typ‑I‑iNKT‑Zellen fehlten, verschwand, sich aber durch die Rückübertragung von iNKT‑Zellen, die zuvor Sulfatid ausgesetzt waren, wiederherstellen ließ. Zusammengenommen zeigen diese Experimente eine Staffelung: Sulfatid aktiviert Typ‑II‑NKT‑Zellen, die wiederum das Verhalten von iNKT‑Zellen umformen, und diese programmieren die alveolären Makrophagen um.
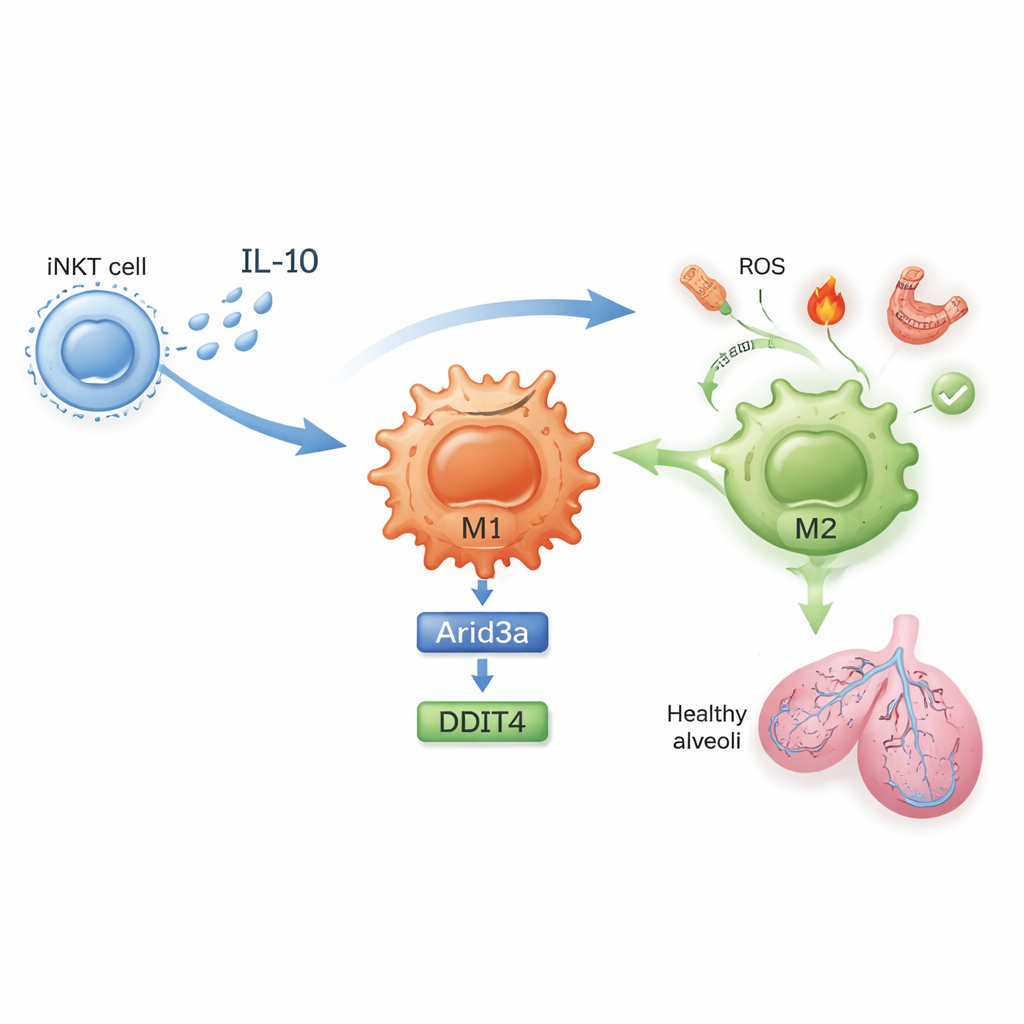
Eine molekulare Kette, die Entzündung beruhigt
Was ändert sich genau in diesen Zellen? In unbehandelten Mäusen proliferierten Lungen‑iNKT‑Zellen während Ischämie–Reperfusion und produzierten hohe Mengen an Interferon‑gamma, ein starkes entzündungsförderndes Signal. Nach Sulfatid‑Exposition produzierte iNKT‑Zellen stattdessen mehr Interleukin‑10 (IL‑10), ein potentes antiinflammatorisches Molekül, und weniger Interferon‑gamma. Die Studie zeigt, dass IL‑10 aus iNKT‑Zellen direkt auf Makrophagen wirkt, um ihre M2‑Polarisation zu fördern. Mithilfe von Genexpressionsprofilen und genau gestalteten Zellkulturversuchen entdeckten die Autoren eine molekulare Kaskade in Makrophagen: IL‑10 erhöht einen Transkriptionsfaktor namens Arid3a, der wiederum ein Stressantwort‑Gen namens DDIT4 hochfährt. Diese Arid3a–DDIT4‑Achse hilft, einen wachstumssteuernden Signalweg herunterzufahren, der sonst Makrophagen in einem entzündlichen Zustand hält, und lenkt sie so zum schützenden M2‑Programm.
Von Mauslungen zu zukünftigen Therapien
Um zu testen, wie zentral diese molekulare Kette ist, setzten die Forscher kleine interferierende RNAs ein, um Arid3a oder DDIT4 in Makrophagen stummzuschalten, bevor sie diese Mäusen übertrugen. Wenn eines der Gene herunterreguliert war, schaffte es Sulfatid nicht mehr vollständig, Makrophagen in den Reparaturmodus zu bringen, und der Lungenschutz war geschwächt. Weitere Analysen deuten darauf hin, dass ein Signalmolekül namens YES1 hilft, sulfatidaktivierte Typ‑II‑NKT‑Zellen so umzuprogrammieren, dass iNKT‑Zellen verstärkt IL‑10 produzieren. Obwohl diese Befunde aus Mausmodellen und aus im Labor veränderten Zellen stammen, zeichnen sie ein klares Bild: Durch eine kurzzeitige Aktivierung einer spezifischen NKT‑Zell‑Untergruppe mit Sulfatid könnte man schädliche Immunreaktionen in schützende verwandeln, die transplantierte oder verletzte Lungen schützen. In Zukunft könnten Medikamente, die diesen Weg nachahmen, mehr Patienten helfen, lebensrettende Lungenverfahren zu überstehen und sich besser zu erholen.
Zitation: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Schlüsselwörter: Lungen‑Ischämie‑Reperfusions‑Schaden, alveoläre Makrophagen, natürliche Killer‑T‑Zellen, Interleukin‑10, Immunmodulation