Clear Sky Science · de
MHC1-TIP ermöglicht ein einstufiges multimodales Immunopeptidom-Profiling und deckt intratumorale Heterogenität in der Antigenpräsentation auf
Blick auf die Identitätskarten von Krebszellen
Jede Zelle trägt winzige molekulare „Ausweiskarten“ auf ihrer Oberfläche, die dem Immunsystem helfen zu entscheiden, ob eine Zelle gesund oder gefährlich ist. Bei Krebs können diese Ausweiskarten — kurze Proteinfragmente, sogenannte Antigene — aufzeigen, was eine Tumorzelle abnorm macht, und sie für die Zerstörung durch Immunzellen markieren. Diese Studie stellt eine neue Labormethode vor, MHC1-TIP, die das Auslesen dieser Ausweise aus sehr kleinen Patientengeweben deutlich einfacher und günstiger macht und damit Möglichkeiten für präzisere Krebsimmuntherapien eröffnet.
Warum Signale auf der Zelloberfläche wichtig sind
Unser Immunsystem überprüft Zellen ständig, indem es die auf speziellen Molekülen, den MHC-Klasse-I-Molekülen, präsentierten Antigene kontrolliert. Tumorzellen zeigen häufig ungewöhnliche Antigene, die von T‑Zellen erkannt und durch Therapien wie personalisierte Impfstoffe gezielt werden könnten. Die tatsächliche Messung, welche Antigene in Patientenproben vorhanden sind, war jedoch technisch anspruchsvoll. Traditionelle Methoden benötigen große Zellmengen, viele Verarbeitungsschritte und teure Antikörper, was sie für winzige Biopsien oder knappe klinische Proben ungeeignet macht. Gleichzeitig sind Tumoren nicht homogen: Unterschiedliche Regionen können unterschiedliche Proteine exprimieren, sodass auch die Antigenpräsentation innerhalb eines einzelnen Tumors variieren kann.
Eine One‑Tube‑Abkürzung zu Krebsantigenen
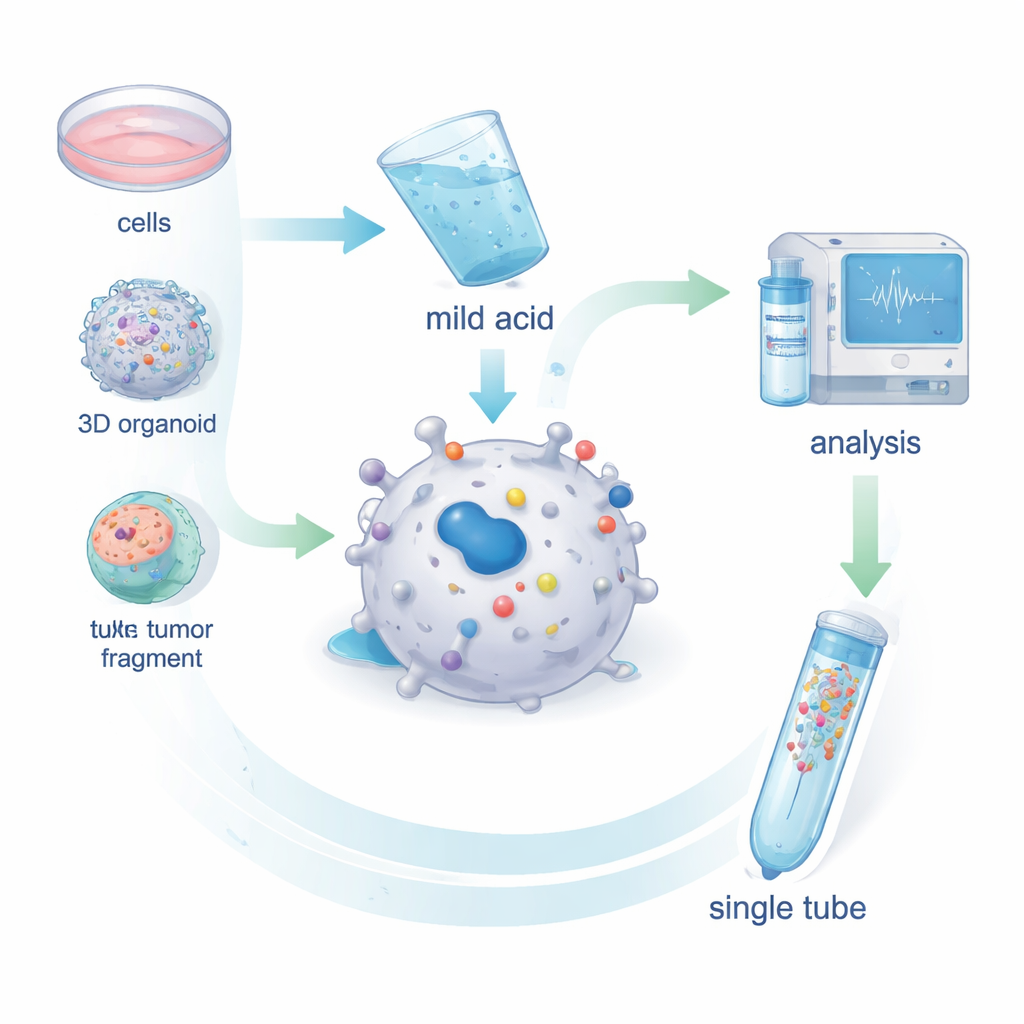
Die Forschenden entwickelten MHC1-TIP (MHC‑I 1‑Tube Immunopeptidomics) als vereinfachtes Verfahren, um Antigene aus lebenden Zellen zu gewinnen. Statt Zellen aufzubrechen und MHC‑Moleküle mit Antikörpern herauszufischen, waschen sie intakte Zellen — oder kleine Tumorfragmente — kurz mit einer milden Säurelösung. Diese schonende Behandlung bewirkt, dass die in der MHC‑Rinne sitzenden Antigene ausfallen, ohne die Zellen abzutöten. Die freigesetzten Peptide passieren dann einen kleinen Filter, der größere Partikel entfernt, und werden auf einer winzigen Säule in einem einzigen Röhrchen gebunden. Von dort gehen sie direkt in ein Massenspektrometer, das die Peptidsequenzen identifiziert. Tests an Melanomzellen zeigten, dass dieser milde Säureschritt nahezu alle Oberflächen‑MHC–Antigenkomplexe entfernt und dass die zurückgewonnenen Peptide in Länge und Sequenzmustern echten MHC‑gebundenen Antigenen entsprechen.
Mehr Daten aus weniger Material
MHC1-TIP wurde so konzipiert, dass es mit sehr wenigen Zellen arbeitet und dennoch viele identifizierbare Antigene liefert. In Kombination mit einem modernen Massenspektrometrie‑Modus namens data‑independent acquisition erkannte das Team Hunderte von Antigenen aus bereits 100.000 Zellen und Tausende aus wenigen Millionen Zellen — eine ähnliche Tiefe wie die herkömmliche Antikörpermethode, jedoch mit weniger Material und geringeren Kosten. Die Methode funktionierte außerdem bei patientenabgeleiteten Organoiden, also im Labor gezüchteten 3D‑Mini‑Tumoren, und bei winzigen ex vivo Tumorfragmenten, die kleiner als ein Kubikmillimeter sind. Wichtig ist, dass die Säurewäsche die Zellen weitgehend intakt lässt, sodass das verbleibende Material für umfassende Proteom‑Analysen aus derselben Probe genutzt werden kann. So lässt sich direkt vergleichen, wie viel eines bestimmten Proteins vorhanden ist und wie viel davon tatsächlich als Antigen präsentiert wird.
Verborgene Unterschiede innerhalb eines einzelnen Tumors
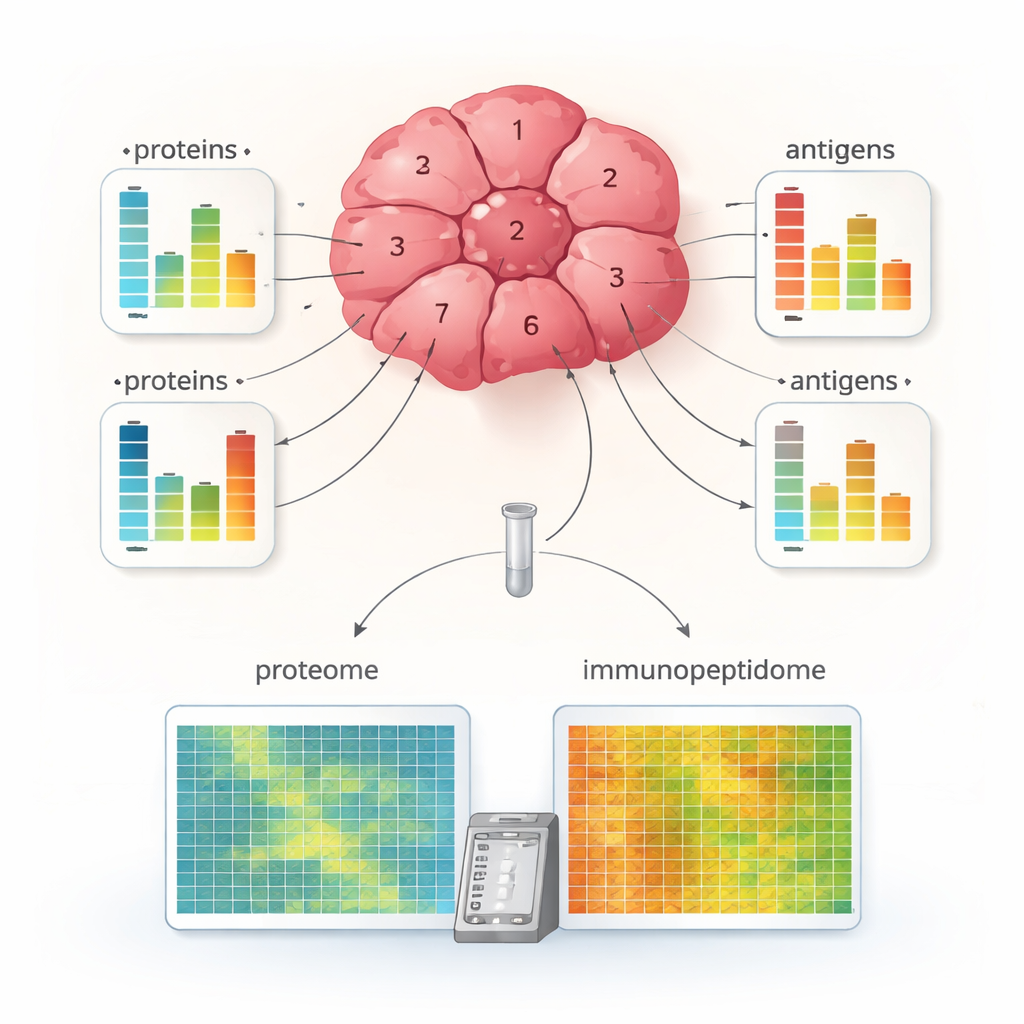
Die Anwendung von MHC1-TIP auf mehrere kleine Fragmente aus verschiedenen Regionen eines Nierenzellkarzinoms offenbarte eine auffällige interne Vielfalt. Einige Fragmente zeigten reichhaltige Antigenpräsentation, andere nur sehr wenige Antigene, obwohl ihr Gesamtproteingehalt ähnlich sein konnte. Bei vielen Proteinen stimmten Veränderungen in den Antigenmengen nicht mit Änderungen der Proteinhäufigkeit überein, was darauf hindeutet, dass Antigenverarbeitung und -beladung auf MHC‑Moleküle unabhängig von der Menge des Ausgangsproteins reguliert werden. Das Team kombinierte die Antigendaten außerdem mit Markern für Immunzellen und MHC‑Maschinerie und identifizierte Tumorregionen, die „immune‑hot“ waren, mit hoher Antigendarstellung und Anzeichen aktiver T‑Zellen, sowie „immune‑cold“ Regionen mit weniger Antigenen und geringerer erkennbarer Immunaktivität. Ein derartiges Detailniveau war bisher selten aus so kleinen Gewebestücken erreichbar.
Was das für die künftige Krebsversorgung bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Allein zu messen, welche Proteine ein Tumor herstellt, reicht nicht aus, um zu wissen, was das Immunsystem tatsächlich sehen kann. Die neue MHC1-TIP‑Methode bietet einen praktischen Weg, die tatsächliche Antigendarstellung aus sehr kleinen, klinisch realistischen Proben zu lesen und gleichzeitig die breitere Proteinkonstellation zu messen. Die Entdeckung, dass die Antigenpräsentation innerhalb eines Tumors stark variieren kann und nicht immer den Proteinmengen folgt, mahnt davor, Impf‑ oder T‑Zell‑Ziele allein auf Basis von Gen‑ oder Proteinexpression auszuwählen. Zukünftig könnten Ansätze wie MHC1-TIP helfen, effektivere, personalisierte Immuntherapien zu entwerfen, indem sie sich auf Antigene konzentrieren, die tatsächlich an der Oberfläche gezeigt und im gesamten Tumor konsistenter präsentiert werden.
Zitation: Bathini, M., Bocaniciu, D., Johnson, F.D. et al. MHC1-TIP enables single-tube multimodal immunopeptidome profiling and uncovers intratumoral heterogeneity in antigen presentation. Commun Biol 9, 296 (2026). https://doi.org/10.1038/s42003-026-09570-6
Schlüsselwörter: Antigenpräsentation, Immunopeptidomik, Krebsimmuntherapie, Tumorheterogenität, Massenspektrometrie