Clear Sky Science · de
Neu bewertete Spezifität von Gα-Protein–Antwort-Elementen in der GPCR-Signalübertragung
Warum winzige Schalter in Zellen für die Medizin wichtig sind
Viele der heute verwendeten Medikamente wirken, indem sie molekulare „Schalter“ an der Zelloberfläche umlegen, die als G‑Protein-gekoppelte Rezeptoren (GPCRs) bekannt sind. Diese Schalter leiten Nachrichten ins Zellinnere über Hilfsproteine weiter, die G‑Proteine genannt werden, und schalten schließlich Gene an oder aus. Jahrzehntelang verließen sich Forscher auf einfache, lichtproduzierende Tests, um zu sehen, welche G‑Proteine ein bestimmtes Medikament oder Rezeptor nutzt. Diese Studie stellt eine grundlegende, aber kritische Frage: Sagen diese Tests wirklich das aus, was wir ihnen zuschreiben — und kann man ihnen beim Design der nächsten Generation präziser Medikamente noch vertrauen?
Wie Wissenschaftler normalerweise GPCR-Signale ablesen
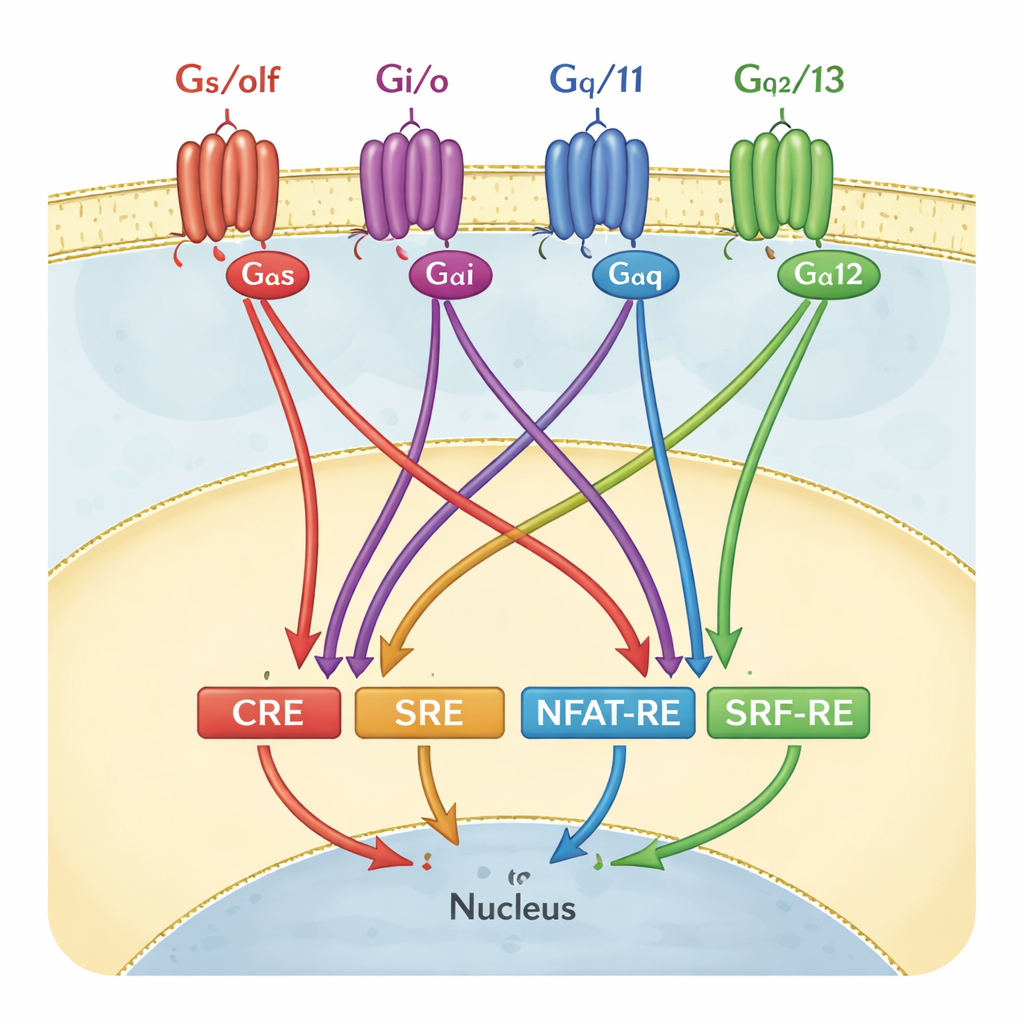
Um GPCR-Aktivität nachzuverfolgen, verwenden viele Labore Reporter-Genassays. Bei diesen Tests werden Zellen so gentechnisch verändert, dass sie aufleuchten, wenn ein bestimmtes Gen-Schaltelement oder „Response Element“ aktiviert wird. Vier solcher Schalter sind besonders gebräuchlich: CRE, SRE, NFAT‑RE und SRF‑RE. Jeder wurde lange als Stellvertreter für einen Zweig der G‑Protein-Signalübertragung betrachtet – etwa CRE für die Gαs/olf-Familie oder SRF‑RE für Gα12/13. In Lehrbüchern und Screening-Pipelines werden diese Paarungen oft fast wie Eins-zu-eins-Schaltpläne dargestellt: Schalte ein bestimmtes G‑Protein ein, und nur ein Reporter leuchtet auf.
Den alten Schaltplan auf die Probe stellen
Die Autoren haben dieses Bild systematisch infrage gestellt, indem sie humanen HEK293-Zellen bestimmte G‑Protein-Familien – oder sogar alle G‑Proteine – mittels Genom-Editing entzogen. Anschließend führten sie einzelne G‑Proteintypen nacheinander wieder ein. In diese Zellen brachten sie neun verschiedene GPCRs ein, die ausgewählt wurden, um Rezeptoren zu repräsentieren, die entweder sehr selektiv signalisieren oder über viele G‑Protein-Partner wirken. Indem sie maßen, wie stark jeder der vier Reporter über zahlreiche Wirkstoffkonzentrationen aufleuchtete, konnten sie feststellen, welche G‑Proteine für jedes Response Element wirklich erforderlich waren und welche indirekt mithelfen konnten.
Überlappende Wege statt sauberer Kanäle
Die Ergebnisse widerlegen das einfache Eins‑Rezeptor‑Eins‑Reporter-Modell. Während CRE weiterhin hauptsächlich von Gαs/olf‑Proteinen abhängig war – dem klassischen cAMP-steigernden Weg –, konnten auch andere G‑Protein-Familien die CRE-Aktivität merklich beeinflussen, allerdings nur, wenn Gαs/olf vorhanden war. Für die anderen drei Reporter, SRE, NFAT‑RE und SRF‑RE, erwies sich die Gαq/11-Familie als der wichtigste Treiber, obwohl SRE und SRF‑RE traditionell mit anderen G‑Protein-Zweigen verknüpft wurden. SRE und SRF‑RE zeigten sich dabei besonders ähnlich, was darauf hindeutet, dass sie gemeinsame nachgeschaltete Mechanismen anzapfen statt getrennte, isolierte Routen. In vielen Fällen lieferten zusätzliche G‑Proteine wie Gα12/13 und Gαi/o zusätzlichen Schub oder Hintergrundaktivität und unterstreichen ein Netz von Crosstalk statt separater Kanäle.
Warum das Netzwerk der Zelle unsere Messwerte verwischt
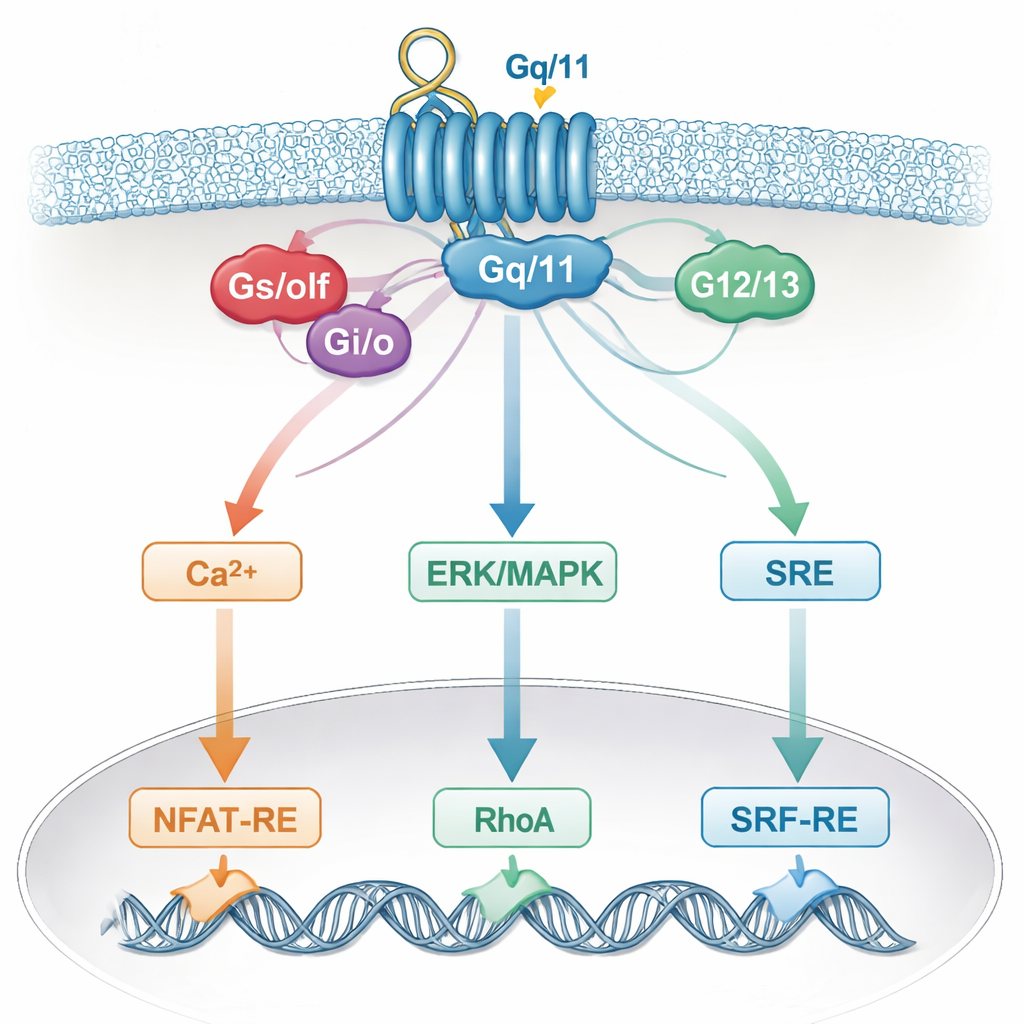
Diese verschwommene Spezifität spiegelt wahrscheinlich wider, wie echte Zellen Signale integrieren. Ein einzelner Rezeptor kann mehrere G‑Proteine aktivieren, die dann auf gemeinsame Botenstoffe wie Calcium, ERK/MAPK, RhoA oder cAMP konvergieren und auf gemeinsame Helfer wie Gβγ‑Untereinheiten wirken. Diese geteilten Wege fließen wiederum in dieselben Gen-Schalter im Zellkern ein. Infolgedessen „hört“ ein Reporter, von dem man annahm, er reagiere auf eine G‑Protein‑Familie, tatsächlich auf mehrere. Zelltypspezifische Faktoren und die genaue Zusammensetzung der vorhandenen Rezeptoren fügen noch mehr Komplexität hinzu, sodass aus einem System gezogene Schlussfolgerungen in einem anderen System nicht gelten müssen.
Was das für die Arzneimittelentwicklung bedeutet
Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass viele weit verbreitete, auf Aufleuchten basierende GPCR‑Tests weniger spezifisch sind, als ihre Etiketten vermuten lassen. Sie können weiterhin anzeigen, dass ein Rezeptor aktiv ist und grob, welche übergeordneten Wege beteiligt sind, liefern aber keinen verlässlichen Beweis dafür, dass eine bestimmte G‑Protein‑Familie — und nur diese eine Familie — beteiligt ist. Die Autoren argumentieren, dass Forscher und Arzneimittelentwickler diese Reporter als grobe Indikatoren behandeln und sie mit direkteren Methoden kombinieren sollten, die Protein‑Interaktionen in Echtzeit beobachten. So erhält man ein realistischeres Bild davon, wie potenzielle Medikamente die zelluläre Signalübertragung steuern, und kann irreführende Abkürzungen bei der Suche nach sichereren, gezielteren Therapien vermeiden.
Zitation: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Schlüsselwörter: GPCR-Signalübertragung, G‑Proteine, Reporterassays, Zelluläre Signalisierungsnetzwerke, Arzneimittelentwicklung