Clear Sky Science · de
HBP1 verstärkt die Progesteronrezeptor-Aktivität und IGFBP1-Expression und treibt die Endometrium-Decidualisation voran
Warum das für die Fruchtbarkeit wichtig ist
Wenn eine Schwangerschaft beginnt, kann sich der Embryo nur dann in der Gebärmutter einnisten, wenn die Gebärmutterschleimhaut eine entscheidende Umgestaltung durchlaufen hat, die als Decidualisation bezeichnet wird. Viele Fälle von Unfruchtbarkeit und wiederholtem Versagen bei Embryotransfers bleiben ungeklärt, und zunehmend deutet vieles darauf hin, dass das Problem eher in dieser Umgestaltung der Schleimhaut liegt als im Embryo selbst. Diese Studie deckt einen zuvor wenig beachteten molekularen "Schalter" auf — einen Transkriptionsfaktor namens HBP1 — der hilft, die Gebärmutterschleimhaut für die Implantation vorzubereiten und neue Ansätze zur Diagnose und Behandlung von Implantationsstörungen eröffnen könnte.
Ein verborgener Schalter in der Gebärmutterschleimhaut
Die innere Auskleidung der Gebärmutter, das Endometrium, verändert sich rhythmisch mit jedem Menstruationszyklus. Unter dem Einfluss von Östrogen wächst es, und unter Progesteron reift es zu einem empfänglichen Lager für einen Embryo heran. In dieser Arbeit konzentrierten sich die Forscher auf menschliche stromale Endometriumzellen, die Strukturzellen, die sich zur Zeit der Implantation in größere, stärker sekretorische Dezidualzellen verwandeln. Durch Auswertung vorhandener Genaktivitätsdaten und neue Experimente stellten sie fest, dass die HBP1-Spiegel stark ansteigen, sobald diese Stromazellen mit der Decidualisation beginnen, was darauf hindeutet, dass HBP1 Teil des eingebauten Zeitgebers ist, der die Gebärmutter vorbereitet.
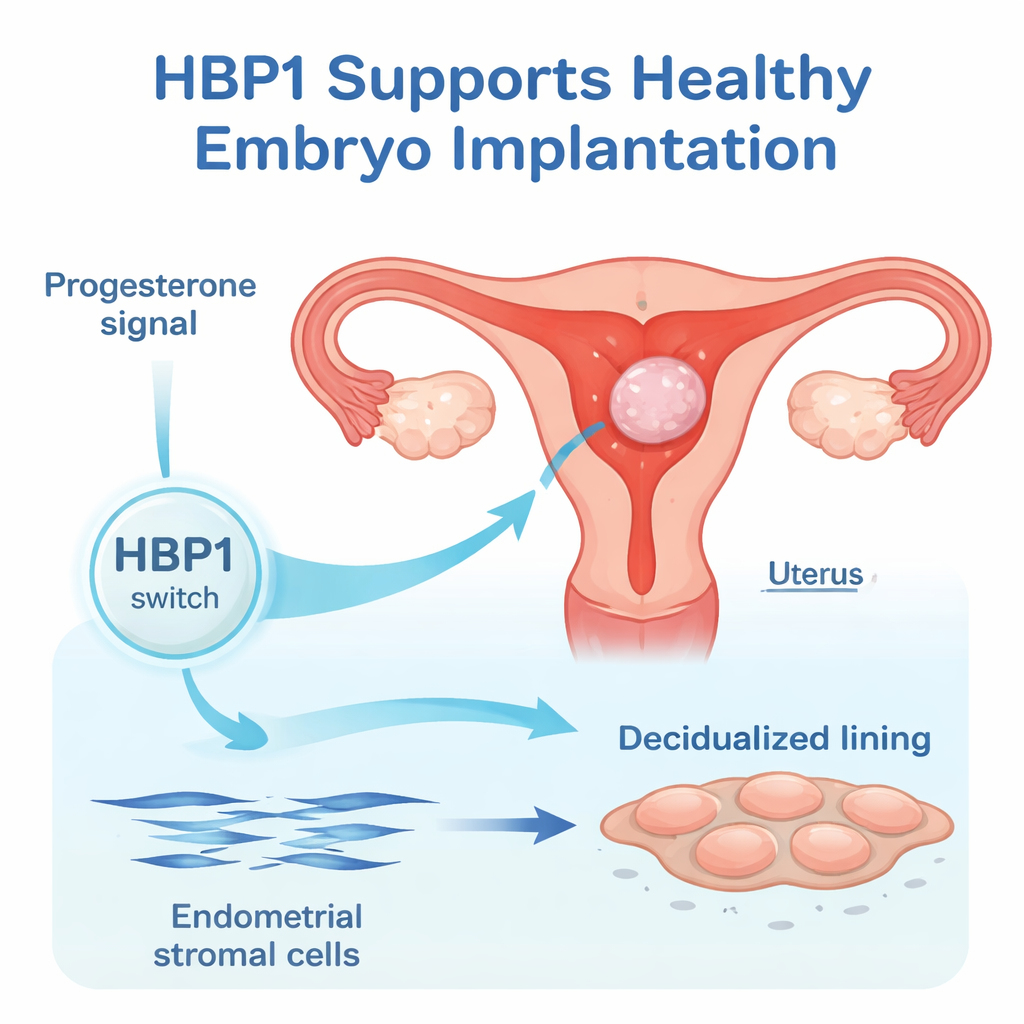
Helfen den Zellen, ihre Form zu ändern und das Wachstum zu bremsen
Um zu prüfen, ob HBP1 nur vorhanden ist oder wirklich benötigt wird, stellten die Forscher dessen Level in kultivierten menschlichen stromalen Endometriumzellen nach oben und unten ein. Bei Reduktion von HBP1 sanken klassische Decidualisationsmarker wie IGFBP1, FOXO1 und Prolactin sowohl auf RNA- als auch auf Proteinebene. Die Zellen durchliefen auch nicht den typischen Formwechsel von schlanken, spindelförmigen Zellen zu breiteren, polygonalen Zellen, sondern teilten sich weiter. Bei Erhöhung von HBP1 stiegen die IGFBP1-Spiegel und die Zellteilung verlangsamte sich. Zusammen zeigen diese Befunde, dass HBP1 den Zellen hilft, den Wachstumsmodus zu verlassen und in den spezialisierten dezidualen Zustand einzutreten, der eine frühe Schwangerschaft unterstützt.
Feinabstimmung hormoneller Signale innerhalb der Zelle
Progesteron und sein Rezeptor sind zentral für die Vorbereitung der Gebärmutter, aber nicht alle Gewebe sprechen gleich gut auf das Hormon an. Die Forscher entdeckten, dass die Progesteron-Signalgebung selbst die HBP1-Spiegel verstärkt und so eine positive Rückkopplungsschleife bildet. Auffällig war, dass eine Erniedrigung von HBP1 nicht die Menge des gebildeten Progesteronrezeptors veränderte, wohl aber die Aktivität wichtiger progesteron-ansprechbarer Gene abschwächte, darunter FKBP4, FKBP5, FOSL2 und den Koaktivator SRC1. Mit genomweiten Methoden zeigten sie, dass HBP1 in der Nähe vieler dieser Gene bindet und mit einer Zunahme einer spezifischen Histon-Markierung, H3K4me3, verbunden ist, die DNA als aktiv kennzeichnet. Im Kern schaltet HBP1 den Rezeptor also nicht an oder aus; es macht die Zielgene des Rezeptors leichter zugänglich.
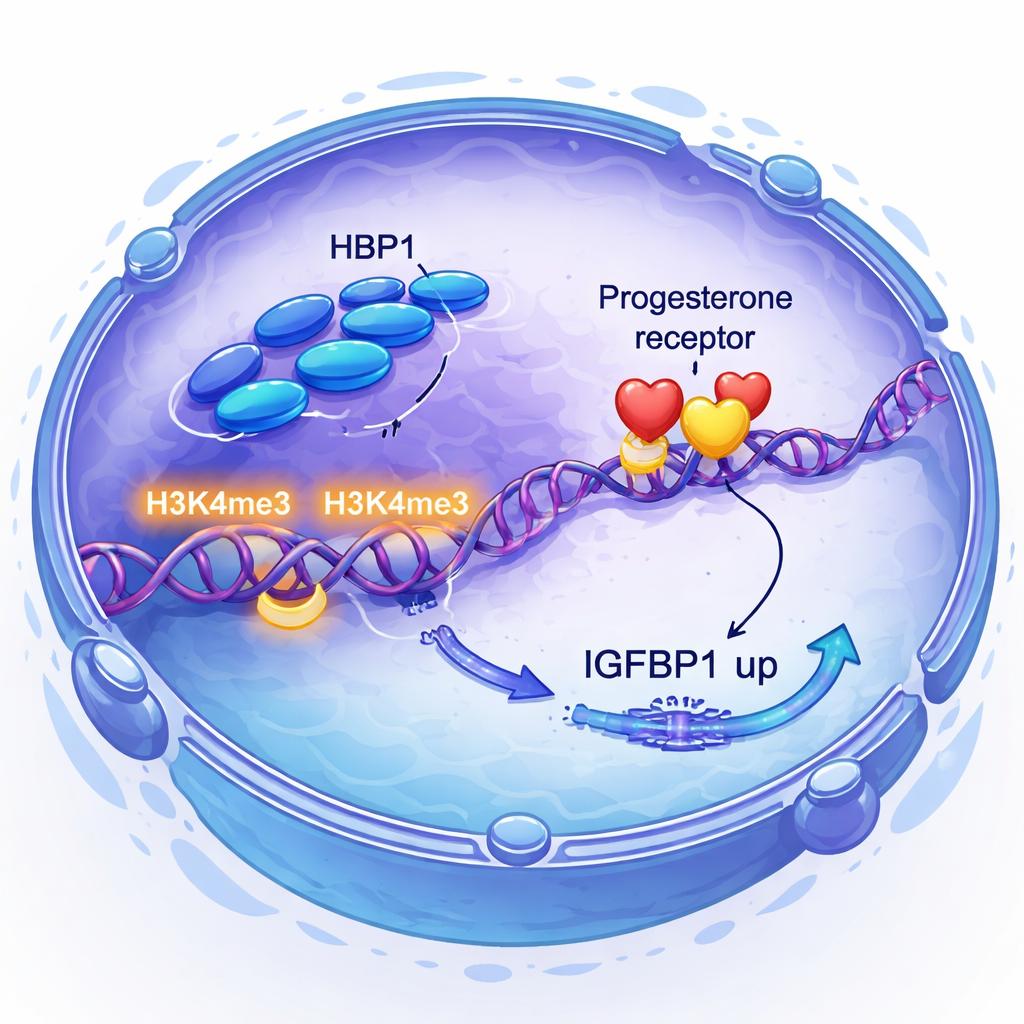
Direkte Kontrolle eines wichtigen Implantationssignals
Die Forscher fragten dann, wie HBP1 mit IGFBP1 verknüpft ist, einem Protein, das seit langem als Marker für gesunde Decidualisation dient und die Kommunikation zwischen Embryo und Gebärmutter beeinflusst. Durch die Kombination von RNA-Sequenzierung mit Chromatin-Immunpräzipitations-Sequenzierung zeigten sie, dass HBP1 direkt an der Promotorregion von IGFBP1 sitzt und dort H3K4me3 erhöht, wodurch die IGFBP1-Produktion gesteigert wird. Sie fanden außerdem, dass die Reduktion von HBP1 den PI3K–AKT-Weg aktivierte, ein wachstumsbezogenes Signal, das bei Überaktivität IGFBP1 unterdrückt. Die Blockade dieses Weges stellte die IGFBP1-Spiegel wieder her. Somit unterstützt HBP1 die Decidualisation auf zwei Wegen: durch direkte Aktivierung von IGFBP1 und durch Dämpfung eines Wachstumssignals, das sonst deziduale Gene zurückhalten würde.
Verknüpfung eines molekularen Defekts mit gescheiterter Implantation
Schließlich untersuchten die Forscher Endometriumsproben von Frauen mit wiederholtem Implantationsversagen und verglichen sie mit Geweben fruchtbarer Kontrollen während der mittelsekretorischen, implantationsbereiten Phase. Frauen mit wiederholtem Versagen wiesen deutlich niedrigere Spiegel von HBP1 und seinen nachgeschalteten Partnern IGFBP1, FKBP5 und FOSL2 auf, obwohl die Progesteronrezeptor-Spiegel zwischen den Gruppen ähnlich waren. Dieses Muster passt zur Idee einer "Progesteronresistenz" — das Hormon ist vorhanden, aber das Gewebe kann keine vollständige Antwort geben, weil wichtige Unterstützungsfaktoren wie HBP1 fehlen.
Was das für Patientinnen bedeutet
Einfach gesagt legt diese Studie nahe, dass HBP1 wie eine Hauptsteuerung auf dem Bedienfeld der Gebärmutterschleimhaut wirkt. Wenn es richtig hochgeschaltet ist, hilft es, Progesteron-Signale hörbar zu machen, ermutigt Zellen, die Teilung einzustellen und sich zu spezialisieren, und steigert die Produktion implantationfreundlicher Moleküle wie IGFBP1. Ist HBP1 zu niedrig, kann die Schleimhaut unter dem Mikroskop normal aussehen, aber funktionell schlecht sein, sodass Embryonen keinen Halt finden. Das Verständnis und die Messung von HBP1 und seinem Netzwerk könnte künftig Ärzten helfen, Frauen mit erhöhtem Risiko für Implantationsprobleme zu identifizieren und neue Therapien zu entwickeln, die die Empfänglichkeit der Gebärmutter wiederherstellen.
Zitation: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Schlüsselwörter: Endometrium-Decidualisation, Embryo-Implantation, Progesteron-Signalübertragung, Unfruchtbarkeit, HBP1