Clear Sky Science · de
Glioblastom-Stammzellen zeigen transcriptionell korrelierte räumliche Organisation
Warum Zellmuster bei Hirntumoren wichtig sind
Das Glioblastom gehört zu den aggressivsten Hirntumoren, und die Überlebenschancen haben sich seit Jahrzehnten kaum verbessert. Viele Labore untersuchen spezielle Tumorzellen, die sogenannten Glioblastom-Stammzellen, die den Tumor nach einer Behandlung wieder neu bilden können. In dieser Studie stellten die Forschenden eine auf den ersten Blick einfache, aber weitreichende Frage: Können die Anordnungen dieser Zellen in einer Petrischale — Muster, die man unter einem gewöhnlichen Mikroskop sieht — verraten, welche Gene in ihnen aktiv sind, und damit womöglich die Suche nach neuen Therapien beschleunigen?
Bilder, die mehr verraten als man denkt
Um diese Idee zu untersuchen, sammelte das Team etwa 17.000 Zeitraffer-Mikroskopbilder aus 15 patientenabgeleiteten Glioblastom-Stammzelllinien, die auf flachen Plastikplatten kultiviert wurden. Diese Aufnahmen, erstellt mit standardmäßiger Phasenkontrastmikroskopie, ähneln dem, was viele Biolabore täglich generieren. Auf den ersten Blick zeigen die Bilder einfach Zellen, die die Platte allmählich ausfüllen. Bei genauerer Betrachtung traten jedoch auffällige Unterschiede in der Organisation zutage: Manche bildeten lange, ausgerichtete Stränge, deren Zellen in ähnliche Richtungen zeigten, während andere rundere Klumpen mit zufälligeren Orientierungen oder überlappenden Schichten entwickelten. Diese visuellen Muster deuteten darauf hin, dass die inneren „Charaktere“ der Zellen sich in ihrem Gruppenverhalten niederschlagen könnten.

Texturen in biologische Bedeutung übersetzen
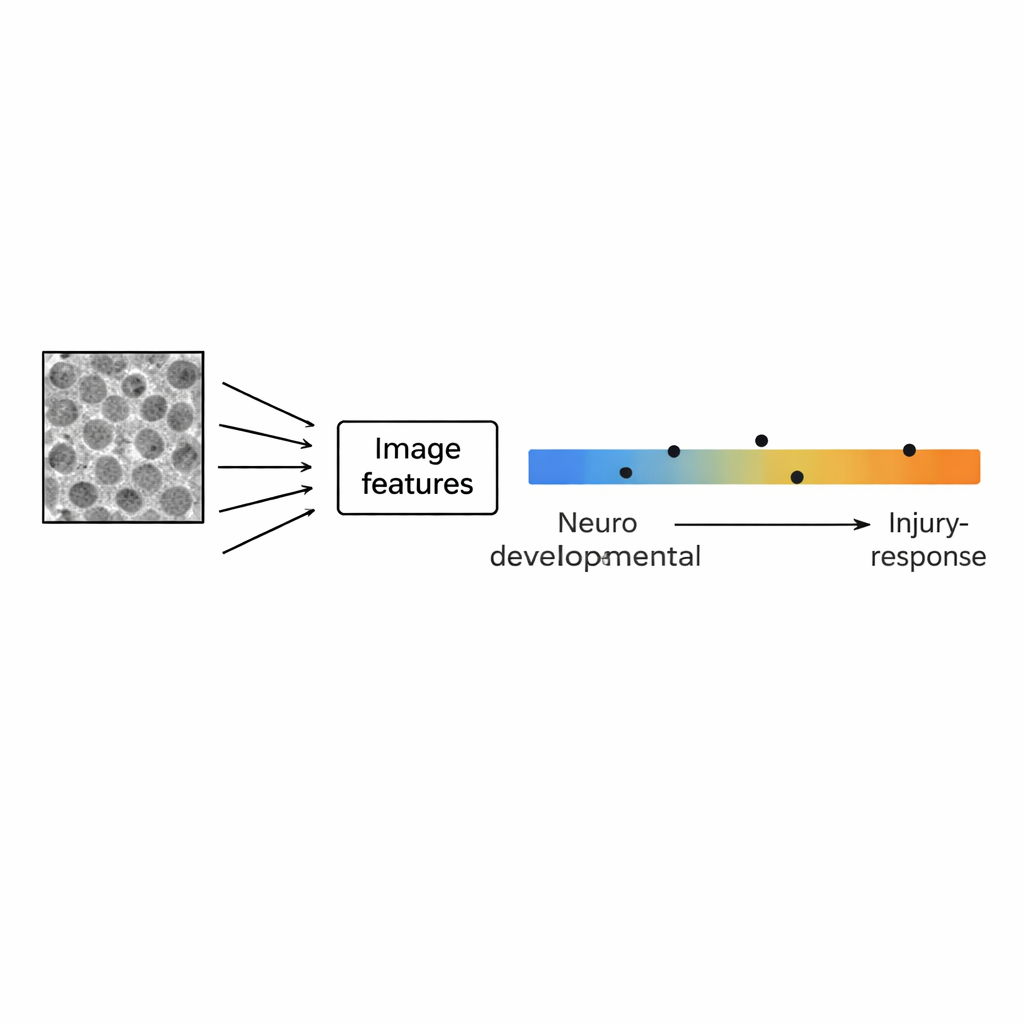
Anstatt einzelne Zellen in den Mittelpunkt zu stellen, behandelten die Forschenden jedes Bild als gesamtes Muster. Mit Open-Source-Software wandelten sie jedes Foto in 29 numerische Merkmale um, die Textur und Struktur beschreiben — etwa wie körnig das Bild in verschiedenen Skalen ist, wie oft benachbarte Pixel ähnlich erscheinen und wie stark der Kontrast in unterschiedlichen Richtungen ausfällt. Diese bildbasierten Fingerabdrücke verglichen sie anschließend mit Genaktivitätsprofilen derselben Zelllinien, wobei sie einen Satz von 111 Gen-Signaturen verwendeten, die Gehirnentwicklung, normale Zelltypen des Gehirns und entzündungsbezogene Zustände erfassen. Eine statistische Methode namens Hauptkomponentenanalyse zeigte, dass die Hauptachse der Variation in den Bildmustern einer bekannten biologischen Gradiente folgte: Am einen Ende exprimierten die Zellen Gene, die mit normaler Gehirnentwicklung (Neurone, Stammzellen, unterstützende Gliazellen) verbunden sind; am anderen Ende dominierten Gene, die mit Verletzung, Entzündung und einem aggressiveren, sogenannten mesenchymalen Verhalten verknüpft sind.
Muster, die beim Zellwachstum bestehen bleiben
Eine Schwierigkeit bei der Interpretation von Zellbildern ist, dass sich Kulturen stark verändern, wenn sie von spärlicher Besiedlung zu dichter Zellschicht heranwachsen. Die Autorinnen und Autoren gingen damit um, indem sie die Bilder in neun Dichtelevels einordneten und jedes Level separat neu analysierten. Bemerkenswerterweise hielt die Verbindung zwischen räumlichem Muster und Genaktivität über alle Wachstumsstadien hinweg: Ob die Platte kaum bepflanzt oder fast konfluente war, stammten Bilder von eher „entwicklungsähnlichen“ Linien tendenziell von glatteren, homogeneren Texturen, während solche von verletzungsreaktiven Linien unregelmäßigere, heterogenere Strukturen zeigten. Die spezifischen Bildmerkmale, die das Signal trugen, veränderten sich jedoch mit der Dichte — etwa waren Maße, die feine Körnigkeit erfassen, bei niedrigen Dichten am informativsten, während Merkmale, die Symmetrie und Homogenität beschreiben, mit zunehmender Zelldichte wichtiger wurden. Das deutet darauf hin, dass die zugrundeliegende Biologie einschränkt, wie sich Muster über die Zeit entwickeln, selbst wenn sich das physische Erscheinungsbild ändert.
Von Mikroskopaufnahmen zu molekularen Vorhersagen
Um zu testen, ob Bilder alleine die Position einer Zelllinie entlang der Entwicklungs–Verletzungs-Gradiente vorhersagen können, trainierte das Team einfache statistische Modelle, die nur die 29 Bildmerkmale als Eingabe und genexpressionsbasierte Scores als „Antwortschlüssel“ nutzten. Ein Modell, das automatisch die informativste Merkmalskombination auswählte, stellte die Gradiente für die ursprünglichen 15 Zelllinien genau nach und zeigte ermutigende Übereinstimmung in vier zusätzlichen Testlinien. Zu den nützlichsten Bildmerkmalen gehörten sowohl Texturbeschreiber als auch Maße zur Strukturgröße — ein Echo dessen, was in den Musteranalysen hervorkam. Wichtig ist, dass dieses Modell mit standardmäßigen, markierungsfreien Bildern funktionierte — keine fluoreszierenden Farbstoffe oder spezialisierten Mikroskope waren erforderlich — und damit einen praktischen Weg aufzeigt, routinemäßige Bildgebung in eine schnelle, kostengünstige Bestimmung des Zellzustands zu verwandeln.
Was das für die zukünftige Hirntumorforschung bedeutet
Für Nicht-Spezialisten ist die wichtigste Erkenntnis, dass das Aussehen und die Gemeinschaftsordnung von Krebszellen als Fenster in die Gene dienen kann, die sie nutzen. Bei Glioblastom-Stammzellen erfassen einfache Hellfeldbilder genügend Informationen, um Zellen zu unterscheiden, die dem normal entwickelnden Gehirn ähneln, von solchen, die in einen verletzungs- und entzündungsgetriebenen Zustand verschoben sind — ein Zustand, der oft mit aggressiverem Krankheitsverlauf verknüpft ist. Künftig könnte dieses bildbasierte „Fingerprinting“ Forschenden ermöglichen, Medikamente oder genetische Veränderungen schnell zu screenen, indem sie beobachten, wie diese Zellen entlang dieser Gradiente verschoben werden, ohne jedes Mal RNA sequenzieren zu müssen. Allgemeiner deutet die Arbeit darauf hin, dass die Architektur lebender Zellkulturen nicht nur visuell interessant ist, sondern biologisch bedeutsame Informationen kodiert, die sich mit den richtigen Werkzeugen entschlüsseln lassen.
Zitation: Ayyadhury, S., Sachamitr, P., Kushida, M.M. et al. Glioblastoma stem cells show transcriptionally correlated spatial organization. Commun Biol 9, 208 (2026). https://doi.org/10.1038/s42003-026-09566-2
Schlüsselwörter: Glioblastom-Stammzellen, Zellbildgebung, räumliche Organisation, Genexpression, Hochdurchsatz-Screening