Clear Sky Science · de
Differenzielle GABA-Dynamik in verschiedenen funktionalen Gehirnnetzwerken bei Autismus
Warum diese Hirnstudie wichtig ist
Viele Menschen im Autismus-Spektrum beschreiben die Welt als überfordernd, wobei Geräusche, Lichter und Emotionen zu intensiv oder seltsam gedämpft wirken. Forschende vermuten, dass ein Teil der Erklärung darin liegt, wie Gehirnzellen „Start“- und „Stopp“-Signale austarieren. Diese Studie betrachtet einen wichtigen „Stopp“-Botenstoff, GABA, und stellt eine praktische Frage: Wie reagiert das autistische Gehirn, wenn man dieses System mit einem Medikament anstößt? Die Antwort könnte helfen zu erklären, warum manche Medikamente bei Autismus unvorhersehbar wirken und warum die Dosierung so schwierig ist.
Signale, die die Hirnaktivität im Gleichgewicht halten
Unser Gehirn läuft auf einem ständigen Tauziehen zwischen Erregung (Neurone feuern) und Hemmung (Neurone dämpfen die Aktivität). GABA ist die wichtigste Chemikalie für diese Bremsfunktion. Bei Autismus deuten jahrelange Studien darauf hin, dass dieses Gleichgewicht gestört ist, besonders in Systemen, die Sinnesinformationen verarbeiten wie Sehen, Hören und Tastsinn. Die meisten bisherigen Arbeiten waren jedoch statisch: Man hat Chemie oder Struktur des Gehirns in Ruhe gemessen und autistische mit nicht-autistischen Personen verglichen. Es fehlte ein dynamischer Test, wie das GABA-System tatsächlich reagiert, wenn es durch eine Arznei herausgefordert wird — besonders über die großräumigen Netzwerke hinweg, die Wahrnehmung, Bewegung, Aufmerksamkeit und Emotion stützen.
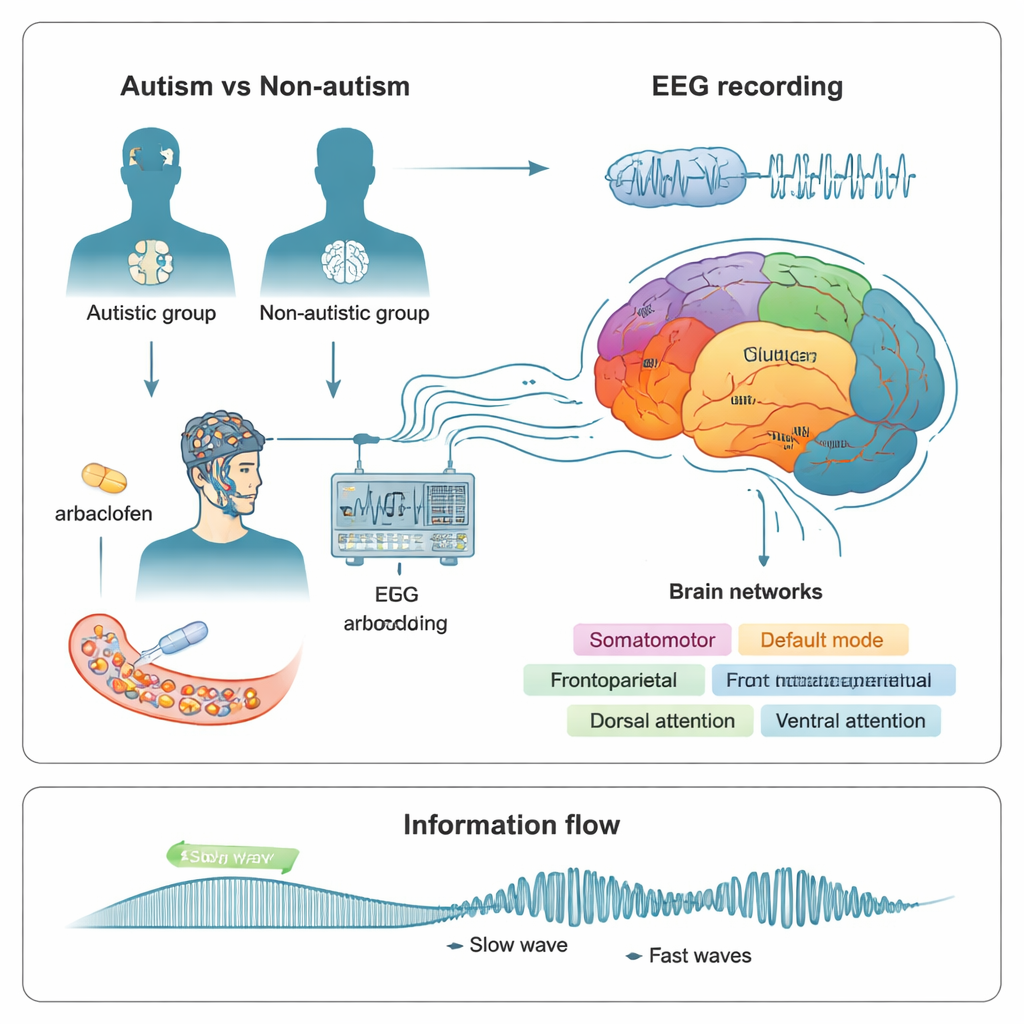
Den Hirnrhythmen zuhören
Um das zu untersuchen, zeichneten die Forschenden die Ruheaktivität des Gehirns mit EEG auf, das winzige elektrische Signale von der Kopfhaut misst. Sie untersuchten 24 nicht-autistische und 15 autistische Erwachsene über mehrere Besuche. Jedes Mal nahmen die Teilnehmenden entweder ein Placebo oder eine von zwei Dosen (15 mg oder 30 mg) Arbaclofen ein, ein Medikament, das einen bestimmten GABA-Rezeptortyp namens GABAB aktiviert. Etwa drei Stunden später, wenn das Medikament wirksam war, wurde EEG bei offenen und geschlossenen Augen aufgezeichnet und mit Computermodellen die Signale auf 400 Orte über der Großhirnrinde zurückgeführt. Diese Orte wurden dann in sieben große funktionale Netzwerke gruppiert, darunter visuelles, somatomotorisches (Bewegung und Tastsinn), limbisches (Emotion und Gedächtnis) und mehrere höherstufige Denk- und Aufmerksamkeitsnetzwerke.
Wie langsame und schnelle Hirnwellen miteinander sprechen
Statt nur die Stärke bestimmter Hirnwellen zu betrachten, konzentrierte sich das Team darauf, wie verschiedene Frequenzen miteinander interagieren. In gesunden Gehirnen helfen langsame Wellen, die große Bereiche überspannen, oft dabei, schnellere, lokalere Aktivitätsausbrüche zu koordinieren. Diese Interaktion, Phasen–Amplitude-Kopplung genannt, kann man sich vorstellen wie einen langsamen Rhythmus, der „Fenster“ öffnet und schließt, in denen schnelle Aktivität wahrscheinlicher ist. Die Autorinnen und Autoren maßen, wie stark langsame Rhythmen in Bereichen wie Theta und Alpha mit schnellerer Beta- und Gamma-Aktivität sowohl innerhalb als auch zwischen den sieben Netzwerken gekoppelt waren. Stärkere Kopplung kann manchmal nützlich sein, doch wenn sie zu eng oder unflexibel wird, kann das ein Hinweis auf ein Ungleichgewicht im Informationsfluss des Gehirns sein.
Autistische Gehirne zeigen im Ruhezustand stärkere Kopplung
Unter Placebo zeigten autistische Teilnehmende durchgehend erhöhte Kopplung zwischen Theta- und Beta-Rhythmen über die meisten Gehirnnetzwerke hinweg, wenn die Augen geschlossen waren, verglichen mit nicht-autistischen Freiwilligen. Besonders auffällig war das limbische System: Dort waren alle vier untersuchten Kopplungsmaße erhöht, was ungewöhnlich starke Verbindungen zwischen langsamen, großflächigen Rhythmen und schneller lokaler Aktivität in Regionen nahelegt, die an Emotion und Gedächtnis beteiligt sind. Das somatomotorische Netzwerk zeigte ebenfalls verstärkte Kopplung zwischen Theta- und Gamma-Rhythmen. Diese Muster stützen die Idee, dass das Erregungs–Hemmungs-Gleichgewicht auf der Ebene dynamischer Hirnrhythmen bei Autismus verändert ist, insbesondere in sensorischen und emotionalen Netzwerken.
Die Dosis zählt — und verschiedene Netzwerke verhalten sich unterschiedlich
Als die Forschenden Arbaclofen einführten, wurde das Bild komplexer und dosisabhängig. Bei autistischen Teilnehmenden verschob die höhere 30-mg-Dosis die erhöhte Theta–Beta-Kopplung in visuellen und somatomotorischen Netzwerken in Richtung des Bereichs der nicht-autistischen Gruppe, was auf ein normaleres Muster des sensorischen Informationsflusses hindeutet. Höherstufige Netzwerke, die Planung, selbstbezogenes Denken und Aufmerksamkeit unterstützen, veränderten sich hingegen kaum. Das limbische System reagierte anders: Eine niedrige 15-mg-Dosis brachte seine übermäßige Kopplung — sowohl innerhalb des Netzwerks als auch in seinen Verbindungen zu anderen Netzwerken — näher an die Kontrollwerte. Bei 30 mg traten viele dieser Auffälligkeiten jedoch wieder auf, und atypische limbische Verknüpfungen mit anderen Netzwerken, etwa dem somatomotorischen System, erschienen erneut. Anders gesagt: Einige emotionale Schaltkreise schienen bei niedriger Dosis am besten zu reagieren und konnten bei höheren Dosen überreizt werden.
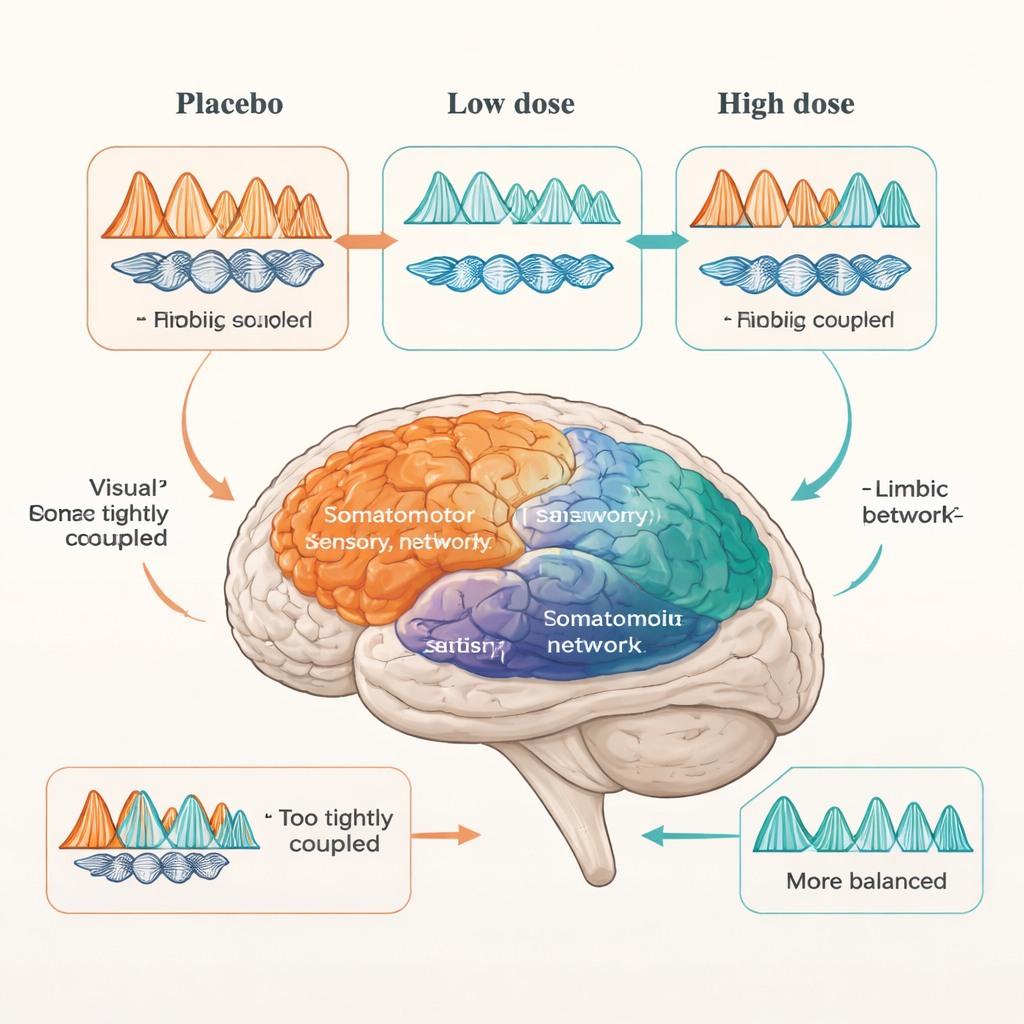
Was das für reale Behandlungen bedeutet
Wichtig für Laien ist die Erkenntnis, dass das autistische Gehirn nicht einfach und einheitlich auf GABA-wirkende Medikamente reagiert. Verschiedene Gehirnnetzwerke — sensorische, emotionale und höhere Denknetzwerke — zeigen unterschiedliche Sensibilitätsmuster, und einige Schaltkreise sind besonders dosisabhängig. Das erklärt, warum Medikamente, die Hemmung anpeilen, bei Autismus manchmal paradoxale oder gemischte Effekte haben können: Sie helfen in einem Bereich, stören aber einen anderen. Obwohl diese Studie nicht prüft, ob Arbaclofen Alltagssymptome verbessert, zeigt sie, dass gezielt gewählte Dosen bestimmte autistische Gehirnnetzwerke zu einem typischeren Aktivitätsgleichgewicht bewegen können. Künftige Arbeiten könnten solche hirnbasierten „Stresstests“ nutzen, um Behandlungen zu personalisieren und eine flexiblere, besser abgestimmte Kommunikation zwischen den Gehirnnetzwerken wiederherzustellen.
Zitation: Huang, Q., Chen, D., Pereira, A.C. et al. Differential GABA dynamics across brain functional networks in autism. Commun Biol 9, 283 (2026). https://doi.org/10.1038/s42003-026-09563-5
Schlüsselwörter: Autismus, GABA, Gehirnnetzwerke, EEG, Arbaclofen