Clear Sky Science · de
Darmmetabolit Indol-3-essigsäure verschlimmert neuropsychiatrischen Lupus über den AHR/STAT3-Weg in Mikroglia
Wie Darmkeime den Geist beeinflussen können
Menschen mit Lupus, einer Autoimmunerkrankung, entwickeln mitunter schwere Störungen von Denken, Stimmung und Gedächtnis — ein Zustand, der als neuropsychiatrischer Lupus bezeichnet wird. Diese hirnbedingten Symptome können stark beeinträchtigend sein, und Ärztinnen und Ärzte haben oft Schwierigkeiten zu erklären, warum sie auftreten oder wie man sie behandelt. Diese Studie untersucht einen unerwarteten Übeltäter: bestimmte Darmbakterien und die von ihnen produzierten Chemikalien, die vom Darm ins Gehirn gelangen und dort Entzündungen anfachen könnten.
Von Darmmikroben zu gestörtem Verhalten
Die Forschenden begannen mit der Frage, ob sich die Darmmikroben von Patientinnen und Patienten mit neuropsychiatrischem Lupus in ihren Effekten von denen von Lupus-Patienten ohne Hirnsymptome unterscheiden. Sie übertrugen Stuhlbakterien aus beiden Patientengruppen in gesunde Mäuse, deren eigene Darmmikrobiota zuvor entfernt worden war. Mäuse, die Mikroben von Patientinnen und Patienten mit neuropsychiatrischem Lupus erhielten, entwickelten vermehrt angstähnliches Verhalten, Anzeichen von Depression sowie Lern- und Gedächtnisprobleme im Vergleich zu Mäusen, die Mikroben von anderen Lupus-Patienten erhielten. In ihren Gehirnen fand sich eine verstärkte Aktivierung der Mikroglia — der Immunzellen des Gehirns — und höhere Spiegel entzündlicher Moleküle. Die schützende Barriere um das Gehirn, die sogenannte Blut-Hirn-Schranke, war in diesen Tieren ebenfalls durchlässiger, was darauf hindeutet, dass etwas in der transplantierten Mikrobiota diese wichtige Schranke schädigt.
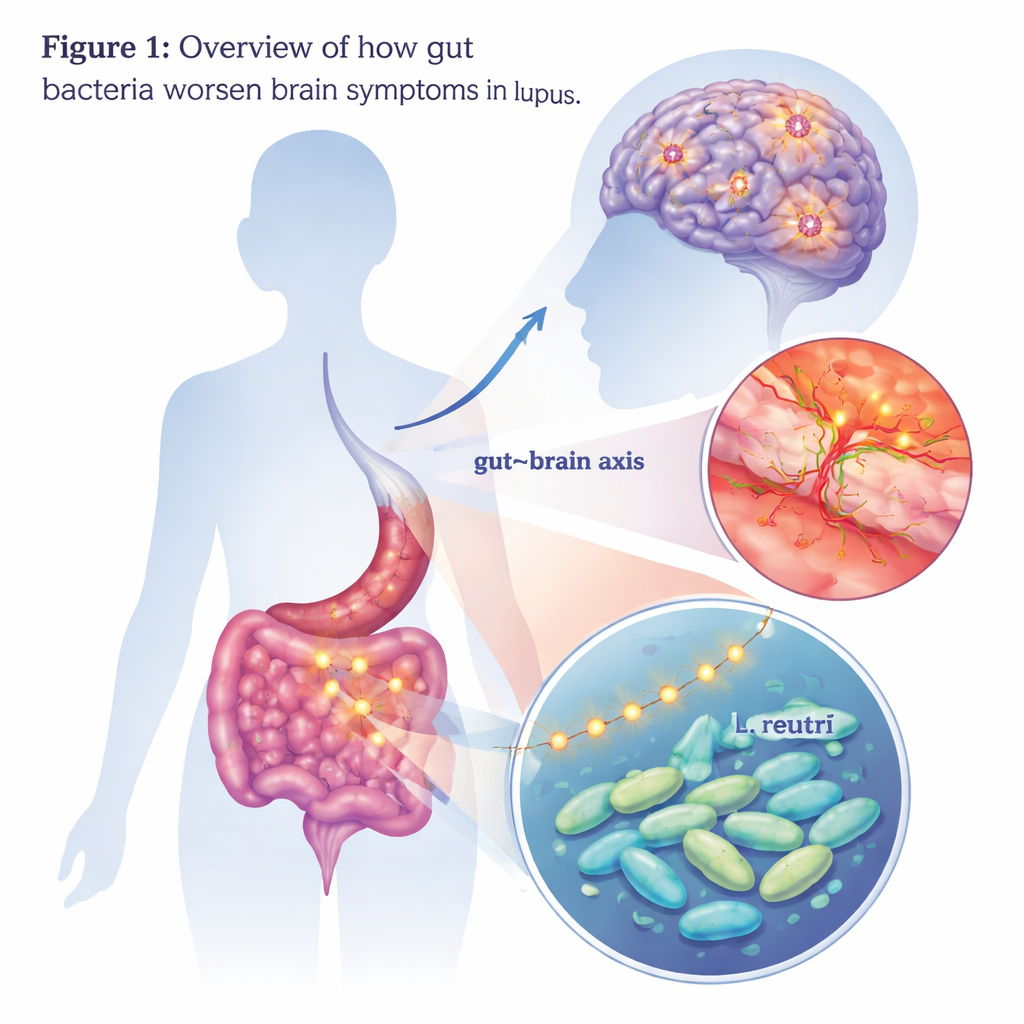
Blick auf ein einzelnes Bakterium
Um herauszufinden, welche Mikroben verantwortlich sein könnten, verglich das Team die Darmbakteriengemeinschaften von Patientinnen, Patienten und Mäusen. Eine Gruppe stach hervor: Lactobacillus, insbesondere eine Art namens Lactobacillus reuteri, war bei Patientinnen und Patienten mit neuropsychiatrischem Lupus und bei Mäusen mit Hirnveränderungen häufiger. Als die Wissenschaftlerinnen und Wissenschaftler L. reuteri allein an lupusanfällige Mäuse fütterten, entwickelten die Tiere stärker ausgeprägte angst- und depressionsähnliche Verhaltensweisen und schnitten bei Gedächtnistests schlechter ab. Ihre Gehirne zeigten mehr aktivierte Mikroglia, größeren Neuronenverlust und eine weitergehende Störung der Blut-Hirn-Schranke. Diese Befunde deuten darauf hin, dass dieses normalerweise als probiotisch betrachtete Bakterium im Kontext von Lupus eine schädlichere Rolle einnehmen kann.
Ein kleines Molekül mit großen Effekten
L. reuteri ist dafür bekannt, aus dem Nahrungsaminosäure Tryptophan ein Molekül namens Indol‑3‑essigsäure (IAA) zu produzieren. Mithilfe empfindlicher chemischer Analysen fand das Team höhere IAA-Spiegel im Stuhl von Patientinnen und Patienten mit neuropsychiatrischem Lupus als bei anderen Lupus-Patienten und bestätigte, dass L. reuteri-Kulturen deutlich mehr IAA herstellen als verbreitete Darmbakterien wie Escherichia coli. Bei Patientinnen und Patienten mit neuropsychiatrischem Lupus korrelierten IAA-Werte in der Gehirn-Rückenmarks-Flüssigkeit mit höheren Spiegeln entzündlicher Zytokine, was nahelegt, dass dieses Molekül das zentrale Nervensystem erreichen und dort Entzündungen auslösen kann. Bei lupusanfälligen Mäusen erhöhte die Fütterung mit L. reuteri die IAA-Spiegel im Darm, Blut und Gehirn. Die alleinige Gabe von IAA an diese Mäuse reproduzierte viele der gleichen Veränderungen: abnormes Verhalten, Aktivierung der Mikroglia, erhöhte Entzündungssignale sowie eine geschwächte Blut‑Hirn‑ und Darmbarriere.
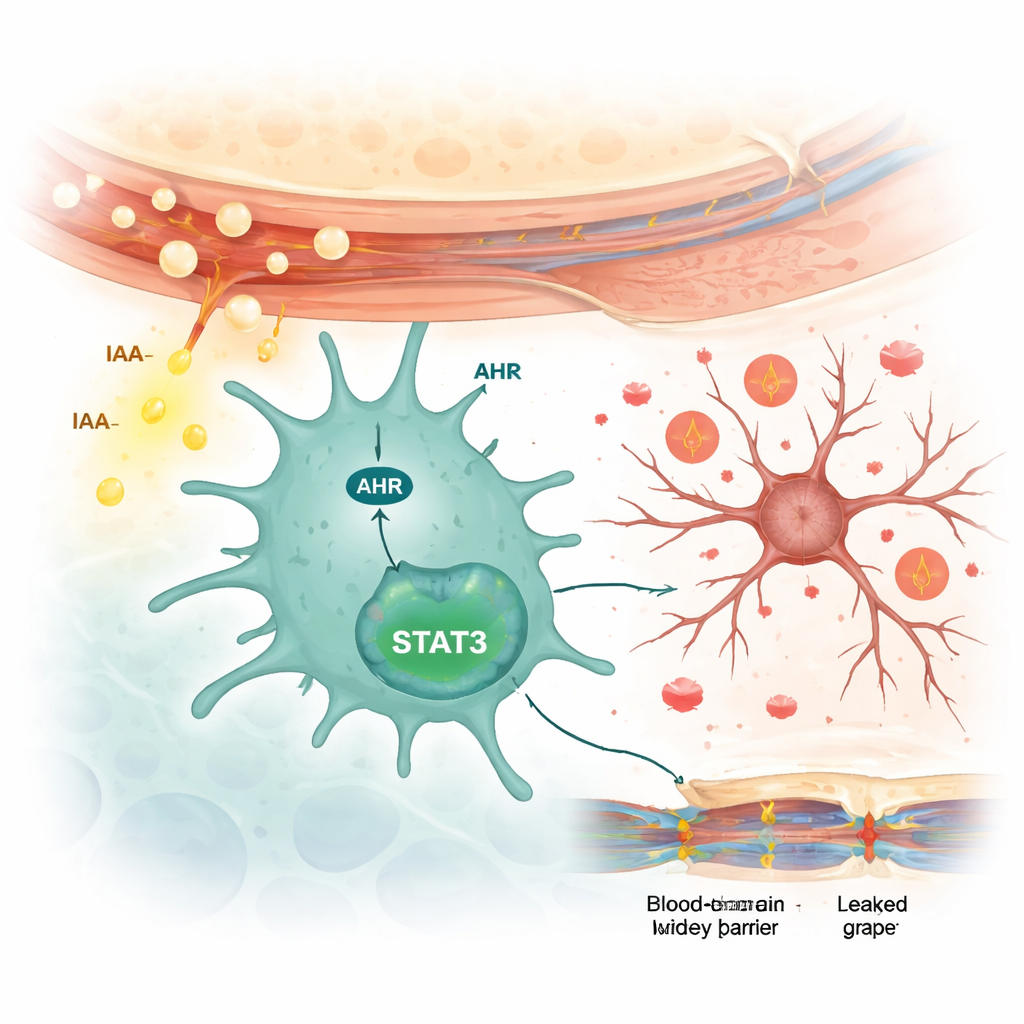
Wie die Immunzellen des Gehirns eingeschaltet werden
Die Forschenden untersuchten dann, wie IAA mit Gehirnzellen kommuniziert. Sie fanden heraus, dass IAA die Aktivität eines Sensorproteins namens aryl-Hydrokarbon-Rezeptor (AHR) speziell in Mikroglia erhöhte, nicht in Neuronen oder den sternförmigen Stützzellen, den Astrozyten. In kultivierten Mikroglia-Zellen steigerte IAA die AHR-Spiegel und schaltete ein nachgeschaltetes Signalprotein namens STAT3 ein, das wiederum die Produktion entzündlicher Zytokine vorantrieb. Das Blockieren von AHR mit einem Wirkstoff verhinderte die Aktivierung von STAT3 und verringerte die Freisetzung dieser entzündlichen Signale. Als lupusanfällige Mäuse mit dem AHR-blockierenden Wirkstoff behandelt wurden, besserten sich ihre angst- und depressionsähnlichen Verhaltensweisen, die Mikroglia-Aktivierung nahm ab, die Entzündungsmoleküle sanken und die Blut-Hirn-Schranke wurde weniger durchlässig.
Was das für Patientinnen und Patienten bedeutet
Insgesamt skizziert die Studie eine Ereigniskette, die den Darm mit dem Gehirn beim neuropsychiatrischen Lupus verbindet. Eine Überfülle an L. reuteri im Darm produziert zusätzliches IAA, das die Darmbarriere schwächt und ins Blut gelangt. IAA erreicht dann das Gehirn, wo es die AHR‑ und STAT3-Signalgebung in Mikroglia einschaltet, Entzündungen auslöst, Neuronen schädigt und die Blut-Hirn-Schranke lockert. Für Patientinnen und Patienten deuten diese Ergebnisse darauf hin, dass Maßnahmen zur Veränderung der Darmbakterien, die Verringerung schädlicher Metaboliten wie IAA oder das Blockieren des AHR/STAT3-Wegs in Mikroglia eines Tages dazu beitragen könnten, das Gehirn vor den verheerenden Folgen des neuropsychiatrischen Lupus zu schützen.
Zitation: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Schlüsselwörter: neuropsychiatrischer Lupus, Darmmikrobiota, Lactobacillus reuteri, Mikroglia-Entzündung, Blut-Hirn-Schranke