Clear Sky Science · de
HCN-Kanäle zeigen konvergente und divergente Physiologie in supragranulären pyramidalen Neuronen bei Primaten
Warum Unterschiede in der Gehirnverdrahtung wichtig sind
Menschen denken und verhalten sich eindeutig anders als Mäuse, doch die Neurowissenschaften arbeiten noch daran, was das für die einzelnen Nervenzellen bedeutet, aus denen unsere Gehirne bestehen. Diese Studie konzentriert sich auf eine spezielle Gruppe von Neuronen in den oberen Schichten des Kortex – Zellen, die helfen, verschiedene Hirnareale zu verknüpfen – und fragt, ob ein zentrales elektrisches Merkmal, das menschliche Neuronen von Nagetieren unterscheidet, einzigartig menschlich ist oder stattdessen bei Primaten geteilt wird. Die Antwort trägt dazu bei zu erklären, wie Primatenhirne langsame rhythmische Aktivität verarbeiten, die Wahrnehmung, Gedächtnis und Aufmerksamkeit unterstützt.
Spezielle Kanäle, die neuronale Rhythmen formen
Neurone kommunizieren über winzige elektrische Signale. Diese Signale werden stark durch Poren in der Zellmembran, sogenannte Ionenkanäle, geprägt. Die Autoren konzentrieren sich auf HCN-Kanäle, die leise öffnen, wenn die Spannung einer Zelle negativer wird, und sie dann sanft zurück in Richtung Ruhepotenzial ziehen. Dieser selbstkorrigierende Strom lässt Neurone besonders gut auf Eingänge im langsamen Delta- und Theta-Bereich (etwa 1–8 Zyklen pro Sekunde) reagieren – Frequenzen, die in Gehirnwellen bei Schlaf, Navigation und fokussierter Aufmerksamkeit häufig vorkommen. Frühere Arbeiten zeigten, dass pyramidale Neurone der oberen Schichten beim Menschen besonders ausgeprägte HCN-bezogene Eigenschaften im Vergleich zu Mäusen besitzen, was die Möglichkeit aufwarf, dass diese Kanäle Teil dessen sind, was den menschlichen Kortex besonders macht.
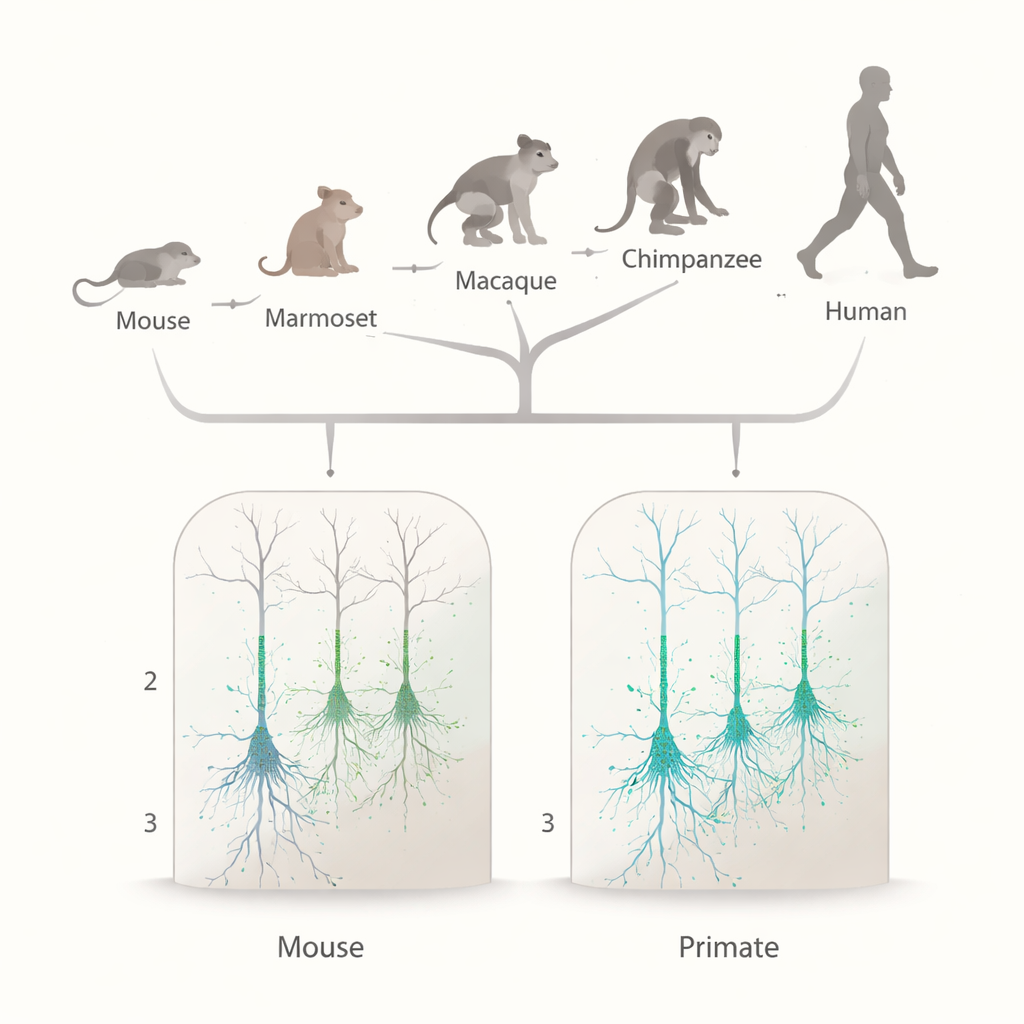
Primatenhirne nach dem gleichen elektrischen Signatur durchsuchen
Um herauszufinden, ob diese HCN-Anreicherung einzigartig menschlich oder bei Primaten allgemein ist, verglich das Team Genaktivität und elektrisches Verhalten in Neuronen mehrerer Arten. Mithilfe von Einzelkern-RNA-Sequenzierungsdaten maßen sie zunächst die Expression des Gens HCN1 und eines Hilfsproteins namens TRIP8b (kodiert durch PEX5L) in exzitatorischen Neuronen der oberen kortikalen Schichten von Neuweltaffen, Altweltaffen, Menschenaffen und Menschen und stellten diese Daten Mäusen gegenüber. In allen Primatenarten wurden HCN1 und TRIP8b in exzitatorischen Neuronen der oberen Schichten weit verbreitet exprimiert, auf Niveaus, die mit einer bereits als stark HCN-abhängig bekannten tiefen Neuronenklasse vergleichbar sind. Bei Mäusen hingegen war HCN1 in diesen oberen Schichten deutlich seltener. Das deutet auf ein breites Primatenmuster hin und nicht auf ein einmaliges menschliches Merkmal.
Lebende Neurone aus Affen testen
Die Autoren gewannen anschließend lebende Hirnschnitte von zwei Makakenarten und Baumhörnchenaffen und zeichneten Messungen von mehr als 500 pyramidalen Neuronen der oberen Schichten im Temporal- und Motorkortex auf. Sie setzten clevere Stromreize ein, um zu prüfen, ob die Zellen eine „Membranresonanz“ zeigten – eine Präferenz für Oszillationen in einem bestimmten Frequenzband –, was ein Kennzeichen aktiver HCN-Leitfähigkeit ist. Viele Neurone in allen drei Affenarten zeigten Resonanz oberhalb von 2 Hz, besonders im Motorkortex, was auf eine starke HCN-Beteiligung hinweist. Weitere Messgrößen, wie ein typisches „Sag“ der Spannung bei negativer Strominjektion und ein schnellerer Abfall bei Tiefpassfiltern, stützten ebenfalls die weit verbreitete HCN-Aktivität. Im Temporalkortex des Schweinschwanzmakaken wurden HCN-bezogene Effekte in tiefer gelegenen Neuronen der oberen Schichten stärker, was frühere Befunde im menschlichen mittleren Temporalgyrus widerspiegelt.
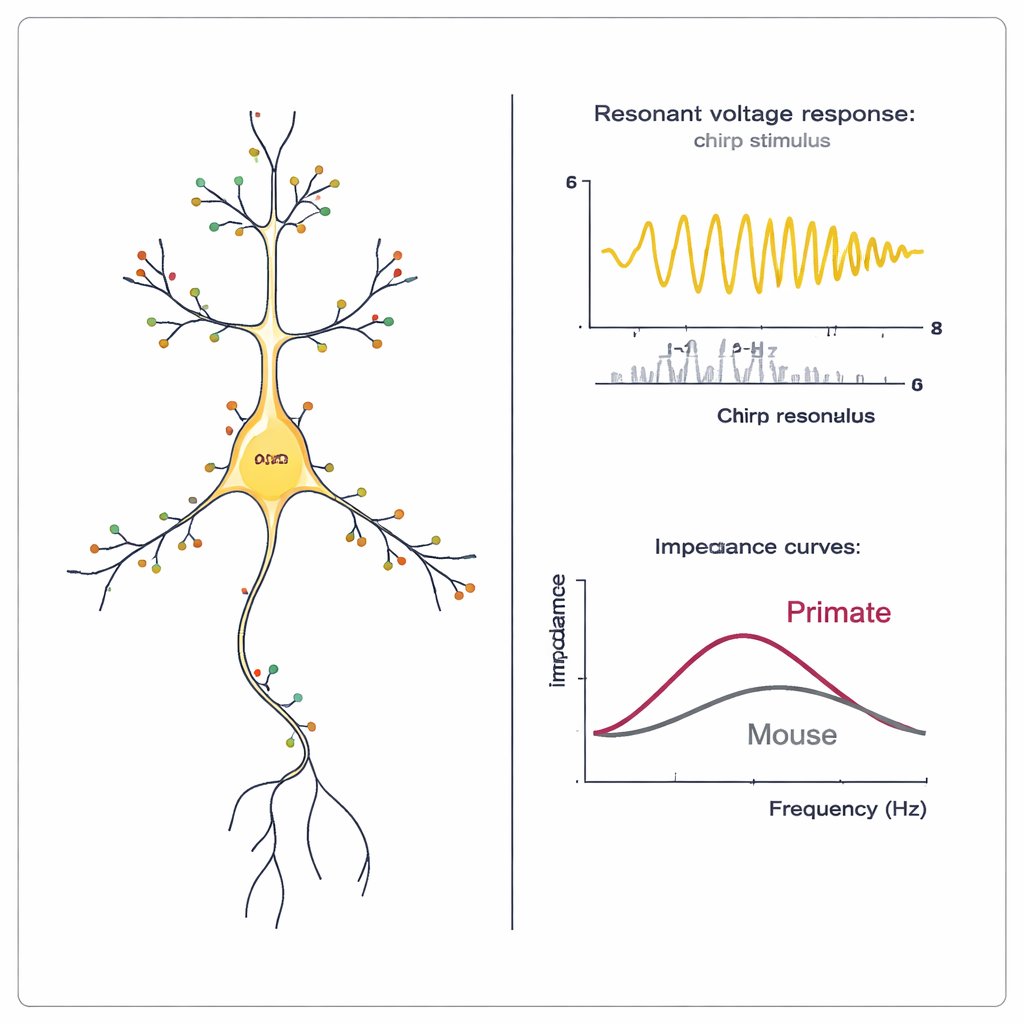
Kanäle blockieren und Menschen mit Makaken vergleichen
Um zu bestätigen, dass HCN-Kanäle diese Effekte tatsächlich verursachen, wendeten die Forschenden einen spezifischen Blocker, ZD7288, an Schnitten des makakenen Temporalkortex an. Wenn HCN-Kanäle blockiert waren, wurden die Neurone elektrischer widerstandsfähiger, ihr Ruhepotenzial verschob sich negativer, und sowohl Sag als auch Resonanz verschwanden im Wesentlichen. Das Ausmaß der Veränderung bei Resonanz und Sag korrelierte mit der Änderung des Eingangswiderstands, was darauf hindeutet, dass Neurone mit den stärksten HCN-Signaturen auch die größte HCN-Leitfähigkeit hatten. Schließlich konnten die Forschenden durch die Kombination elektrischer Aufzeichnungen und Genexpression derselben Zellen mit der Methode Patch-seq makaken- und menschliche Neurone anhand ihrer Transkriptomtypen abgleichen. In einem wichtigen oberen Schichttyp (L2/3 IT_1) nahmen HCN-bezogene Eigenschaften – einschließlich Resonanz und Sag – in beiden Arten mit zunehmender Tiefe von der Gehirnoberfläche zu und korrelierten mit der HCN1-Expression. Interessanterweise zeigten Makakenneurone innerhalb dieses Zelltyps sogar stärkere HCN-abhängige Eigenschaften als ihre menschlichen Gegenstücke, während ein zweiter oberer Schichttyp (L2/3 IT_3) nur milde Unterschiede zwischen den Arten aufwies.
Was das für die Informationsverarbeitung in Primatenhirnen bedeutet
Insgesamt zeigt die Studie, dass eine verstärkte Expression und Funktion von HCN-Kanälen in pyramidalen Neuronen der oberen Schichten ein konserviertes Merkmal bei Primaten ist und keine ausschließlich menschliche Anpassung. Verglichen mit Nagetieren haben Primaten dickere obere kortikale Schichten und Neurone mit längeren, stärker verzweigten Dendriten. Starke HCN-Leitfähigkeit hilft diesen großen Zellen, Eingänge gleichmäßiger über ihre dendritischen Bäume zu integrieren und sie auf langsame Delta-/Theta-Rhythmen abzustimmen, die die kortikale Aktivität von Primaten dominieren. Subtile Variationen zwischen Zelltypen, Hirnarealen und Arten – etwa die besonders starken HCN-Effekte in einem Makakenneurontyp – könnten zusätzliche Flexibilität für die Feinabstimmung kognitiver Funktionen liefern. Aber die Grundbotschaft ist klar: Die elektrischen Spezialisierungen, die einst als Unterscheidungsmerkmal menschlicher kortikaler Neurone galten, erscheinen stattdessen als eine gemeinsame Strategie der Primaten zur Handhabung komplexer, rhythmischer Informationsflüsse.
Zitation: Radaelli, C., Schmitz, M., Liu, XP. et al. HCN channels reveal conserved and divergent physiology in supragranular pyramidal neurons in primate species. Commun Biol 9, 279 (2026). https://doi.org/10.1038/s42003-026-09558-2
Schlüsselwörter: HCN-Kanäle, Primatenkortex, pyramidale Neuronen, Delta-Theta-Rhythmen, Patch-seq