Clear Sky Science · de
Radionuklid‑aktivierte dynamische Therapie induziert komplementäre immunogene Nekroptose- und Apoptose-Wege des Krebszelltods
Krebs’ Tricks gegen sich selbst wenden
Krebs ist dafür bekannt, selbst unseren besten Behandlungen zu entkommen, insbesondere bei aggressiven Brusttumoren, die sich im Körper ausbreiten. Diese Studie untersucht einen erfinderischen Ansatz, die radionuklid‑aktivierte dynamische Therapie (RaST), die bildgebende Tracer und lichtaktivierbare Nanopartikel nutzt, um Krebszellen so zu töten, dass gleichzeitig das Immunsystem geweckt wird. Für Leser ist diese Arbeit wichtig, weil sie andeutet, wie vorhandene Bildgebungswerkzeuge und intelligente Materialien umgenutzt werden könnten, um eine länger anhaltende, immungetriebene Krebsbekämpfung statt nur vorübergehender Tumorverkleinerung zu erreichen.
Eine neue Art, Tumoren von innen zu beleuchten
Traditionelle lichtbasierte Krebstherapien wirken nur dort, wo ein äußerer Strahl hingelangt, etwa bei Haut- oder Oberflächentumoren. RaST umgeht diese Einschränkung, indem es ein radioaktives Zuckerderivat verwendet, ähnlich dem Tracer, der bereits in PET-Scans eingesetzt wird und sich bevorzugt in schnell wachsenden Krebszellen anreichert. Während dieser Tracer durch den Tumor wandert, emittiert er ein schwaches blaues Leuchten, bekannt als Cherenkov‑Strahlung. Die Forschenden entwickelten winzige Titandioxid‑Nanopartikel, die mit einem tumortargetierenden Protein beschichtet sind, sodass auch sie den Tumor ansteuern. Treffen Tracer und Nanopartikel aufeinander, schaltet das interne Licht die Partikel an, die daraufhin Schübe reaktiver Sauerstoffspezies erzeugen — hochreaktive Moleküle, die Krebszellen von innen schädigen.
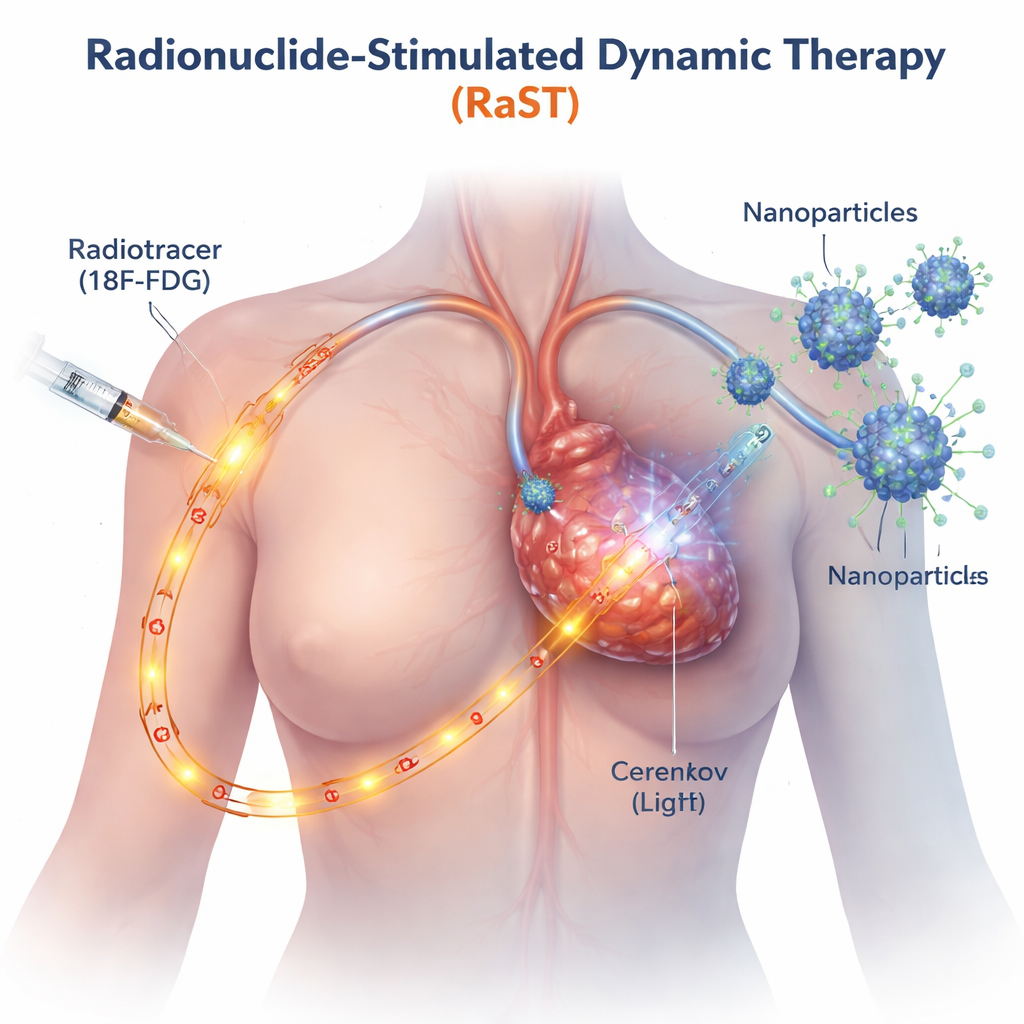
Auslösen von zwei unterschiedlichen Wegen zum Zelltod
Das Team wollte nicht nur wissen, ob RaST Krebszellen tötete, sondern wie. An mehreren aggressiven Brustkrebszelllinien im Labor stellten sie fest, dass sorgfältig abgestimmte Dosen des radioaktiven Tracers und der Nanopartikel zusammen wirkten, um Tumorzellen wirksamer zu schädigen als jede Komponente allein — selbst bei Typen, die gegen Standardchemotherapie resistent sind. Detaillierte Bildgebung und Proteinmessungen zeigten, dass RaST gleichzeitig zwei regulierte Programme des Zelltods aktivierte. Das eine war die Apoptose, oft als zellulärer „Suizid“ beschrieben, bei dem sich Zellen geordnet selbst demontieren. Das andere war Nekroptose, eine gewaltsamere Form des Zelltods, bei der Zellen anschwellen, aufreißen und molekulare Notrufe in ihre Umgebung freisetzen. Diese Signale, bekannt als damage‑associated molecular patterns und entzündungsfördernde Zytokine, können als Signalfackeln dienen, die Immunzellen anziehen und aktivieren.
Das Immunsystem für langfristige Kontrolle mobilisieren
Um zu prüfen, ob diese entzündliche Art der Tumortötung in lebenden Organismen relevant ist, testeten die Forschenden RaST in Mausmodellen des Brustkrebses. In Mäusen ohne wichtige Immunfunktionen bewirkte RaST wenig gegen Tumorwachstum oder Lungenstreuung, obwohl lokal reichlich Zelltod entstand. In immunkompetenten Mäusen hingegen führte dieselbe Behandlung zu teilweisen und vollständigen Tumorantworten und verhinderte Metastasen in die Lunge. Tumoren, die RaST ausgesetzt waren, waren stark mit Immunzellen durchsetzt — insbesondere myeloide Zellen wie Makrophagen und dendritische Zellen —, die spezialisiert darauf sind, totes Material aufzunehmen und Tumorfragmente T‑Zellen zu präsentieren. Bluttests zeigten über die Zeit Wellen von immunstimulierenden und immunregulierenden Signalen, was darauf hindeutet, dass RaST zunächst eine Angriffswelle auf den Tumor auslöst und später zu einem ausgewogeneren Zustand übergeht, während Tumoren schrumpfen oder stabil bleiben.
Versteckte Überreste aufspüren und Rückfällen vorbeugen
Selbst in Mäusen, bei denen Tumoren scheinbar vollständig durch RaST geheilt wurden, enthüllte ein hochempfindlicher Farbstoff später winzige Nester residueller Krebszellen in Lymphknoten. Erstaunlicherweise entwickelten diese Tiere dennoch über viele Monate weder neue Tumoren noch Fernmetastasen. Chemische Analysen zeigten, dass die Titandioxid‑Nanopartikel, die ursprünglich in Knochen und Leber reichlich vorhanden waren, sich nach und nach in Milz und Lymphknoten umverteilten — genau die Orte, an denen Immunzellen patrouillieren. Diese langsame Migration hält wahrscheinlich eine lokale Quelle reaktiver Sauerstoffspezies verfügbar für Immunzellen, was ihnen hilft, diese verborgenen Krebsreste zu erkennen und zu kontrollieren, bevor sie erneut wachsen oder streuen können.
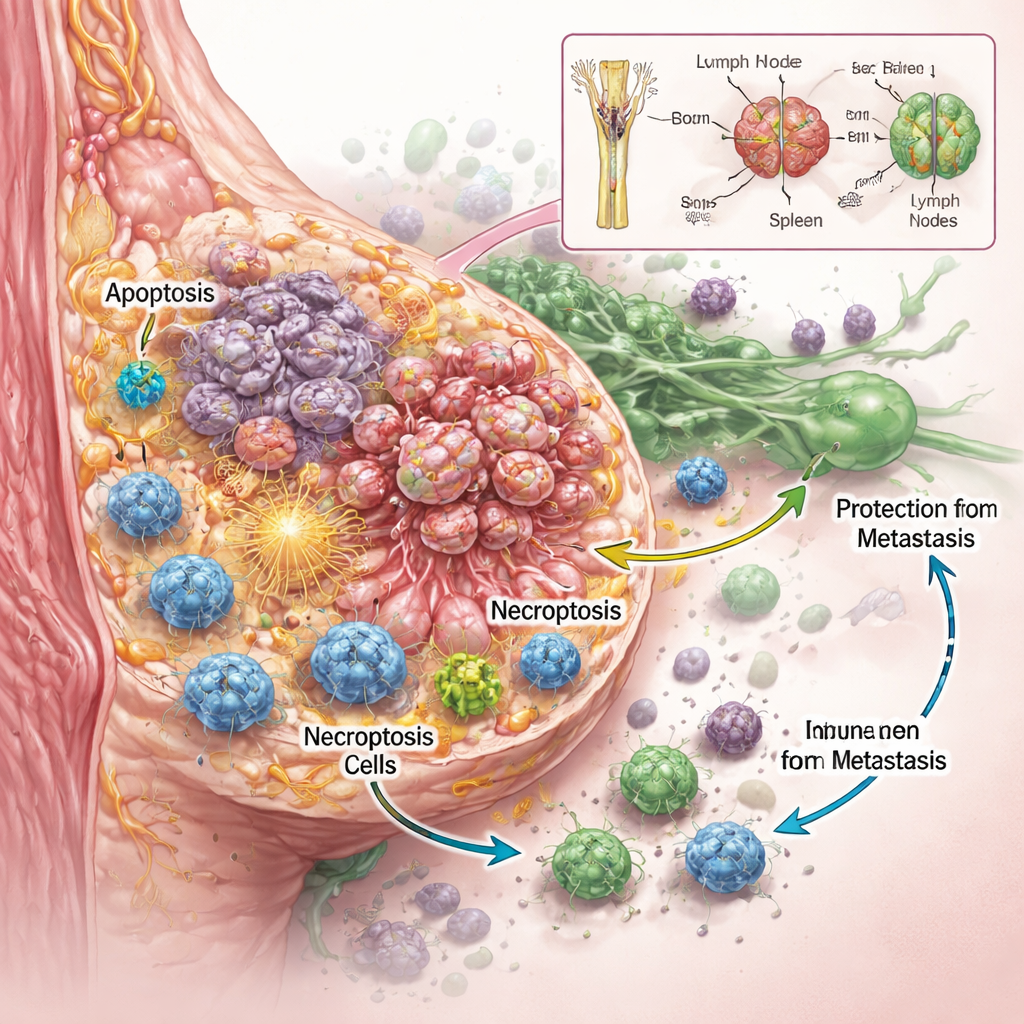
Was das für die künftige Krebsbehandlung bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass RaST mehr ist als nur eine weitere Methode, Tumorzellen zu vergiften. Durch die Kombination radioaktiver Tracer, lichtreaktiver Nanopartikel und der körpereigenen Abwehr zwingt sie Krebszellen in zwei Formen des programmierten Zelltods, die das Immunsystem lautstark alarmieren. In immunintakten Tieren führt dies zu dauerhafter Kontrolle aggressiver Brusttumoren und blockiert Metastasen, selbst wenn einige Krebszellen in Lymphknoten verbleiben. Zwar ist noch viel zu tun, bevor dieser Ansatz breit am Menschen getestet werden kann, doch die Studie weist in Richtung künftiger Behandlungen, die nicht allein auf Tumorschrumpfung abzielen, sondern die Beziehung zwischen Krebs, Zelltod und Immunität so umgestalten, dass der Körper langfristig zur Kontrolle der Krankheit beitragen kann.
Zitation: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Schlüsselwörter: Brustkrebs, Nanopartikel, Immuntherapie, Radionuklidtherapie, Nekroptose