Clear Sky Science · de
Glykophagie ist ein uralter bilateraler Weg, der metabolische Anpassung durch strukturelle Evolution von STBD1 unterstützt
Wie Austern versteckte Energietricks aufdecken
Tiere überstehen harte Zeiten, indem sie auf gespeicherte Energiereserven zugreifen, doch nicht alle verlassen sich auf dieselbe Art von „Batterie“. Diese Studie betrachtet Pazifische Austern und zeigt, dass Austern, im Gegensatz zu vielen anderen Tieren, die auf Fett setzen, stark von gespeichertem Zucker in Form von Glykogen abhängig sind. Die Arbeit enthüllt einen wenig bekannten zellulären Recyclingweg — die Glykophagie — der Austern erlaubt, ihre Zuckervorräte schnell zu entleeren und wieder aufzufüllen, und zeichnet nach, wie dieses System im Tierreich entstanden ist.
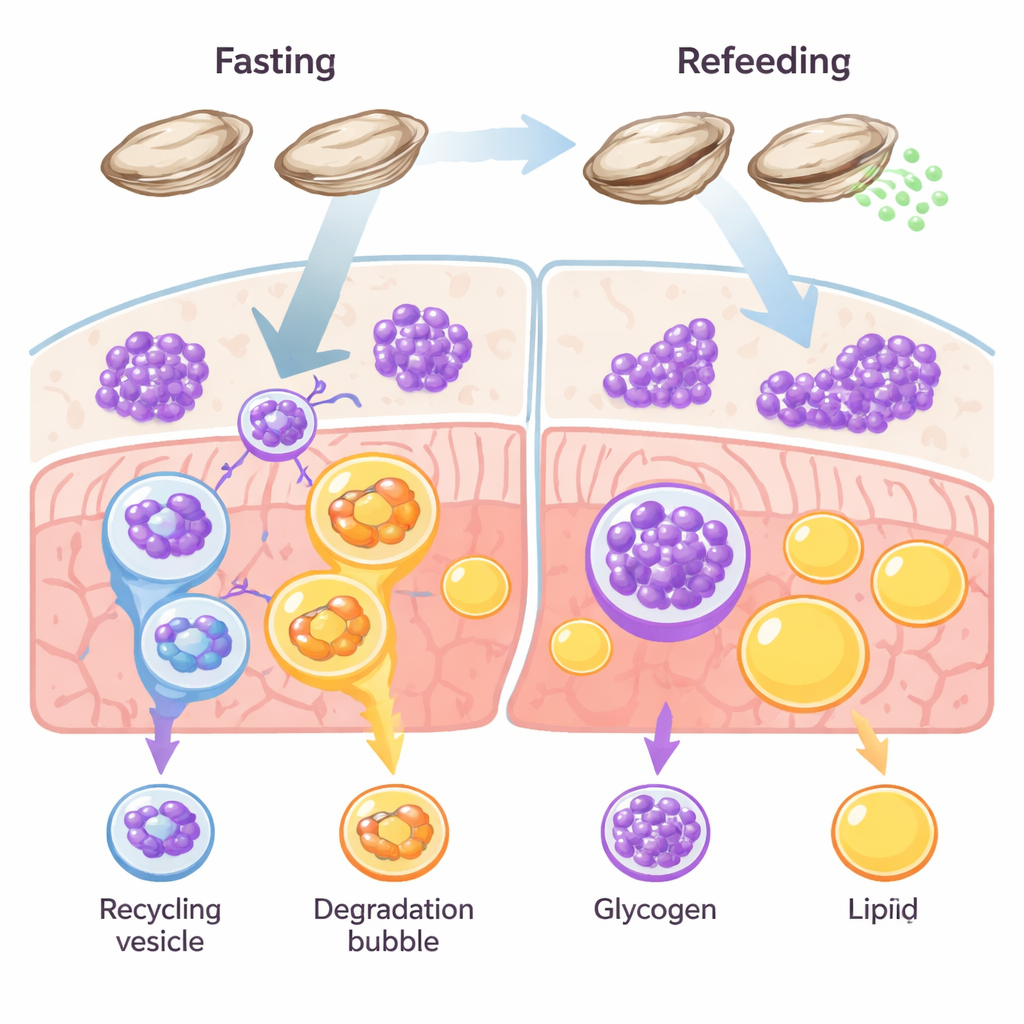
Eine Zucker-zuerst-Überlebensstrategie
Die meisten Tiere nutzen mehrere Energiespeicher, vor allem Fett und Glykogen. Bei Wirbeltieren wie Fischen und Säugetieren dominiert in der Regel Fett als Langzeitspeicher. Austern brechen diese Regel: Ihre Gewebe sind mit Glykogen durchzogen, und frühere Untersuchungen deuteten darauf hin, dass diese Schalentier bei Nahrungsmangel oder während der Gametenproduktion eher Zucker als Fett verbrennen. Die Autorinnen und Autoren wollten prüfen, ob Glykophagie — ein gezielter Abbau von Glykogen innerhalb der Zelle — in Austern während Fasten und Erholung als primärer Überlebensweg dient.
Zusehen, wie Zellen vom Speichern zum Ausgeben umschalten
Das Team setzte Pazifische Austern zwei Wochen lang unter Nahrungsentzug und fütterte sie anschließend wieder, um zu verfolgen, wie ihre Gewebe im Zeitverlauf reagierten. Während des Fastens zeigten mikroskopische Färbungen einen Anstieg von Autophagie-Markern — zellulären „Reinigungs“-Signalen — genau dort, wo Glykogen gespeichert war, während das Glykogen selbst abnahm. Die Fettreserven veränderten sich im Gegensatz dazu kaum. Nach dem Wiederfüttern kehrte Glykogen schnell zurück und die Autophagie-Signale sanken. Gleichzeitig schwankten die Mengen eines Schlüsselrezeptorproteins namens STBD1, das Glykogen speziell mit der Autophagie-Maschinerie verbindet, im Einklang mit dem Glykogenverbrauch. Ein anderer Rezeptor, der mit dem Fettrecycling verknüpft ist, p62, blieb größtenteils unverändert. Zusammengenommen deuten diese Muster auf einen dedizierten, zuckerzentrierten Recyclingweg hin: Glykophagie, nicht lipophagie zur Fettverbrennung, übernimmt die Hauptarbeit im Energiehaushalt der Auster.
Der molekulare Haken, der Glykogen greift
Glykophagie beruht darauf, dass STBD1 als molekularer Haken fungiert: Es bindet Glykogen und übergibt es an kleine Adapterproteine, die Recyclingvesikel aufbauen. Bei Austern erwies sich STBD1 als anders verdrahtet als sein Wirbeltiergegenstück. Das Austerprotein trägt seine glykogenbindende Region, bekannt als CBM20-Domäne, am vorderen Ende (N-Terminus), während wirbeltierliches STBD1 dieses Modul am hinteren Ende (C-Terminus) platziert und einen zusätzlichen fettigen Schwanz enthält, der es an Zellmembranen verankert. Computermodelle und Simulationen deuteten darauf hin, dass die N-terminale Anordnung bei Austern dem CBM20 eine stärkere, vielseitigere Greifkraft an verzweigten Zuckerketten verleiht. Laborexperimente bestätigten dies: gereinigtes Auster-STBD1 band Glykogen stärker als Fisch- oder Maus-STBD1, und als alle Versionen in menschlichen Zellen exprimiert wurden, bewirkte das Austerprotein einen stärkeren Abfall des Glykogens bei induzierter Autophagie.
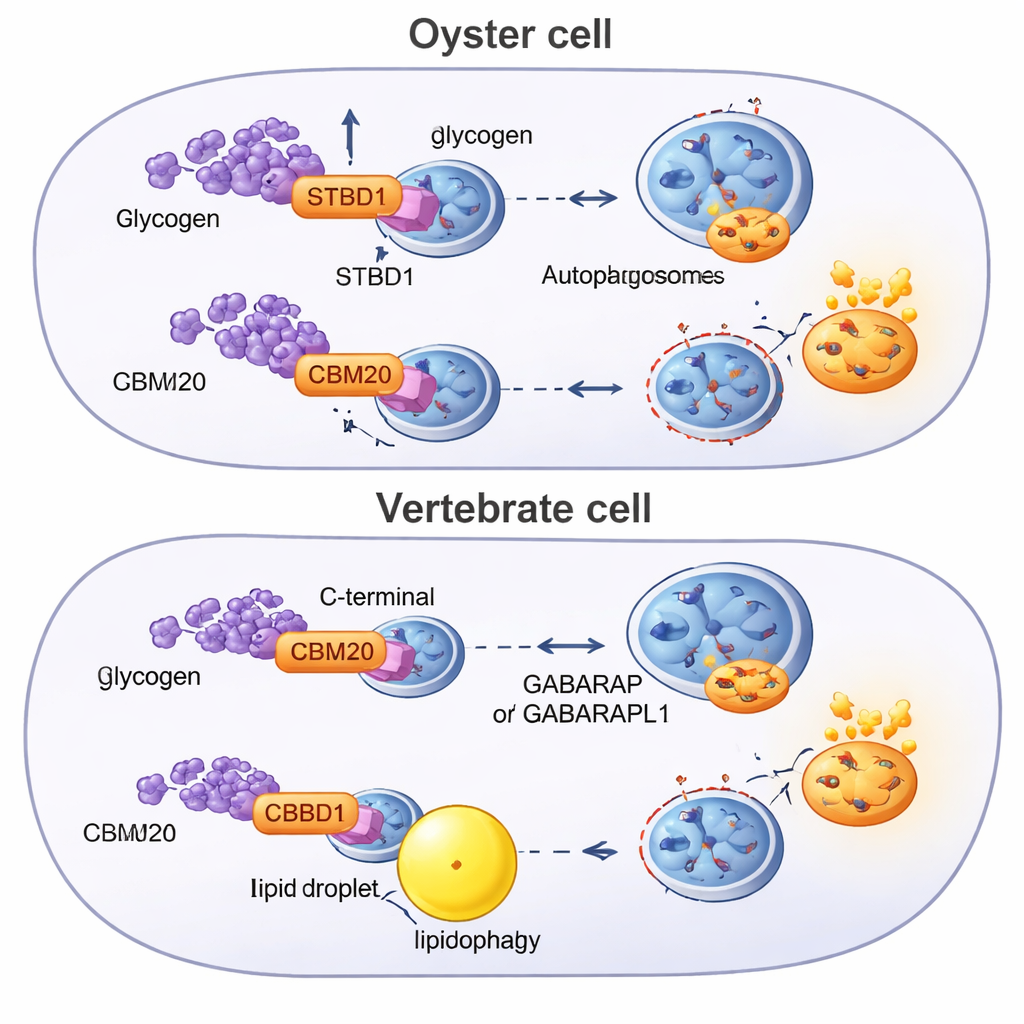
Umschaltung eines uralten Weges im Tierreich
Um herauszufinden, woher dieses System stammt, durchsuchten die Forschenden Genome zahlreicher Tiere nach CBM20-haltigen Proteinen und bauten evolutionäre Stammbäume. Sie fanden heraus, dass STBD1 eine bilaterale Erfindung ist — es erschien beim gemeinsamen Vorfahren der Tiere mit zweiseitigen Körperplänen —, aber seine Struktur wurde in verschiedenen Linien umgestaltet. Austern und andere Lophotrochozoa behalten tendenziell das ursprüngliche N-terminale CBM20-Design bei, wobei die Zuckerbindungsdomäne manchmal sogar dupliziert ist. Chordaten, die Gruppe, zu der Wirbeltiere gehören, zeigen eine andere Version, in der CBM20 an das Proteinende verschoben wurde. Diese Umordnung korreliert mit schwächerer Glykogenbindung und mit einer Stoffwechselstrategie, die stärker auf Fettabbau durch Lipophagie setzt, unterstützt durch andere Autophagie-Rezeptoren und Adapterproteine, die Austern fehlen.
Was das für die energetischen Entscheidungen des Lebens bedeutet
Für Nicht-Fachleute ist die Kernaussage, dass Tiere mehr als einen Weg entwickelt haben, um Energiemangel zu überstehen. Austern demonstrieren eine alte, zuckerzentrierte Strategie: eine hochaffine Version von STBD1 greift Glykogen schnell und führt es in zelluläre Recyclingeinheiten, wodurch Glykophagie eine Hauptenergiequelle bei Stress wird. Wirbeltiere dagegen scheinen diesen starken Zuckergriff gegen einen ausgewogeneren oder fettorientierteren Ansatz eingetauscht zu haben, unterstützt von anderen Proteinpartnern und Domänenanordnungen. Indem die Studie detaillierte Proteinstruktur mit den Energieentscheidungen ganzer Organismen verknüpft, zeigt sie, wie kleine molekulare „Umschaltungen“ verschiedenen Zweigen des Tierbaums helfen können, sich an ihre jeweiligen Umgebungen und Lebensweisen anzupassen.
Zitation: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Schlüsselwörter: Glykophagie, Glykogenstoffwechsel, Austernbiologie, Autophagie, Evolution des Stoffwechsels