Clear Sky Science · de
Epigenetische und metabolische Umbauprozesse in metastasierenden Phäochromozytomen und Paragangliomen, angetrieben durch SDHB‑Mutationen
Warum diese seltenen Tumoren wichtig sind
Phäochromozytome und Paragangliome sind seltene Tumoren, die aus hormonbildenden Nervenzellen entstehen, häufig in der Nähe der Nebennieren. Die meisten wachsen langsam und lassen sich durch Operationen heilen, aber bei etwa einem von fünf Fällen streuen sie schließlich in andere Organe und werden lebensbedrohlich. Diese Studie stellt eine einfache, aber entscheidende Frage: Was lässt einige dieser Tumoren gefährlich werden? Durch genaue Untersuchung, wie diese Krebsarten ihre Gene an- und abschalten und wie sie sich mit Energie versorgen, entdecken die Forschenden eine verborgene Verwundbarkeit, die sich eines Tages mit neuen Therapien angreifen lassen könnte.
Vom stillen Wachstum zur tödlichen Ausbreitung
Das Team konzentrierte sich auf Tumoren mit Veränderungen in einem Gen namens SDHB. SDHB unterstützt die Mitochondrien — die Kraftwerke der Zelle — bei einem Teil des Krebs‑Zyklus, einem zentralen energieproduzierenden Weg. Wenn SDHB beschädigt ist, reichert sich eine Substanz namens Succinat an, und die Zellen verhalten sich, als lebten sie in Sauerstoffmangel, selbst wenn dem nicht so ist. Die Forschenden untersuchten Gewebe von 34 Patientinnen und Patienten und verglichen Tumoren, die lokalisiert blieben, mit solchen, die bereits gestreut hatten. Mithilfe einer hochaufgelösten DNA‑Methylierungs‑Karte, die zeigt, wie chemische Marker Gene hoch- oder herunterregeln, stellten sie fest, dass metastatische Tumoren ein stärkeres Muster von Genabschaltung aufwiesen als gutartige Tumoren, insbesondere wenn SDHB mutiert war.
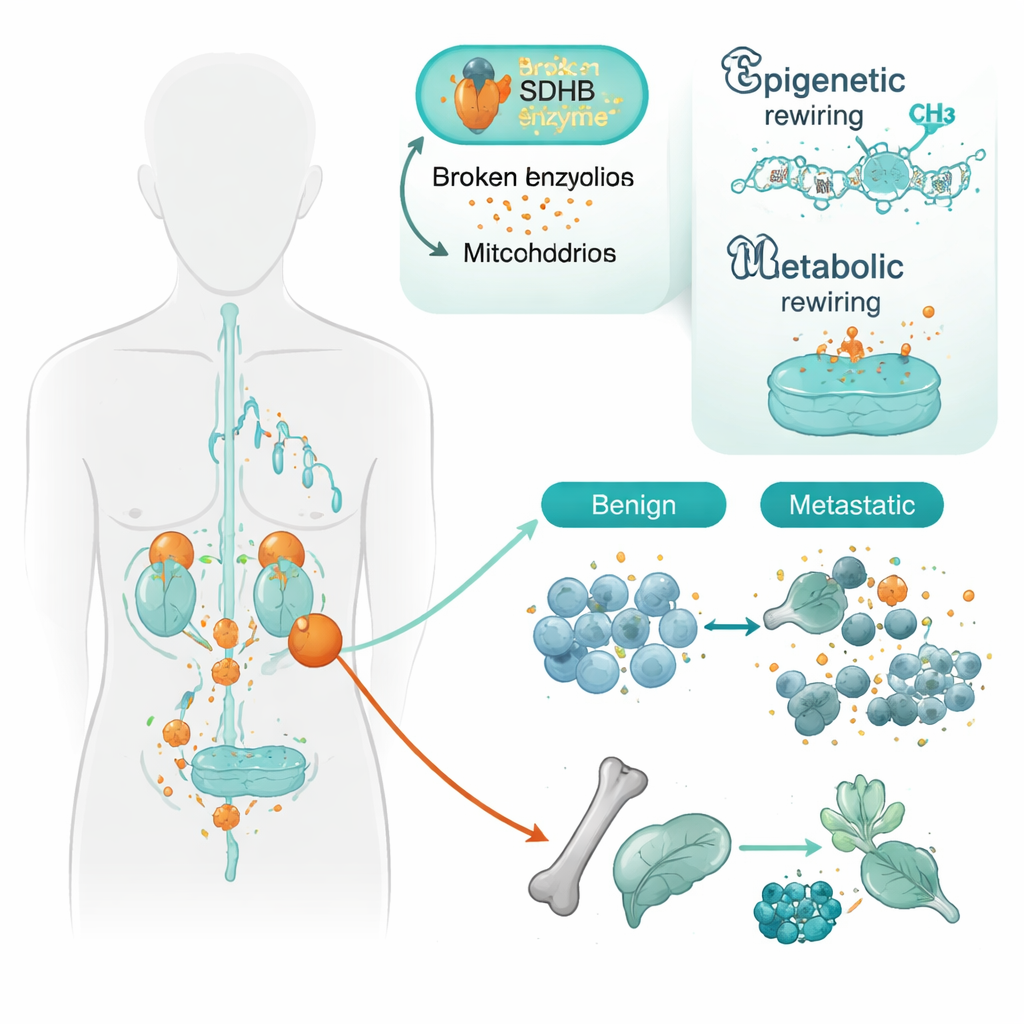
Umschaltung der Zellidentität
Viele der in aggressiven Tumoren stillgelegten Gene waren solche, die den nervenähnlichen Zellen helfen, auszureifen und ihre spezialisierte Identität zu erhalten. Dazu gehören Genfamilien, die steuern, wie Zellen aneinander haften, wie sie ihr Erbgut organisieren und wie sie sich zu einem bestimmten Zelltyp entwickeln. Ein auffälliges Beispiel war das Zelladhäsionsgen PCDHGC3. Sogar in nicht streuenden SDHB‑mutanten Tumoren war die Kontrollregion dieses Gens bereits teilweise abgeschaltet; in metastatischen Tumoren war die Stilllegung noch ausgeprägter. Ein anderes Gen, SATB2, das bei der Organisation großer DNA‑Abschnitte eine Rolle spielt, war ausschließlich in metastatischen Tumoren stillgelegt, unabhängig vom SDHB‑Status. Zusammen deuten diese Muster darauf hin, dass der Verlust von SDHB Zellen für einen weniger ausgereiften, beweglicheren Zustand „vorbereitet“, und zusätzliche epigenetische Veränderungen ihnen dann helfen, sich zu lösen und auszubreiten.
Umverdrahtung, wie Tumoren Zucker verwerten
Überraschenderweise führten nicht alle Veränderungen zu Genabschaltung. Eine kleinere Gruppe von Genen wurde weniger methyliert und dadurch aktiver; diese waren stark an der Aufnahme von Zuckern in Zellen beteiligt. Hervor stach dabei das Fructosetransporter‑Gen SLC2A5. Sein Produkt, bekannt als GLUT5, schleust Fructose — einen in Früchten und vielen verarbeiteten Lebensmitteln verbreiteten Zucker — in die Zellen. In Labormodellen von tumorähnlichen Zellen, die niedrigem Sauerstoff ausgesetzt waren, schaltete sich SLC2A5 kontinuierlich an, während andere Zuckertransporter weniger konsistent reagierten. Die Autorinnen und Autoren züchteten dann patientenabgeleitete Zellkulturen aus PPGL‑Tumoren und zeigten, dass bei Glucosemangel die Zugabe von Fructose diesen Zellen half, weiter zu teilen, besonders unter sauerstoffarmen Bedingungen, die das Tumorumfeld nachahmen.
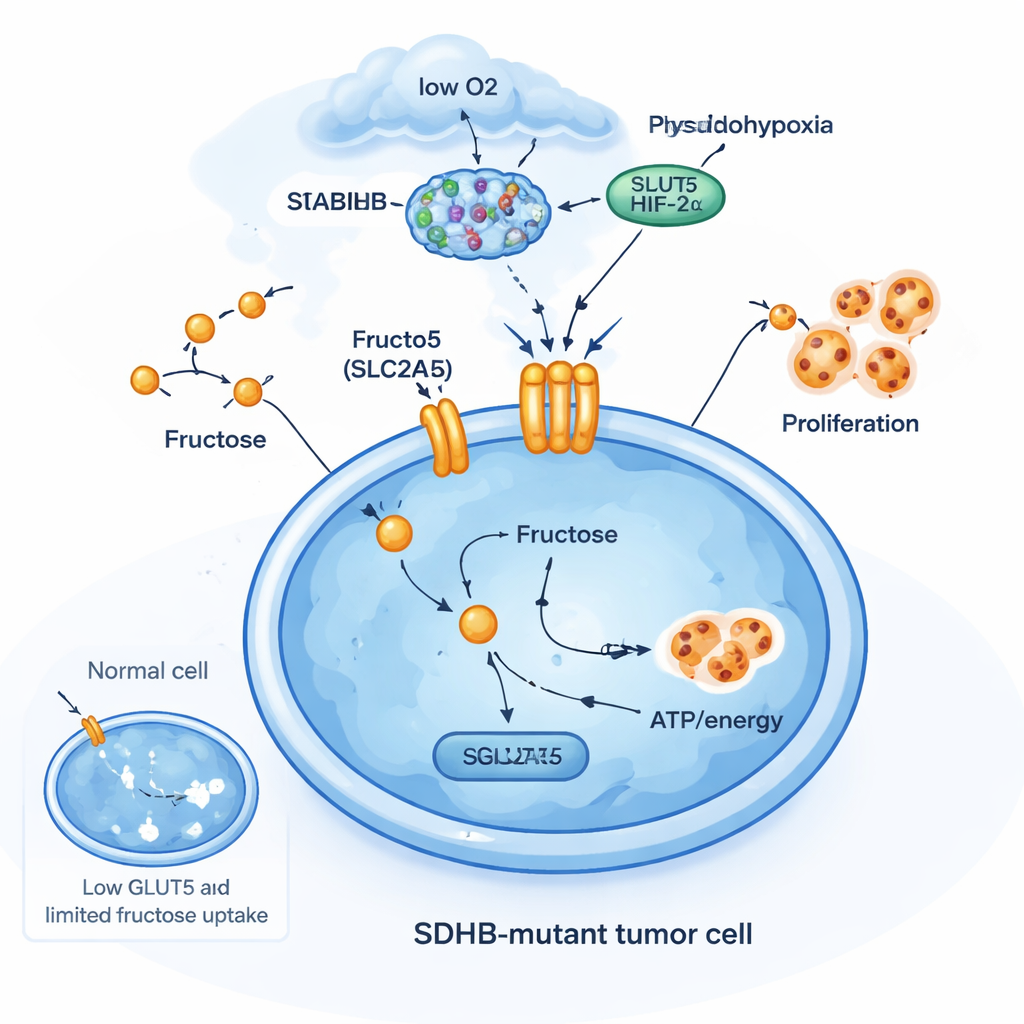
Ein Fructose‑betriebenes Überlebensmanöver
Um zu verstehen, warum SDHB‑Mutationen hier eine Rolle spielen, entfernte das Team SDHB in mehreren Zelltypen per Geneditierung. In chromaffinähnlichen Zellen aus der Nebenniere und in einer Nierenkrebszelllinie mit konstanter Aktivierung des sauerstoffsensitive Faktors HIF2α erhöhte der Verlust von SDHB die SLC2A5‑Spiegel. In gängigen Krebszelllinien, die diese neuroendokrinen oder HIF2α‑Eigenschaften nicht besaßen, aktivierte derselbe SDHB‑Knockout SLC2A5 jedoch nicht. Das zeigt, dass der Fructosetransporter kein generischer Stress‑Antwortmechanismus ist; er ist eine hochspezifische Anpassung in bestimmten Zelltypen, die bereits in einem „pseudo‑hypoxischen“ Zustand leben. In diesen Zellen kooperieren SDHB‑Verlust, Succinatansammlung und HIF2α‑Aktivität, um eine neue metabolische Tür zu öffnen: Fructoseaufnahme zur Energieversorgung, wenn Sauerstoff und Glucose begrenzt sind.
Was das für Patientinnen und Patienten bedeutet
Kurz gesagt zeigt die Studie eine doppelte Umstellung in SDHB‑mutanten metastatischen PPGLs. Erstens ist ihr DNA‑Kontrollsystem so umprogrammiert, dass Zellen in einen weniger spezialisierten, plastischeren Zustand gedrängt werden, der zur Invasion neigt. Zweitens wird ihr Energiesystem so umgebaut, dass es Fructose als alternativen Brennstoff in rauen, sauerstoff‑ und glucosearmen Nischen anzapft. Indem die Arbeit den Fructosetransporter SLC2A5/GLUT5 als Schlüsselakteur dieses Prozesses identifiziert, weist sie auf eine mögliche Achillesferse hin: Das Blockieren der Fructoseaufnahme oder ihres Stoffwechsels könnte diese Tumoren selektiv aushungern, während die meisten normalen Gewebe verschont blieben. Obwohl derartige Therapien noch nicht verfügbar sind, ist die Kartierung dieser epigenetischen und metabolischen Landschaft ein entscheidender Schritt hin zu präziseren, stoffwechselorientierten Behandlungen für Patientinnen und Patienten mit hochriskanten SDHB‑mutanten PPGLs.
Zitation: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Schlüsselwörter: Phäochromozytom, Paragangliom, SDHB‑Mutation, Epigenetik, Fructosestoffwechsel