Clear Sky Science · de
Multi-omische Analyse der menschlichen PHACTR1-Signalnetzwerke
Warum dieses Gefäßgen für Sie wichtig ist
Herzinfarkte, Schlaganfälle und Bluthochdruck lassen sich alle auf die Gesundheit unserer Blutgefäße zurückführen. Ein einzelnes Gen namens PHACTR1 tauchte in großen genetischen Studien zu diesen Erkrankungen immer wieder auf, doch Forscherinnen und Forscher haben lange nicht verstanden, warum. Diese Studie nutzte einen umfassenden „auf allen Ebenen“ Blick in menschliche Zellen, um zu kartieren, was PHACTR1 tatsächlich bewirkt. Sie zeigt, wie das Gen Zellwachstum, Energieverbrauch und Eisenhandling beeinflussen kann — Prozesse, die letztlich die Gesundheit der Arterien mitbestimmen.
Ein großflächiger Scan innerhalb der Zellen
Anstatt sich auf ein Molekül nach dem anderen zu konzentrieren, verwendeten die Forscher eine Strategie namens Multi-Omics — sie maßen gleichzeitig Tausende von RNAs, Proteinen, kleinen Metaboliten und Fetten (Lipiden) in den Zellen. Sie veränderten menschliche Zellen so, dass diese entweder zusätzliches PHACTR1 produzierten oder das Gen herunterreguliert war, um natürliche genetische Unterschiede zwischen Menschen nachzuahmen. Durch den Vergleich dieser veränderten Zellen mit normalen Kontrollen über vier molekulare Ebenen hinweg und mithilfe ausgefeilter Pfad-Analyse-Software erstellten sie eine globale Karte, wie Änderungen an PHACTR1 in die zellulären Abläufe hineinwirken. 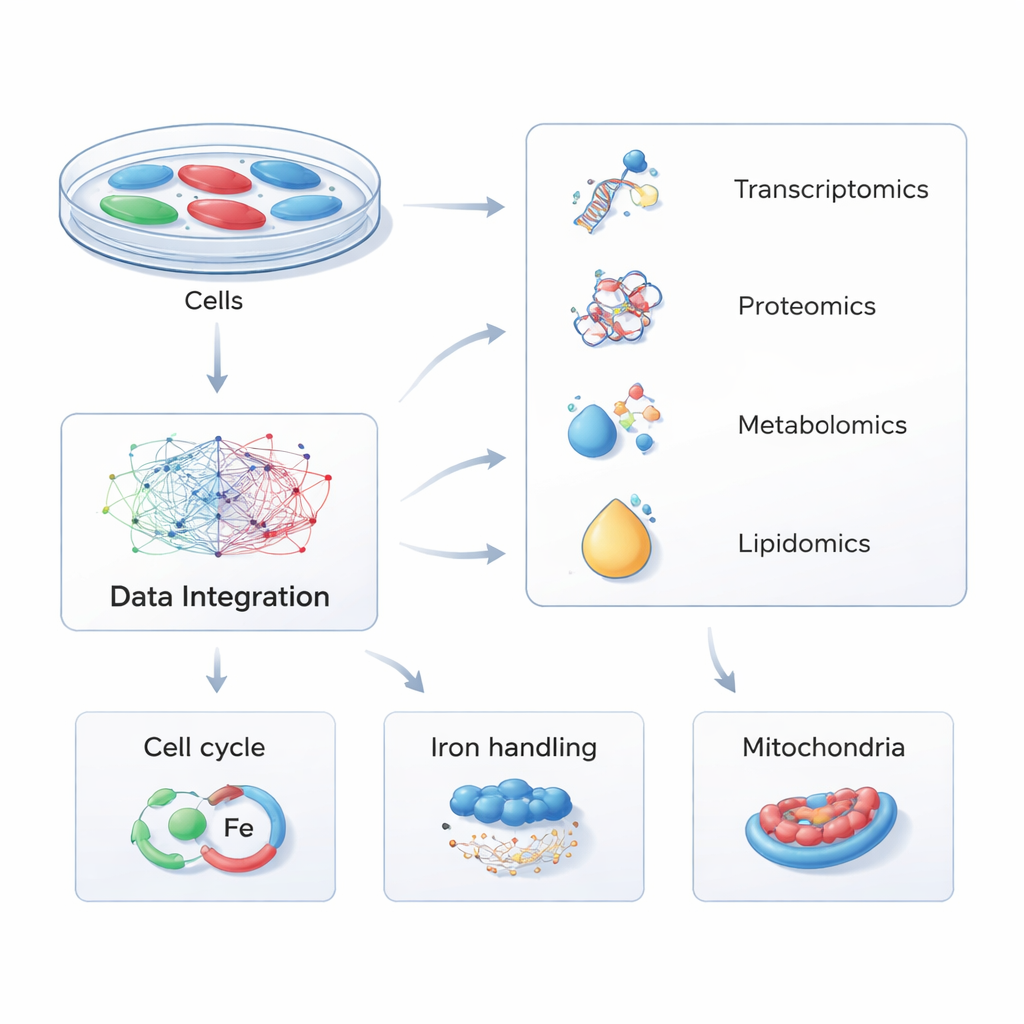
Jenseits des Zellskeletts: Steuerung der Wachstumszyklen
PHACTR1 war bisher hauptsächlich für die Organisation des inneren Gerüsts aus Aktinfasern bekannt. Die neuen Daten zeigten jedoch, dass es auch eine starke Rolle bei der Kontrolle des Zellzyklus spielt — der Choreographie, mit der Zellen ihre DNA kopieren und sich teilen. Zellen mit erhöhtem PHACTR1 verließen vermehrt die Ruhephase G1 und sammelten sich in DNA-kopierenden und vor der Teilung liegenden Phasen, während weniger Zellen erfolgreich in die vollständige Mitose eintraten. Schlüsselfaktoren wie Cyclin B1, Cdt1 und andere Zellzyklus-Proteine waren verändert. Als das Team die Experimente in primären humanen Endothelzellen — den Zellen, die Blutgefäße auskleiden — wiederholte, beobachteten sie erneut Veränderungen zentraler Zellzyklus-Regulatoren. Das legt nahe, dass PHACTR1 mitentscheidet, ob Gefäßzellen ruhen, sich teilen oder ins Stocken geraten — ein Gleichgewicht, das sowohl bei der Reparatur von Gefäßwänden als auch bei der Entstehung gefährlicher Gewebeüberwüchse entscheidend ist.
Eisen managen und vor Schäden schützen
Die Multi-Omics-Integration wies außerdem auf eisenbezogene Wege und eine spezialisierte Form eisengetriebener Zellschädigung namens Ferroptose hin. Zwar starben die Zellen nicht aktiv durch Ferroptose, doch erhöhte PHACTR1-Werte verringerten die Mengen wichtiger eisenverarbeitender Proteine, darunter das Ferritin-Schwerketten-Protein (die Hauptschale zur Eisenspeicherung) und Hämoxygenase 1 (die Eisen aus Häm recycelt). In primären Endothelzellen veränderte PHACTR1 ähnlich diese Proteine und zentrale Abwehrfaktoren gegen oxidative Schäden. Da fehlgesteuertes Eisen Entzündungen, oxidativen Stress und instabile Gefäßplaques befeuern kann, deutet dies darauf hin, dass PHACTR1 beeinflussen könnte, wie Gefäßzellen Eisen speichern und entgiften — und damit potenziell die Anfälligkeit für bestimmte Gefäßerkrankungen mitbestimmt.
Mitochondrien, Energie und Gefäßgesundheit
Eine weitere Überraschung war die Rolle von PHACTR1 in Mitochondrien, den Kraftwerken der Zelle. Die Forscher fanden PHACTR1-Protein in isolierten Mitochondrien und beobachteten, dass Änderungen seines Niveaus das mitochondriale Netzwerk umgestalteten. Bei hohem PHACTR1 waren die Mitochondrien stärker verlängert, und ein Protein namens Drp1 war an einer Stelle chemisch modifiziert, die die mitochondriale Spaltung vermindert. Die Konzentration eines Gerüstproteins, AKAP1, das hilft, Signale an der mitochondrialen Oberfläche zu organisieren, stieg und fiel parallel zu PHACTR1. Diese strukturellen Veränderungen korrespondierten mit Verschiebungen in der Energieerzeugung: Hoher PHACTR1 verringerte die mitochondriale ATP-Produktion und war verbunden mit einer Anhäufung bestimmter Fettsäure-abgeleiteter Moleküle, die ein vermindertes Fettverbrennen signalisieren, während niedriges PHACTR1 die Zellen stärker auf zuckerverarbeitende Glykolyse setzte. Analysen menschlicher Arterienproben zeigten, dass PHACTR1 und AKAP1 tendenziell gemeinsam aktiviert sind, wodurch dieser mitochondriale Kontrollkreis direkt mit echten Blutgefäßen verknüpft wird. 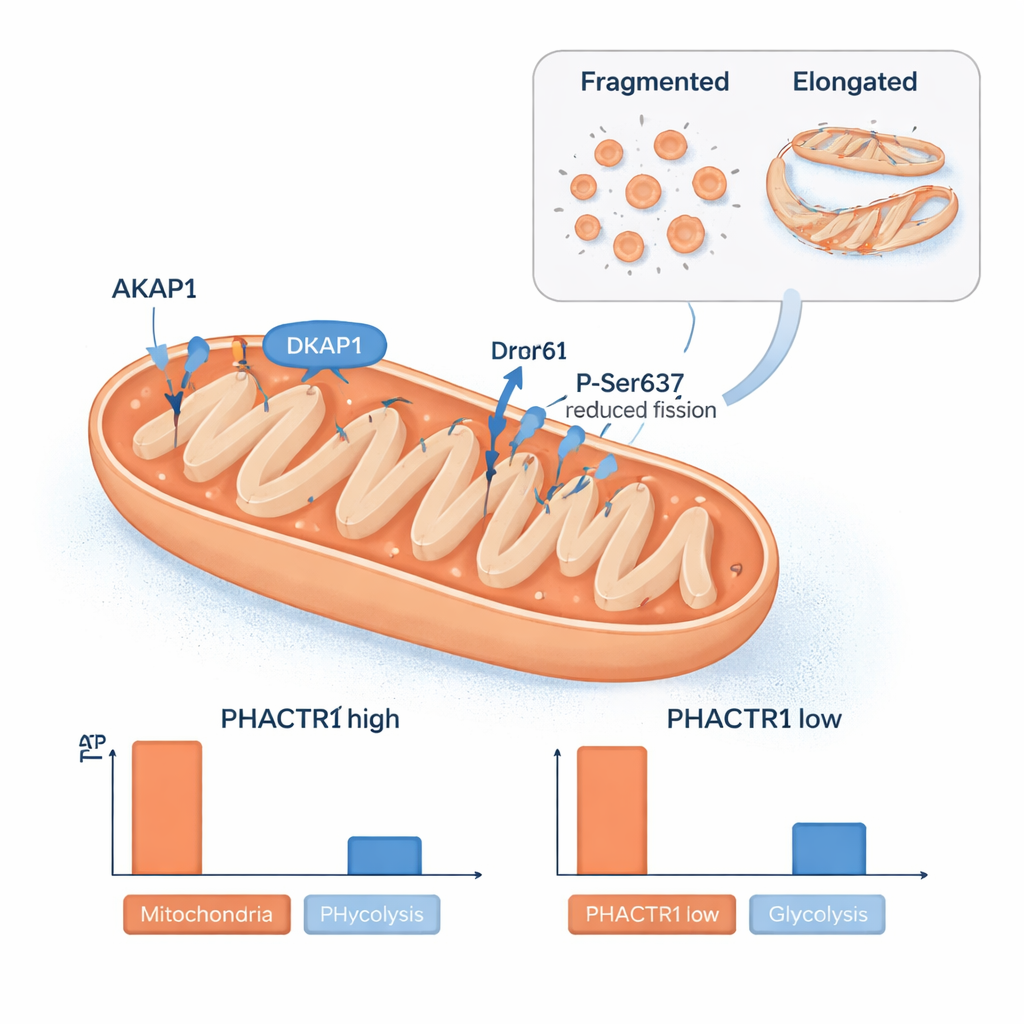
Was das alles für Blutgefäße bedeutet
Insgesamt zeigt diese Arbeit, dass PHACTR1 kein gen mit nur einer Funktion ist, sondern ein übergeordneter Koordinator, der beeinflusst, wie Gefäßzellen sich teilen, Eisen speichern und ihre Energiebilanz steuern. Durch das Kartieren dieser Verbindungen über Tausende von Molekülen hinweg hilft die Studie zu erklären, warum natürliche Unterschiede in PHACTR1 mit einem breiten Spektrum gefäßbezogener Erkrankungen verbunden sind — von koronarer Herzkrankheit über spontane Arterienrisse bis hin zu Migräne. Für Laien lautet die Botschaft: Ein in der Humangenetik identifiziertes Gen wird nun auf konkrete zelluläre Verhaltensweisen zurückgeführt, die Plaquebildung, Gefäßstabilität und Energiehaushalt beeinflussen. Langfristig kann das Verständnis dieser von PHACTR1 gesteuerten Netzwerke den Weg zu präziseren Therapien ebnen, die Zellzyklen, Eisenmanagement oder mitochondriale Funktionen wieder in einen gesünderen Zustand lenken — bei Menschen mit erhöhtem kardiovaskulärem Risiko.
Zitation: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Schlüsselwörter: PHACTR1, Gefäßerkrankungen, Multi-Omics, Mitochondrien, Eisenstoffwechsel