Clear Sky Science · de
Die Hemmung von PAK4 fördert gemcitabin-induzierte Pyroptose bei Bauchspeicheldrüsenkrebs über die NLRP1/caspase-3/GSDME-Achse
Warum es wichtig sein könnte, Krebszellen auf „feurige“ Weise zu töten
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebserkrankungen, und selbst unsere besten Chemotherapeutika versagen häufig, wenn Tumoren Resistenzen entwickeln. Diese Studie untersucht eine überraschende Wendung: Dasselbe Medikament, Gemcitabin, kann Krebszellen auf eine explosivere, entzündliche Weise abtöten — Pyroptose genannt — wenn eine wichtige molekulare „Bremse“ namens PAK4 ausgeschaltet wird. Das Verstehen und gezielte Ausschalten dieser Bremse könnte bestehende Therapien für viele Patienten wirkungsvoller machen.
Ein hartnäckiger Krebs, der Behandlungen abschüttelt
Das duktale Adenokarzinom der Bauchspeicheldrüse wird meist spät diagnostiziert und spricht schlecht auf Therapien an, weshalb Gemcitabin trotz seiner Einschränkungen eine zentrale Rolle spielt. Gemcitabin tötet Zellen typischerweise durch Apoptose, eine ordentliche, stille Form des programmierten Zelltods. Mehr als die Hälfte der in dieser Studie untersuchten Pankreastumoren produzierte jedoch hohe Mengen eines Proteins namens GSDME, das diesen stillen Tod in Pyroptose umschalten kann — eine schnelle, „explodierende“ Form des Zelltods, die die Zellmembran beschädigt und entzündliche Signale freisetzt. Das wirft eine zentrale Frage auf: Wenn Tumoren Pyroptose durchlaufen können, warum sind so viele dennoch gegen Gemcitabin resistent?
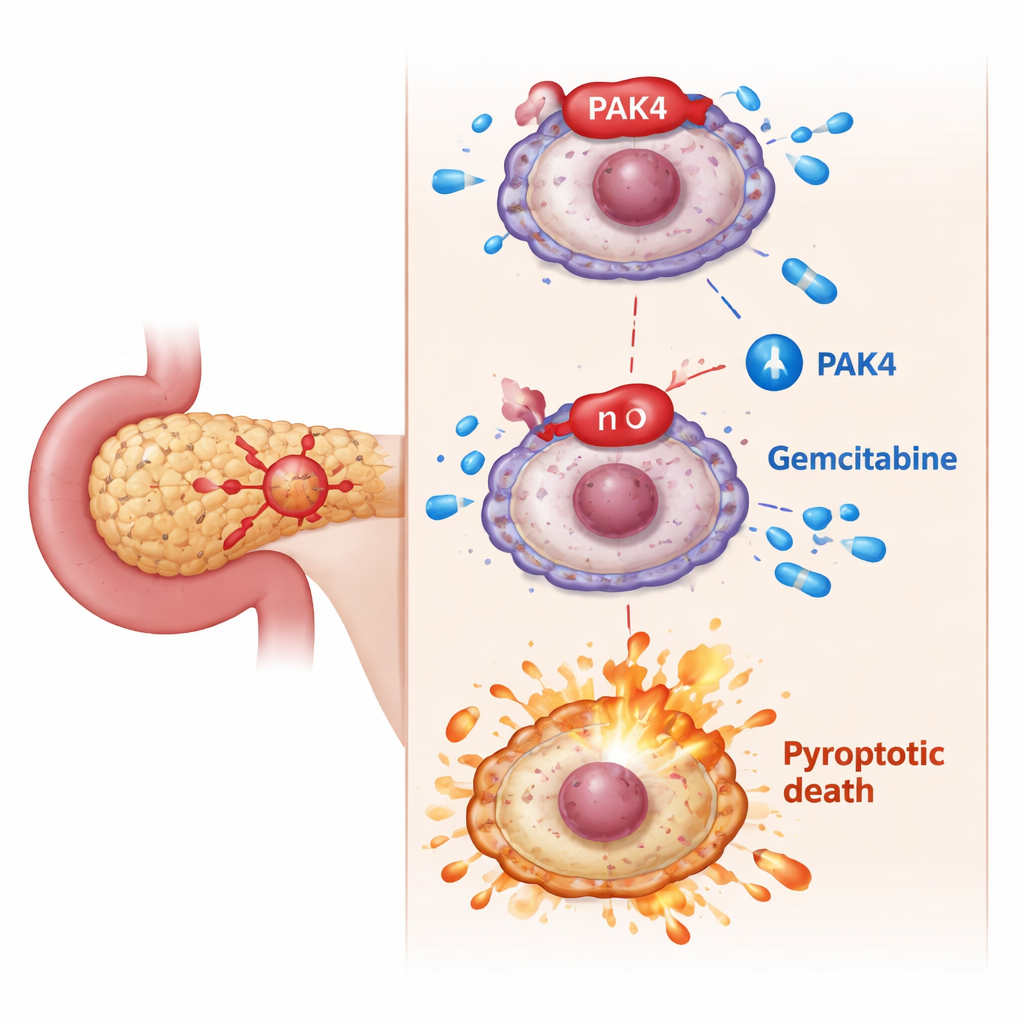
Die versteckte Bremse: PAK4 blockiert den „feurigen“ Zelltod
Die Forschenden konzentrierten sich auf PAK4, ein wachstumsförderndes Protein, das bei Bauchspeicheldrüsenkrebs häufig überaktiv ist und mit schlechter Reaktion auf Gemcitabin in Verbindung gebracht wird. In Zellexperimenten ließen sich Krebszellen mit hohem PAK4-Spiegel schwerer mit Gemcitabin töten. Als das Team PAK4 reduzierte, wurde Gemcitabin plötzlich wesentlich tödlicher: Die Zellen zeigten typische pyroptotische Merkmale — Anschwellen, ballonartige Blasen, platzende Membranen und vermehrte Freisetzung von Zellinhalten. Auf molekularer Ebene hing dieser Wechsel davon ab, dass GSDME von einem anderen Protein, caspase-3, in ein aktives Fragment geschnitten wurde. Die Blockade von caspase-3 verhinderte, dass GSDME Pyroptose auslöst, was bestätigt, dass PAK4 normalerweise diese Todesbahn bremst.
Wie PAK4 den Todesalarm der Zelle ausschaltet
Tiefer gehende Untersuchungen zeigten, dass PAK4 GSDME nicht direkt angreift. Stattdessen sabotiert es einen upstream „Alarmsensor“ namens NLRP1. Bei Patienten war ein höherer NLRP1-Spiegel mit besserem Überleben verbunden, was darauf hindeutet, dass er hilft, Tumoren in Schach zu halten. In Krebszellen führte das Entfernen von NLRP1 zu einem starken Rückgang der gemcitabin-induzierten Zellsterblichkeit und der GSDME-Aktivierung, was zeigt, dass NLRP1 in die Pyroptose-Mechanik einspeist. PAK4- und NLRP1-Spiegel standen in Tumorproben in umgekehrtem Verhältnis zueinander: Wo PAK4 hoch war, war NLRP1 niedrig. Die Studie zeigte, dass aktives PAK4 über ein anderes Protein, die E3-Ligase Mdm2, wirkt, um NLRP1 für den Abbau durch das zelluläre Entsorgungssystem zu markieren. Indem PAK4 NLRP1 so markiert, verhindert es die Aktivierung einer Kaskade — über caspase-9 und caspase-3 — die normalerweise in einer GSDME-vermittelten Pyroptose enden würde.
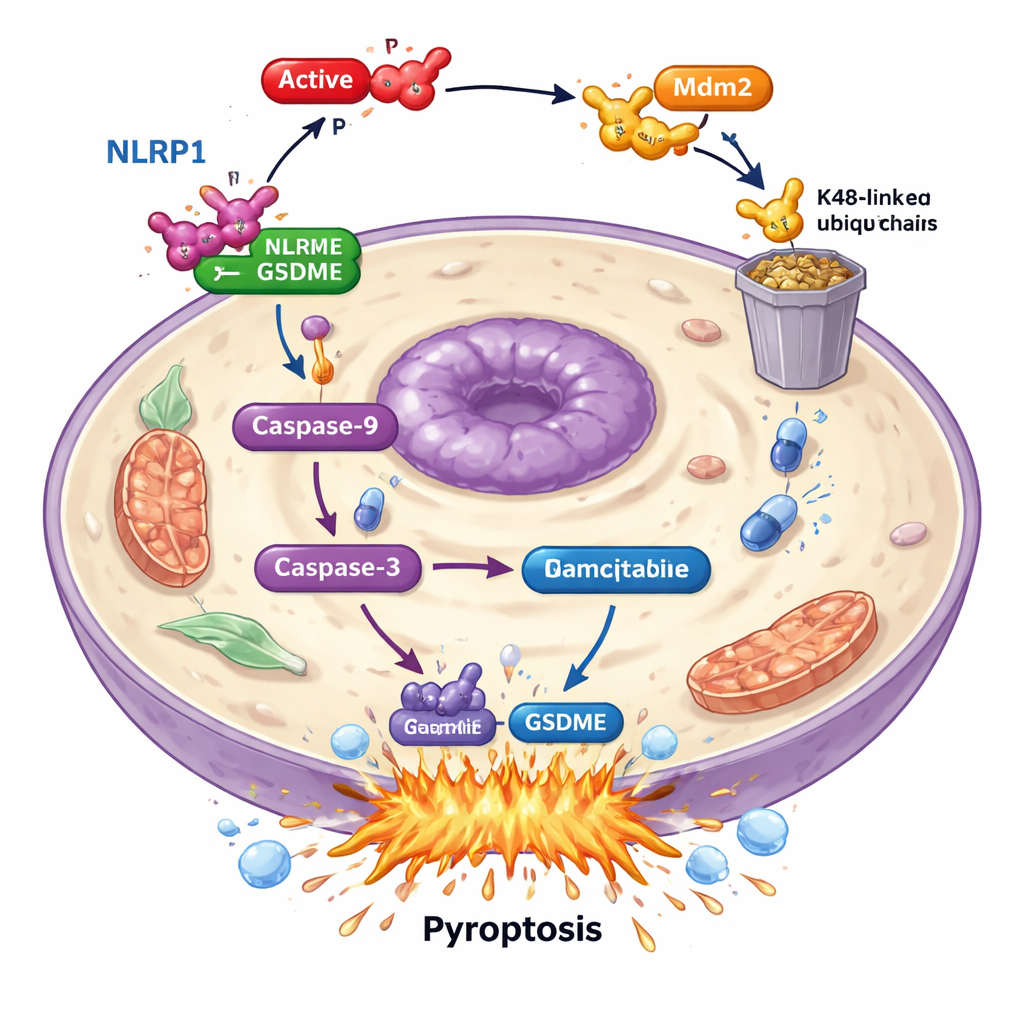
PAK4 ausschalten, um die Chemotherapie zu verstärken
Da PAK4 als Bremse der Pyroptose wirkt, prüfte das Team, ob das Blockieren seiner Aktivität Gemcitabins Wirksamkeit wiederbeleben kann. Sie verwendeten einen kleinen PAK4-Inhibitor namens PF-3758309. Allein bewirkte dieser Inhibitor bereits eine Verlagerung der Pankreaskrebszellen in Richtung Pyroptose, mit gesteigerter Aktivierung von caspase-3, GSDME-Spaltung und Membranruptur. In Kombination mit Gemcitabin war der Effekt noch stärker: Mehr Zellen starben durch Pyroptose, und molekulare Marker dieses Todeswegs wurden verstärkt. In Mausmodellen mit menschlichen Pankreastumoren führten sowohl die Reduktion von PAK4 als auch die Behandlung mit dem PAK4-Inhibitor dazu, dass Gemcitabin Tumoren wirksamer verkleinerte und pyroptotische Marker in den Tumoren verstärkte.
Was das für Patienten und künftige Therapien bedeutet
Einfach gesagt offenbart diese Arbeit ein molekulares Schloss — PAK4 — das Bauchspeicheldrüsenkrebszellen daran hindert, bei Chemotherapie auf eine besonders zerstörerische Weise zu sterben. Durch das Ausschalten von PAK4 könnten Ärzte Tumoren, die mit Gemcitabin behandelt werden, in Pyroptose treiben, das Medikament wirksamer machen und möglicherweise das Immunsystem gegen den Krebs mobilisieren. Obwohl weitere Arbeiten in patientenabgeleiteten Modellen und klinischen Studien nötig sind, schlägt die Studie einen klaren Fahrplan vor: Zielgerichtete Interventionen in der PAK4–Mdm2–NLRP1–GSDME-Achse könnten resistente Tumoren in therapierbare verwandeln, zum Teil mit bereits verfügbaren Wirkstoffen in intelligenteren Kombinationen.
Zitation: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Resistenz gegen Gemcitabin, Pyroptose, PAK4, zielgerichtete Therapie