Clear Sky Science · de
CHK1-Hemmung beseitigt abnorme Glykogenansammlungen in einem Caenorhabditis elegans-Modell der Glykogenspeicherkrankheit III
Warum ein winziger Wurm für eine seltene Krankheit wichtig ist
Die Glykogenspeicherkrankheit Typ III ist eine seltene vererbte Erkrankung, bei der der Körper Glykogen, die Speicherform von Zucker, nicht richtig abbauen kann. Das führt zu abnormen Glykogenansammlungen in Organen wie Leber und Muskeln und verursacht Unterzucker, vergrößerte Lebern, Muskelschwäche und andere schwere Probleme. Die verfügbaren Behandlungen sind begrenzt, und bestehende Tiermodelle bilden nicht vollständig ab, was beim Menschen passiert. In dieser Studie wandten sich die Forschenden einem unerwarteten Helfer zu — einem mikroskopisch kleinen Fadenwurm namens Caenorhabditis elegans — um ein präziseres Krankheitsmodell zu entwickeln und nach neuen therapeutischen Zielen zu suchen.
Ein Wurmmodell der menschlichen Erkrankung erstellen
Das Team konzentrierte sich auf das AGL-Gen, das das Enzym herstellt, das Verzweigungen im Glykogen abschneidet, damit es abgebaut werden kann. Mutationen in AGL verursachen die Glykogenspeicherkrankheit Typ III. Würmer besitzen ein eng verwandtes Gen namens agl-1, daher nutzten die Forschenden CRISPR-Geneditierung, um in Würmern zwei patientenbezogene Mutationen nachzubilden und eine vollständige Gen-Deletion zu erzeugen. Diese gentechnisch veränderten Würmer zeigten alle deutliche Anzeichen abnormaler Glykogenansammlungen, sichtbar als starke Färbung in ihren Därmen, hautähnlichen Geweben und Muskeln. Sie wurden außerdem empfindlicher gegenüber Glukose: Bei Zuckerexposition überlebten mehr ihrer Embryonen nicht, was das widerspiegelt, wie Patienten-Zellen Schwierigkeiten haben, mit Energie umzugehen. 
Gesundheitsprobleme über die Zuckeransammlung hinaus
Obwohl die Mutantenwürmer mit bloßem Auge normal wirkten, zeigten genauere Tests weitreichende Gesundheitsprobleme. Alle drei agl-1-Mutanten hatten eine verkürzte Lebensdauer und produzierten weniger Nachkommen als normale Würmer. Sie entwickelten sich langsamer von Larven zu Erwachsenen, und ihre Beweglichkeit war eingeschränkt. Eine Variante, genannt S1444R, zeigte besonders starke Probleme beim Schwimmen und entwickelte altersbedingte Lähmungserscheinungen auf festen Oberflächen. Diese Beobachtungen deuten darauf hin, dass das Wurmmodell nicht nur falsche Glykogenspeicherung abbildet, sondern auch den breiteren Vitalitätsverlust einfängt, der bei Menschen mit der Erkrankung beobachtet wird, wodurch es ein leistungsfähiges Werkzeug ist, um zu untersuchen, wie spezifische Mutationen den Körper beeinflussen.
Die Gene der Würmer nach verborgenen Hinweisen lesen
Um zu verstehen, was in den Zellen schieflief, untersuchten die Forschenden die Genaktivität im gesamten Wurmgenom. Sie fanden über tausend Gene, die in den Mutanten stärker aktiviert waren als in normalen Würmern, und eine kleinere Gruppe, die weniger aktiv war. Gene, die an Spermienfunktion, Wachstum und Muskelentwicklung beteiligt sind, wurden tendenziell herunterreguliert, was zu den beobachteten Fortpflanzungs- und Bewegungsproblemen passt. Gleichzeitig waren Wege, die mit Proteinmodifikation und Phosphatstoffwechsel zusammenhängen, hochreguliert, was darauf hinweist, dass die Zellen der Würmer durch Änderungen in der Steuerung der Proteinaktivität zu kompensieren versuchen. Diese umfassende Verschiebung der Genaktivität zeichnete ein Bild eines Organismus unter chronischem metabolischem Stress.
Von tausenden Wirkstoffen zu einigen vielversprechenden Treffern
Als Nächstes fragten die Forschenden, ob vorhandene Medikamente die Gesundheit der Würmer verbessern könnten. Sie testeten fast 4.000 kleine Moleküle und identifizierten 25, die das Schwimmverhalten des S1444R-Mutanten verbesserten. Beim Überprüfen, welche dieser Substanzen auch die Glykogenansammlung reduzierten, stachen zwei Verbindungen hervor: Pimozid, ein Antipsychotikum, und Pramoxin, ein lokales Betäubungsmittel. Beide beeinflussen bekannte Signalwege in Zellen, und ihre Wirkung auf Glykogen deutet auf tiefere Verbindungen zwischen nervenbezogener Signalgebung und Energiemanagement hin. Parallel gruppierten die Forschenden Wirkstoff-Treffer nach ihren bekannten Zielen und entwickelten eine rechnerische Pipeline, um Gene hervorzuheben, deren Hemmung die vorteilhaften Effekte der Verbindungen nachahmen könnte. Diese Analyse wies auf mehrere Kandidatengene hin, deren Abschaltung durch RNA-Interferenz die Glykogenwerte in den Würmern veränderte.
CHK1-Hemmung als neuer therapeutischer Ansatz
Unter den Kandidatengenen stach eines hervor: chk-1, das ein Protein namens CHK1 kodiert, das vor allem für die Kontrolle des Zellzyklus und die Reaktion auf DNA-Schäden bekannt ist. Die Herunterregulierung von chk-1 in den S1444R-Würmern verringerte deren Glykogenansammlungen und verbesserte ihre Lähmungserscheinungen, ohne dieselbe Wirkung in anderen Mutanten zu zeigen — was darauf hindeutet, dass der Nutzen von der spezifischen Variantenabhängigkeit bestimmt wird. Ein Wirkstoff, der CHK1 selektiv blockiert, namens Rabusertib, brachte ähnliche Verbesserungen bei Glykogenwerten und Bewegung. Das Team prüfte, ob dieser Effekt über AMPK, einen zentralen Energiesensor, vermittelt wird, fand jedoch, dass das Blockieren von AMPK Glykogen oder chk-1-Aktivität nicht veränderte. Das deutet darauf hin, dass CHK1 die Glykogenspeicherung über einen separaten, zuvor unbekannten Weg beeinflusst. 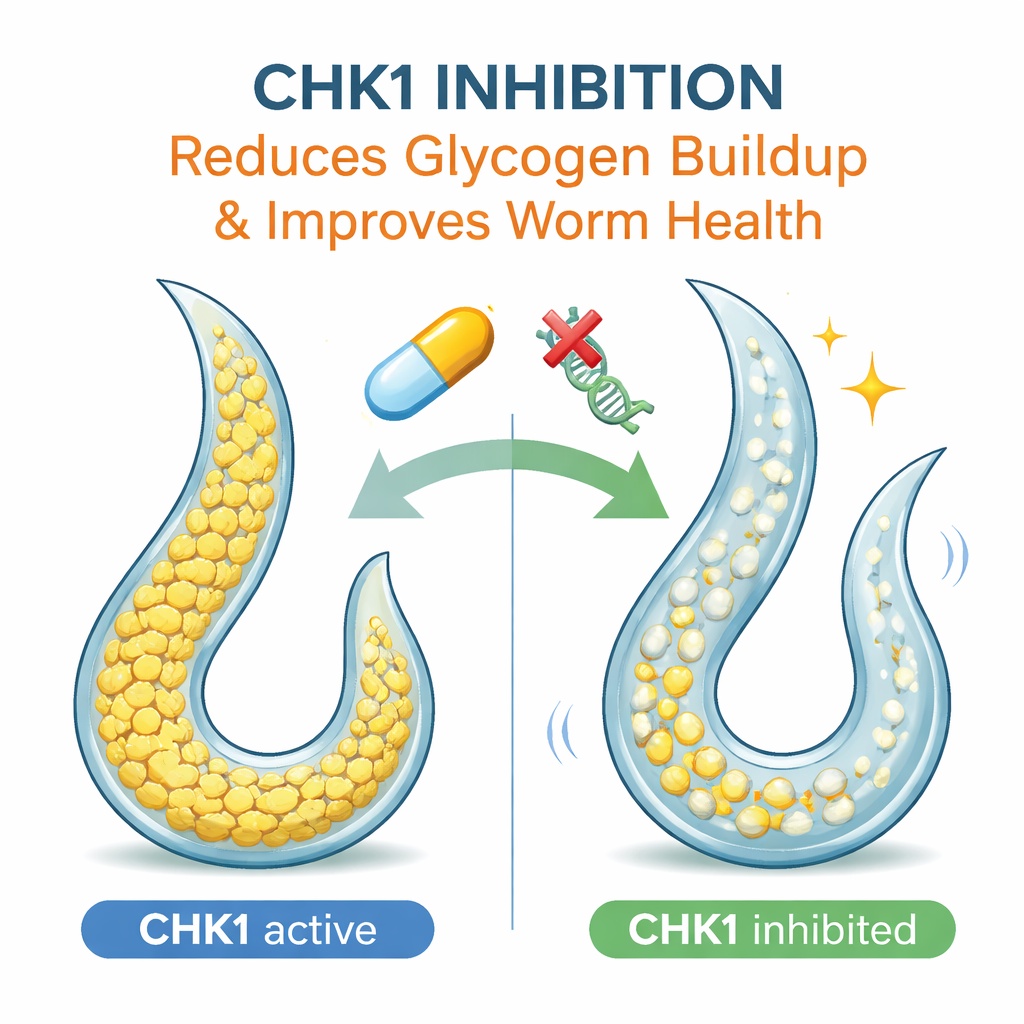
Was das für Patienten und weitere Forschung bedeutet
Die Studie zeigt, dass ein einfacher Wurm wesentliche Merkmale einer komplexen menschlichen Erkrankung zuverlässig nachbilden kann, einschließlich variantspezifischer Unterschiede in der Schwere. Mithilfe dieses Modells fanden die Forschenden Hinweise darauf, dass das Herunterregeln von CHK1, genetisch oder pharmakologisch, schädliche Glykogenansammlungen reduzieren und Gesundheitsparameter in den Würmern verbessern kann. Zwar sind diese Ergebnisse bisher auf C. elegans und eine bestimmte Mutation beschränkt, doch sie machen CHK1 zu einem vielversprechenden therapeutischen Ziel und veranschaulichen, wie die Kombination aus Tiermodellen, groß angelegten Wirkstoffscreenings und computergestützter Analyse unerwartete Strategien zur Behandlung seltener Stoffwechselerkrankungen aufdecken kann.
Zitation: Daghar, H., Pyman, B., Maios, C. et al. CHK1 inhibition rescues abnormal glycogen buildup in a Caenorhabditis elegans model for glycogen storage disease III. Commun Biol 9, 257 (2026). https://doi.org/10.1038/s42003-026-09535-9
Schlüsselwörter: Glykogenspeicherkrankheit, Caenorhabditis elegans, CHK1-Inhibitor, seltene Stoffwechselstörung, Arzneimittel-Neuzuordnung