Clear Sky Science · de
Fötale Reversion aus unterschiedlichen Abstammungen erhält den intestinalen Stammzellpool und verleiht Stressresistenz
Wie der Darm sich unter Beschuss heilt
Die Schleimhaut Ihres Darms ist eines der geschäftigsten Gewebe Ihres Körpers. Sie verdaut Nahrung, nimmt Nährstoffe auf und schützt vor Erregern – und erneuert sich dabei alle paar Tage. Dieses Papier untersucht, wie diese fragile Oberfläche harte Angriffe übersteht – von Entzündungen bis zu Chemotherapie – indem Zellen vorübergehend in einen fötalähnlicheren, flexibleren Zustand zurückversetzt werden, der dem Darm hilft, sich zu reparieren und Schäden zu widerstehen.
Die alltägliche Fließbandarbeit im Darm
In gesunden Därmen sitzt eine spezialisierte Zellgruppe, die sogenannten crypt base columnar cells (CBCs), am Grund winziger Vertiefungen, der Krypten. Diese stammdzellenähnlichen Zellen teilen sich ständig und schicken ihre Nachkommen nach oben zu den fingerartigen Zotten, die in das Darmlumen ragen. Auf dem Weg reifen die Zellen zu verschiedenen Funktionen heran, etwa zu absorptiven Enterozyten, die Nährstoffe aufnehmen, oder sekretorischen Zellen, die Schleim und antimikrobielle Substanzen produzieren. Unter normalen Bedingungen sorgt dieser Fluss von unten nach oben für die Erneuerung und Ordnung der Darmschleimhaut.
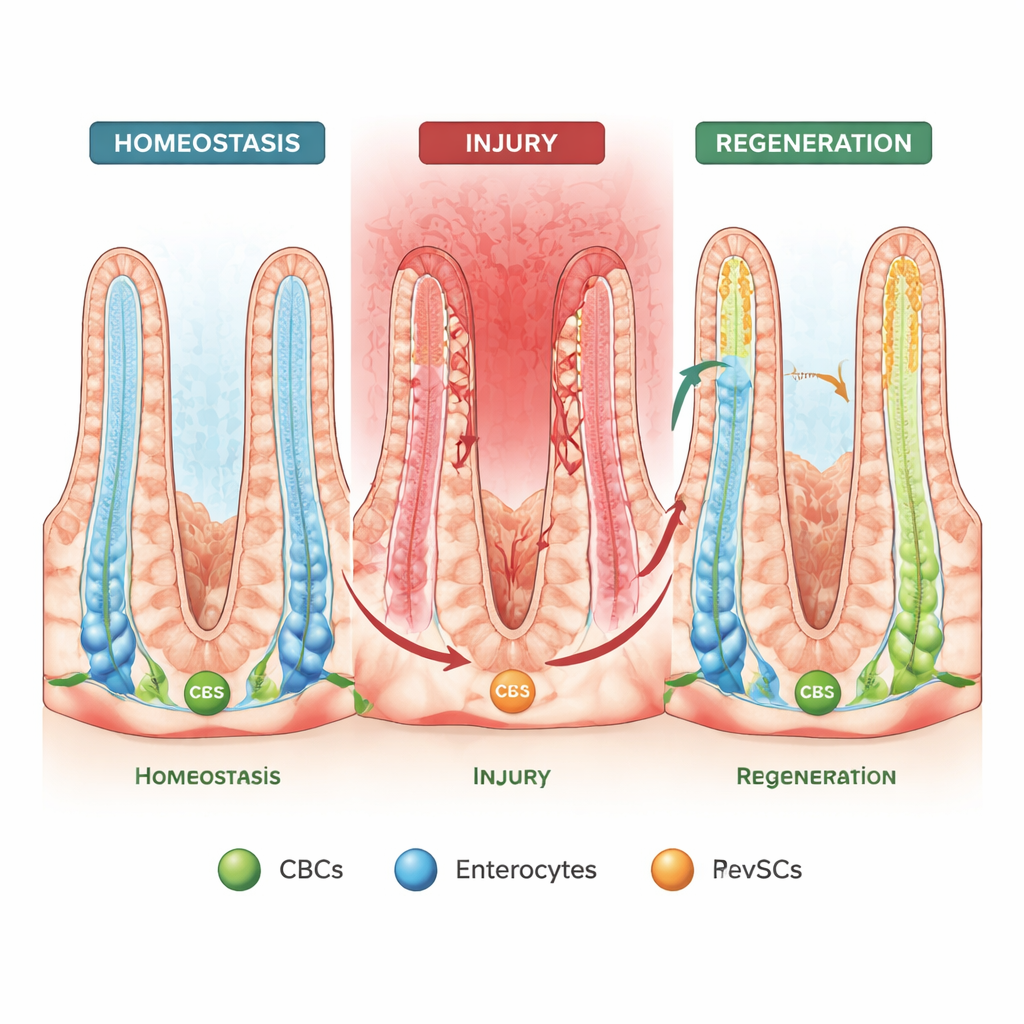
Zellen, die das Fließband rückwärts laufen können
Wenn die Darmschleimhaut verletzt ist und CBCs verloren gehen, zeigte frühere Arbeit, dass einige ausgereifte Zellen „den Weg zurück“ in die Krypten antreten und stammdzellenähnliche Fähigkeiten wiedererlangen können – ein Verhalten, das als räumliche Plastizität bezeichnet wird. Ein zweites, neueres Phänomen ist die „fötale Reversion“, bei der Zellen ein Genaktivitätsmuster annehmen, das dem sich entwickelnden Darm ähnelt. In dieser Studie verknüpfen die Autoren diese beiden Ideen mithilfe ausgefeilter Organoid-(Mini-Darm-)Kulturen, Einzelzell-RNA-Sequenzierung und Linienverfolgung in Mäusen. Sie identifizieren eine spezielle fötalähnliche Population, die sie revival stem cells (revSCs) nennen, die sowohl aus CBCs als auch aus gewöhnlichen absorptiven Enterozyten entstehen kann und dann ein vollständiges Set an Darmzelltypen regeneriert.
Mini-Därme enthüllen verborgene Flexibilität
Um diese Veränderungen in Aktion zu beobachten, züchtete das Team Maus- und humane Darmorganoide in zwei verschiedenen Gelen. In Matrigel verhielten sich Organoide wie normales erwachsenes Gewebe, reich an CBCs und ausgereiften Zelltypen. In einem Kollagen-Gel jedoch dominierten revSC-ähnliche Zellen mit einem fötalen Gen-Signatur. Einzelzellanalysen zeigten, dass revSCs entlang von zwei Hauptpfaden zurückverfolgt werden konnten: von klassischen CBCs und von absorptiven Enterozyten. Sortierexperimente bestätigten, dass CBCs die höchste Fähigkeit besitzen, in revSCs umzuwandeln, aber selbst reifere Zellen konnten dies tun, wenn sie in die richtige Umgebung gebracht wurden. Entscheidend war, dass gereinigte revSCs in Matrigel zurückversetzt werden konnten und dann CBCs und alle wichtigen intestinalen Linien regenerierten, was beweist, dass der fötalähnliche Zustand reversibel und voll funktionsfähig ist.
Zottenzellen und Verletzungen in der realen Welt
Die Studie geht einen Schritt weiter und fragt, ob diese Flexibilität auch außerhalb des Labors auftritt. Die Forscher markierten Enterozyten in den Zotten von Mäusen und kultivierten entweder Zottenfragmente oder setzten die Tiere einem darmtoxischen Chemotherapeutikum, 5‑Fluorouracil (5‑FU), aus. In Kollagen bildeten Zottenfragmente – die normalerweise als arm an Stammzellen gelten – neue Organoide, die revSC-Merkmale annahmen und später CBC-Marker wiedererlangten, wenn sie in Standardbedingungen zurückverlagert wurden. Bei Transplantation in Kolitis-Modelle bauten diese „zottenabgeleiteten“ Organoide eine gesunde Darmschleimhaut wieder auf. In lebenden Mäusen, die mit 5‑FU behandelt wurden, begannen markierte Enterozyten, revSC-Marker zu exprimieren und erschienen später als lange klonale Streifen, die neue CBCs an der Kryptenbasis einschlossen, was bestätigte, dass ausgereifte Zellen eingesprungen waren, um den Stammzellpool aufzufüllen.
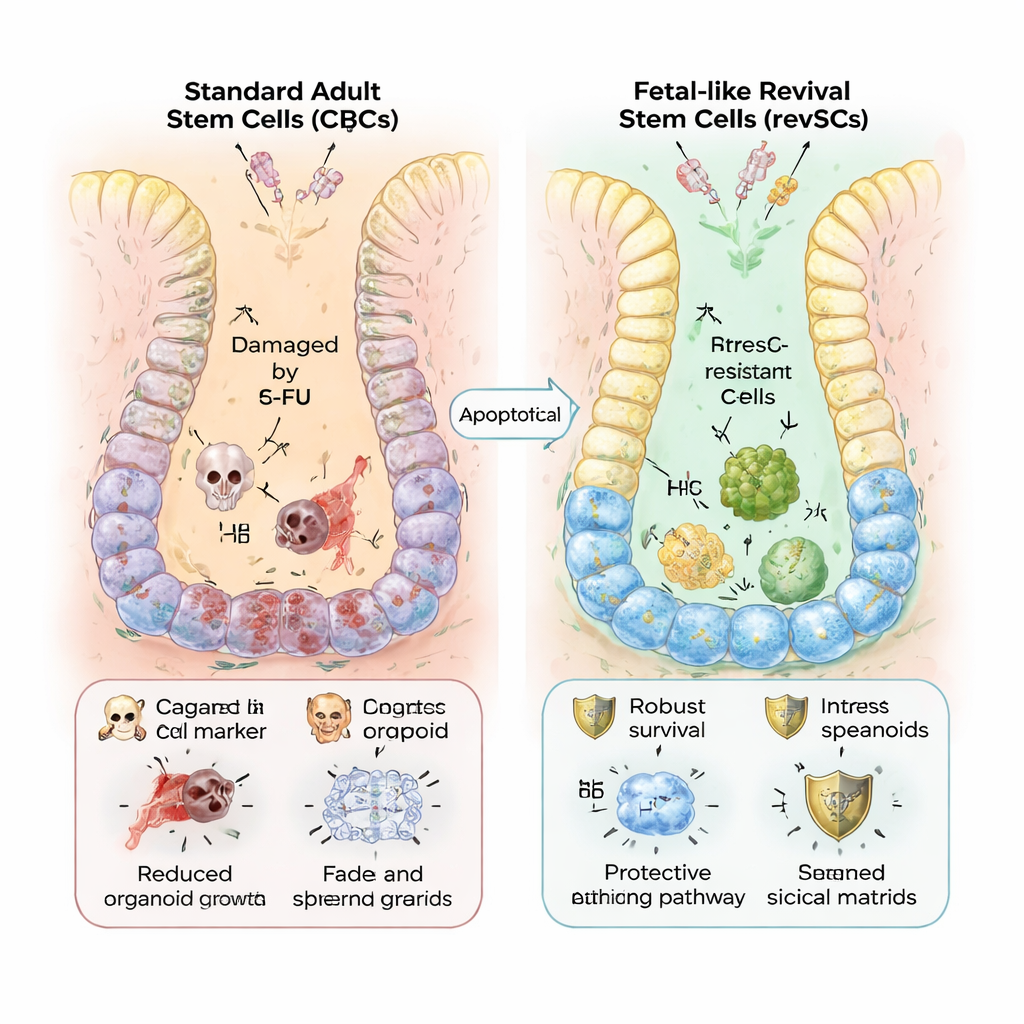
Stressresistente Reparaturtruppen
Warum diese fötalähnliche Umleitung? Die Autoren zeigen, dass revSCs dem Stress deutlich besser standhalten. Wenn Organoide mit 5‑FU konfrontiert wurden, schrumpften jene in Standard-Matrigel und zeigten breit angelegte Genprogramme, die mit DNA‑Schäden und hektischer Proliferation verknüpft sind. Kollagengezüchtete, revSC-reiche Organoide dagegen wuchsen weiter und zeigten eine ruhigere, gezieltere Reaktion. Genanalysen enthüllten eine höhere Aktivität von Antioxidanzsystemen, Anti‑Todes‑Proteinen und Hitzeschock‑Chaperonen – molekulare Schilde, die Zellen helfen, Entzündungen und toxische Schäden zu überstehen. Ähnliche Muster wurden sowohl in Maus- als auch in Humanzellen beobachtet, und dieselben revSC‑Gene sind in entzündeten menschlichen Därmen erhöht.
Was das für Darmkrankheiten und Therapie bedeutet
Für Nichtfachleute lautet die Schlussfolgerung, dass die Darmschleimhaut einen eingebauten Notfallplan besitzt. Wenn Entzündungen oder Medikamente die üblichen Stammzellen bedrohen, können sowohl Stammzellen als auch gewöhnliche absorptive Zellen vorübergehend in einen fötalähnlichen, stressresistenten revSC‑Zustand zurückkehren. Von dort aus können sie das normale Stammzellkompartiment neu erschaffen und das Gewebe wiederaufbauen. Diese Arbeit vereint zwei Regenerationskonzepte – räumliche Plastizität und fötale Reversion – zu einer einzigen Reparaturhierarchie und deutet darauf hin, dass das kontrollierte Nutzen dieses flexiblen, fötalähnlichen Programms Therapien für Erkrankungen wie entzündliche Darmerkrankungen und kolorektalen Krebs verbessern könnte, warnt aber auch davor, dass fehlgesteuerte Reversion das Tumorwachstum fördern kann.
Zitation: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
Schlüsselwörter: intestinale Stammzellen, Geweberegeneration, Zellplastizität, entzündliche Darmerkrankung, Organoide