Clear Sky Science · de
Fluvastatin unterdrückt die Entstehung und das Fortschreiten von Brustkrebs durch Zielgerichtetheit auf CYP4Z1
Warum ein Cholesterinmedikament für Brustkrebs wichtig sein könnte
Viele Frauen, die wegen Brustkrebs behandelt werden, entwickeln abnorme Blutfettwerte und stehen weiterhin vor der Gefahr eines Rückfalls oder einer Metastasierung. Diese Studie untersucht eine interessante Idee: Könnte eine gängige cholesterinsenkende Tablette, Fluvastatin, umfunktioniert werden, um Brustkrebs zu verlangsamen oder zu verhindern, indem sie ein Protein außer Gefecht setzt, das besonders gefährliche, stammzellähnliche Tumorzellen antreibt?
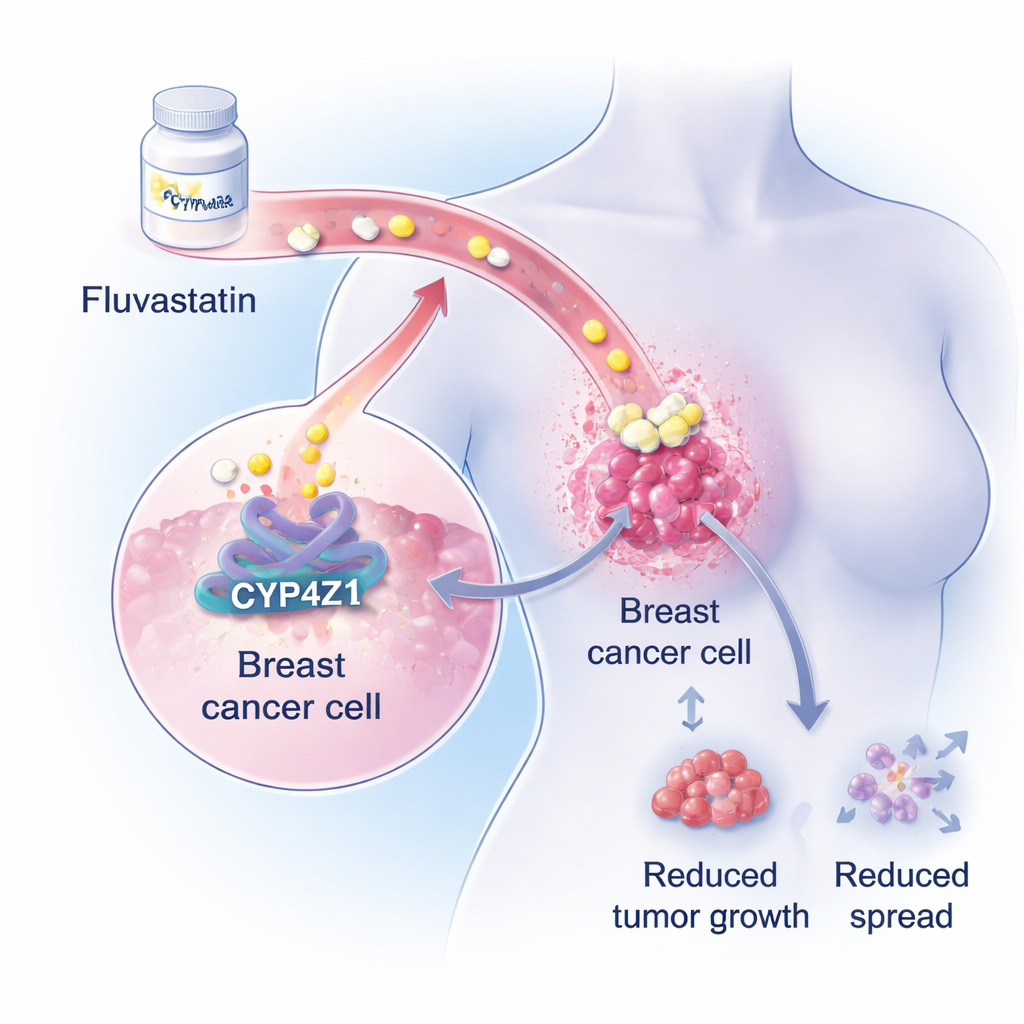
Ein versteckter Treiber in Brusttumoren
Die Forschenden konzentrieren sich auf ein wenig bekanntes Protein namens CYP4Z1, das in Brustkrebszellen stark erhöht vorkommt, in gesundem Brustgewebe jedoch nicht. Frühere Arbeiten zeigten, dass CYP4Z1 Krebszellen stammzellähnlicher machen kann – Zellen, die sich endlos selbst erneuern, Chemotherapien widerstehen und Tumoren nach der Behandlung neu starten können. In umfangreichen genetischen und biochemischen Analysen zeigt das Team nun, dass überaktives CYP4Z1 die fettsynthetischen Wege in Brustkrebszellen kräftig anheizt, insbesondere die Produktion von Triglyceriden, einem wichtigen Speicherfett. Da viele Brustkrebspatientinnen bereits während der Chemotherapie gestörte Blutfettwerte entwickeln, deutete diese fettfördernde Rolle von CYP4Z1 auf eine Möglichkeit für vorhandene lipidsenkende Medikamente hin.
Fluvastatin von der Herzgesundheit zur Krebsbehandlung umnutzen
Um diese Idee zu testen, screente das Forscherteam eine kleine Bibliothek von 23 von der FDA zugelassenen Arzneimitteln zur Senkung der Blutfette. Fluvastatin, eine weit verbreitete Statin-Tablette gegen hohen Cholesterinspiegel, erwies sich als besonders wirksam: Es blockierte direkt die Enzymaktivität von CYP4Z1 in dosisabhängiger Weise. Bei Dosen, die normale Brustzellen deutlich weniger schädigten als Krebszellen, reduzierte Fluvastatin stark wichtige Marker der Stammzelligkeit, die Fähigkeit von Brustkrebszellen, frei schwebende „Tumorkugeln“ zu bilden, sowie ihre Wanderungs- und Invasionsfähigkeit durch gewebeähnliche Barrieren in Labortests. Zudem machte es Tumorzellen empfindlicher gegenüber dem Chemotherapeutikum Adriamycin, was darauf hindeutet, dass es bestehende Behandlungen verstärken könnte.
Erprobung des Medikaments in lebenden Tieren
Das Team bewertete Fluvastatin anschließend in Mausmodellen. Bei Mäusen, die mit menschlichen Brustkrebszellen transplantiert waren, verlangsamte eine periodische Fluvastatinbehandlung das Tumorwachstum, senkte die Tumorwerte des Stammzellmarkers ALDH1A1 und des Zellteilungsmarkers Ki67 und reduzierte die Anzahl metastatischer Knötchen in der Lunge. Wichtig war, dass die mit Fluvastatin behandelten Mäuse ihr Körpergewicht hielten und keine größeren Blut- oder Knochenmarkveränderungen zeigten, was bei der getesteten Dosis ein günstiges Sicherheitsprofil stützt. In einem realistischeren genetischen Modell – Mäuse, die so verändert wurden, dass sie durch ein krebsverursachendes Gen Brusttumoren entwickeln – brachten die Forschenden zusätzlich menschliches CYP4Z1 in das Brustdrüsengewebe ein. Diese Mäuse entwickelten mehr präkanzeröse und kanzeröse Läsionen sowie mehr Leber- und Lungenmetastasen als Kontrolltiere. Die Fluvastatinbehandlung reduzierte sowohl die Zahl der Mammaläsionen als auch der Fernmetastasen deutlich, besonders bei Mäusen mit dem zusätzlichen CYP4Z1-Gen.
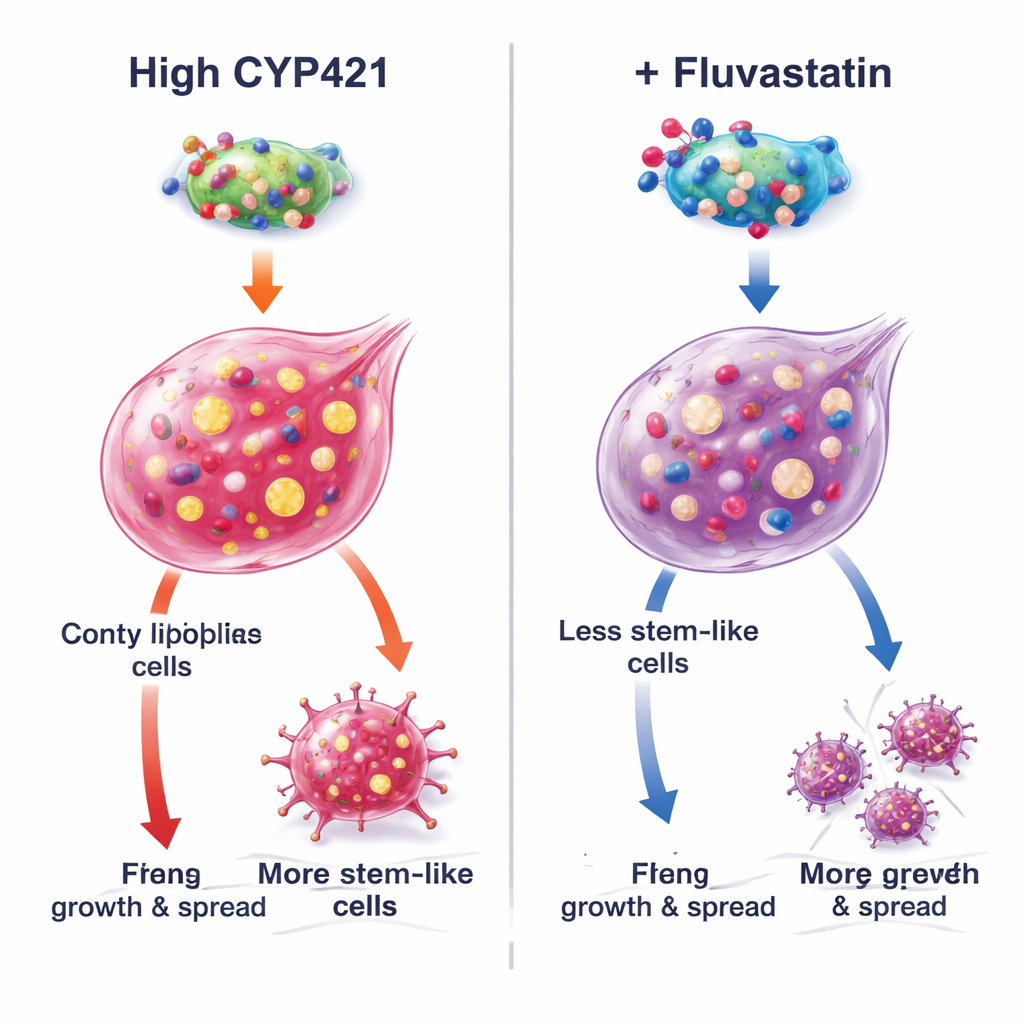
Wie Fluvastatin ein krebsförderndes Protein außer Kraft setzt
Um den Wirkmechanismus zu verstehen, kombinierten die Autorinnen und Autoren Computermodellierung mit präziser Proteinmanipulation. Sie sagten voraus, dass Fluvastatin sich in die aktive Stelle von CYP4Z1 einfügt und dort an drei kritischen Aminosäuren (Lys109, Pro444 und Arg450) andockt. Werden diese Stellen mutiert, fällt die Aktivität von CYP4Z1 ab und Fluvastatin kann es nicht weiter hemmen, was diese Positionen als Andockpunkte bestätigt. In Zellen, die natürlicherweise kein CYP4Z1 exprimieren, erhöhte die Einführung des normalen Proteins die Stammzelligkeit und aktivierte das wachstumsfördernde PI3K/AKT-Signal, während Fluvastatin diese Effekte umkehrte. Mutante Versionen von CYP4Z1 waren weniger wirksam und weniger ansprechbar auf das Medikament. Weitere Experimente zeigten, dass die Wirkung von Fluvastatin nachließ, wenn die Triglyceridproduktion künstlich erhöht wurde oder CYP4Z1 herunterreguliert wurde, was unterstreicht, dass die stärksten Effekte des Medikaments aus der Blockade dieses spezifischen Proteins und seiner fettaufbauenden Folgen resultieren und nicht primär aus der Auslösung von Zelltod durch eisenabhängige „Ferroptose“.
Was das für Patientinnen bedeutet
Insgesamt legt die Studie nahe, dass Fluvastatin über die Cholesterinsenkung hinaus in experimentellen Modellen die frühesten Stadien und die spätere Ausbreitung von Brustkrebs eindämmen kann, indem es CYP4Z1 ins Visier nimmt – ein Protein, das den Fettstoffwechsel und stammzellähnliches Verhalten in Tumoren antreibt. Da Fluvastatin bereits zugelassen ist und sein Sicherheitsprofil gut bekannt ist, eröffnen diese Befunde einen vielversprechenden Weg für schnellere klinische Tests als Zusatztherapie, insbesondere bei Patientinnen, deren Tumoren CYP4Z1 stark exprimieren. Zwar sind weitere Arbeiten nötig, um diesen Ansatz am Menschen zu prüfen und mögliche zusätzliche Ziele des Medikaments zu identifizieren, doch die Forschung öffnet die Tür, ein vertrautes Herzmedikament als Teil einer neuen Strategie gegen aggressive, rückfallanfällige Brustkrebserkrankungen zu nutzen.
Zitation: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Schlüsselwörter: Brustkrebs, Fluvastatin, Krebsstammzellen, Lipidstoffwechsel, Neuzuweisung von Arzneimitteln