Clear Sky Science · de
Different exprimierte miRNAs im Temporallappen von Alzheimer-Patienten und ihr Zusammenhang mit Tau-Pathologie
Warum winzige Schalter im Gehirn bei Alzheimer eine Rolle spielen
Die Alzheimer-Krankheit raubt Menschen schrittweise Erinnerung und Selbstständigkeit, doch Behandlungen, die die Krankheit aufhalten oder umkehren, fehlen weiterhin. Diese Studie untersucht einige der kleinsten Kontrollschalter im Gehirn – kurze RNA-Moleküle, sogenannte microRNAs –, die mitentscheiden, welche Proteine Zellen produzieren. Anhand von Hirngewebe verstorbener Alzheimer-Patienten fragten die Forschenden, ob Veränderungen dieser microRNAs mit einem zentralen Krankheitsmerkmal verbunden sind: der Anreicherung und Ausbreitung abnormaler Tau-Proteine innerhalb von Nervenzellen.
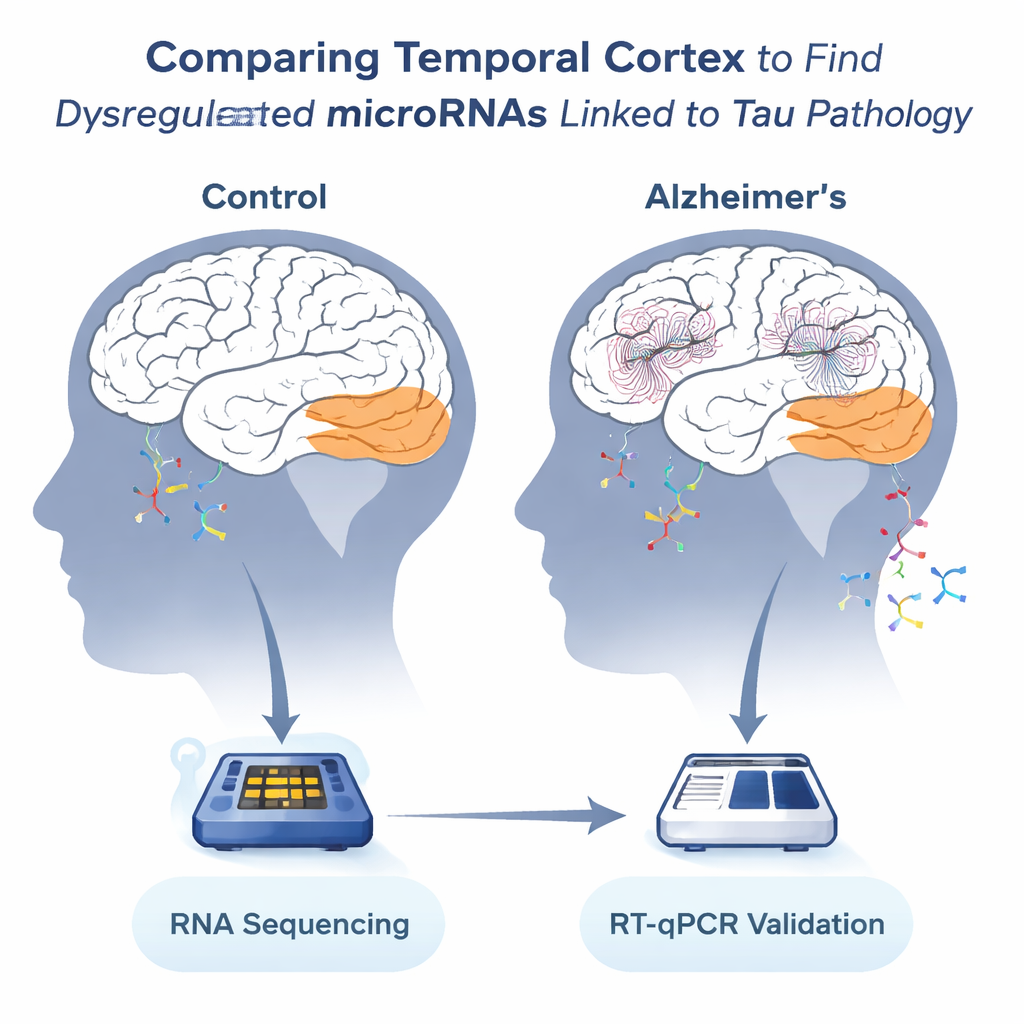
Nachrichten in einer besonders verletzlichen Hirnregion untersuchen
Das Team konzentrierte sich auf den Temporallappen, eine Region, die für Sprache und Gedächtnis wichtig ist und bei Alzheimer stark betroffen ist. Nach dem Tod wurden Proben von 36 Personen – 13 ohne Alzheimer und 23 mit der Erkrankung – aus zwei europäischen Hirnbanken entnommen. Die Wissenschaftler isolierten RNA aus diesem Gewebe und verwendeten Hochdurchsatz-Sequenzierung, um Hunderte verschiedener microRNAs zu quantifizieren. Da Hirngewebe nach dem Tod degradiert, prüften sie sorgfältig die RNA-Qualität und wählten 19 Proben mit akzeptabler Integrität für die detaillierteste Analyse aus; alle 36 Proben wurden dann zur Bestätigung der Hauptbefunde herangezogen.
Eine microRNA-Signatur von Alzheimer entdecken
Unter 449 detektierten microRNAs fielen 13 durch konsistente Veränderungen im Temporallappen von Alzheimer-Patienten auf. Acht waren reduziert und fünf erhöht im Vergleich zu Kontrollgehirnen. Mehrere der stärksten Signale betrafen microRNAs, die bereits im Zusammenhang mit Alzheimer vermutet wurden: miR-129-5p, miR-132-3p und miR-146b-5p waren alle niedriger, während miR-151a-5p erhöht war. Diese Moleküle sind im Gehirn reichlich vorhanden und bekannt dafür, Netzwerke von Genen zu regulieren, die an neuronaler Gesundheit beteiligt sind. Mit einer zweiten, gezielten Methode (RT-qPCR) bestätigten die Autoren, dass dieselben microRNAs in dieselbe Richtung verändert waren, selbst wenn schlechtere Proben eingeschlossen wurden, was die Zuverlässigkeit des Musters stärkt.
Winzige Schalter mit zunehmender Tau-Vernetzung verknüpfen
Das Ausmaß der Alzheimer-Schädigung im Gehirn wird häufig nach dem Braak-Stadium bewertet, das widerspiegelt, wie weit Tau-Fibrillen sich in verschiedenen Regionen ausgebreitet haben. Die Forschenden stellten fest, dass die Werte von miR-129-5p, miR-132-3p und miR-146b-5p mit zunehmendem Braak-Stadium kontinuierlich abnahmen, während miR-151a-5p tendenziell anstieg. Sie maßen außerdem direkt eine stark phosphorylierte, fibrillenbildende Form von Tau in denselben Proben. Gehirne mit mehr dieses abnormalen Tau zeigten dasselbe Muster: weniger miR-129-5p, miR-132-3p und miR-146b-5p und mehr miR-151a-5p. Anders gesagt: Die microRNA-Veränderungen korrelierten sowohl mit der mikroskopischen Stadieneinteilung als auch mit biochemischen Zeichen der Tau-Pathologie, was darauf hindeutet, dass sie eng mit dem Krankheitsprozess verbunden sind und nicht nur zufällige Nebenerscheinungen.
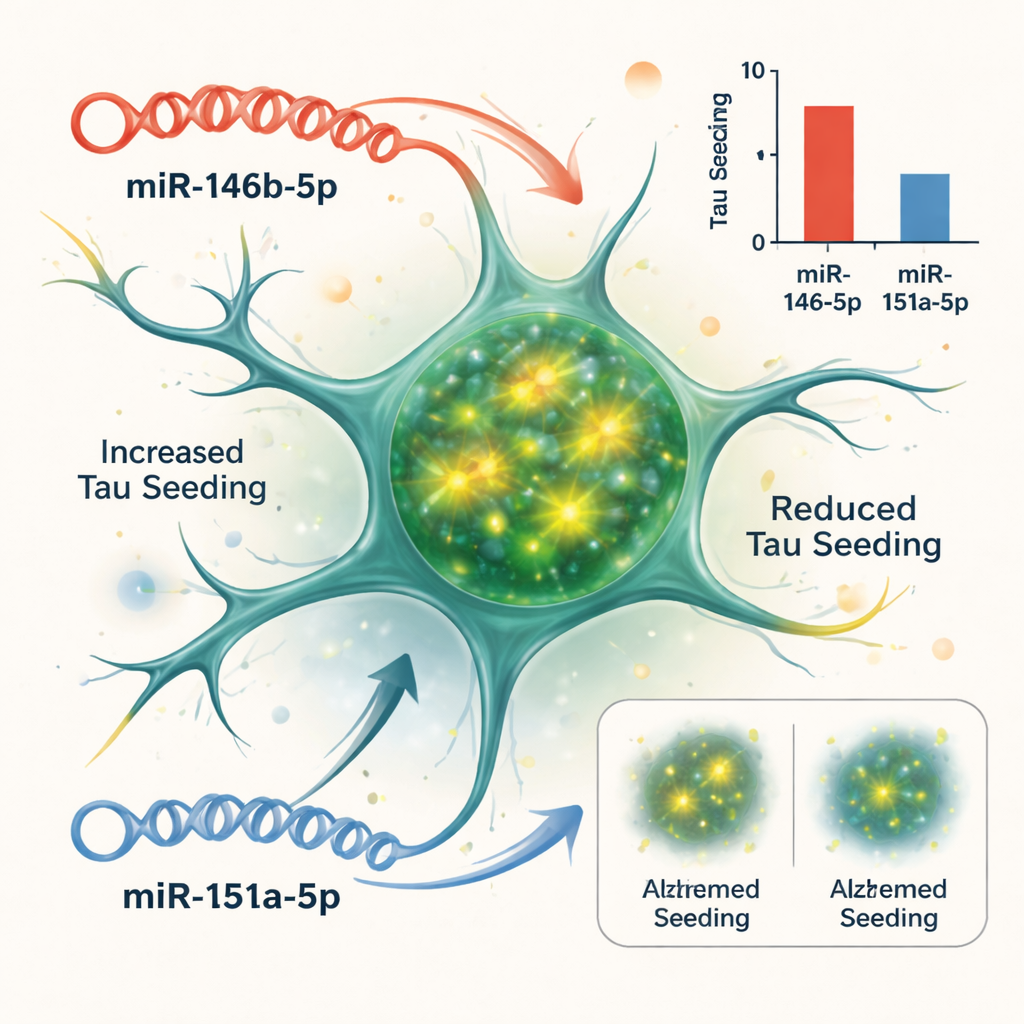
Ursache und Wirkung in einem Zellmodell testen
Korrelation beweist nicht, dass microRNAs die Krankheit antreiben, daher nutzte das Team ein zellbasiertes System, das anzeigt, wie leicht Tau zu neuen Aggregaten „seeden“ kann. Sie verwendeten Biosensor-Zellen, die aufleuchten, wenn sich Tau-Fasern in ihnen bilden. Wenn sie tau-reiches Material aus Alzheimer-Gehirnen hinzufügten, erzeugten die Zellen ein starkes Fluoreszenzsignal. Durch das Erhöhen oder Blockieren bestimmter microRNAs in diesen Zellen konnten die Forschenden erkennen, welche den Tau-Seeding-Prozess beeinflussen. Zwei stachen hervor: Die Erhöhung von miR-146b-5p verschlechterte das Tau-Seeding, während seine Hemmung das Seeding reduzierte; im Gegensatz dazu dämpfte die Erhöhung von miR-151a-5p das Tau-Seeding, während seine Hemmung das Seeding verstärkte. Andere getestete microRNAs zeigten in diesem Test kaum Wirkung.
Was das für künftige Diagnose und Therapie bedeuten könnte
Um besser zu verstehen, was diese microRNAs bewirken könnten, nutzten die Autoren Rechenwerkzeuge, um ihre vorhergesagten Genziele auf bekannte biologische Signalwege abzubilden. Die herunterregulierten microRNAs – insbesondere miR-129-5p, miR-132-3p und miR-146b-5p – waren mit Netzwerken verbunden, die an Überleben von Nervenzellen, chemischer Signalübertragung an Synapsen und Alzheimer-assoziierten Pfaden beteiligt sind. Das legt nahe, dass der Verlust ihrer normalen „Brems“-Funktion mehrere schützende Systeme gleichzeitig stören könnte, während der Anstieg von miR-151a-5p eine späte, teilweise Reaktion des Gehirns darstellen könnte, die versucht, Tau-Aggregation entgegenzuwirken. Obwohl diese Arbeit auf postmortalem Gewebe und vereinfachten Zellmodellen beruht, stärkt sie die Idee, dass spezifische microRNAs sowohl Tau-Pathologie widerspiegeln als auch modulieren. Langfristig könnte das Messen dieser Moleküle in Liquor oder Blut helfen, den Krankheitsverlauf zu verfolgen, und ein gezieltes Anpassen ihrer Konzentrationen im Gehirn könnte einen neuen Weg bieten, die Ausbreitung von toxischem Tau zu verlangsamen oder zu verhindern.
Zitation: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Schlüsselwörter: Alzheimer-Krankheit, microRNA, Tau-Pathologie, Temporallappen, Neurodegeneration