Clear Sky Science · de
Zielgerichtete Blockade des Spleißens kann intron‑eingebettete primäre microRNAs dysregulieren
Verborgene Botschaften in unseren Genen
Viele neue Gentherapien wirken, indem sie die RNA‑Botschaften unserer Zellen lenken, doch diese RNAs verbergen oft zusätzliche „Randnotizen“, deren Bedeutung die Forschung erst langsam erfasst. Diese Arbeit zeigt, dass Wirkstoffe, die fehlerhaftes Spleißen korrigieren sollen, unbeabsichtigt winzige regulatorische RNAs hochregulieren können, die in Introns – den nicht codierenden Abschnitten zwischen Genabschnitten – verborgen sind. Das kann überraschende Auswirkungen auf die Verschaltung des Gehirns und die Entwicklung haben.
Gentherapien, die RNA umschreiben
Antisense‑Oligonukleotide (ASOs) sind kurze synthetische DNA‑ oder RNA‑ähnliche Moleküle, die an RNA binden und deren Ablese‑ oder Verarbeitungsweise verändern. Mehrere ASOs werden bereits für seltene Erbkrankheiten erprobt oder eingesetzt, vor allem bei Krankheiten, die durch fehlerhaftes RNA‑Spleißen entstehen – dem Schritt, der die codierenden Genabschnitte zusammenfügt. Die meisten Sicherheitstests prüfen vor allem, ob ein ASO das richtige Protein wiederherstellt und offensichtliche Nebenwirkungen vermeidet. Viele Gene enthalten jedoch auch nicht‑kodierende RNAs, darunter microRNAs, in ihren Introns. Diese winzigen Moleküle können die Genaktivität stark modulieren; bis zu die Hälfte der bekannten microRNAs bei Wirbeltieren stammt aus Introns. Die neue Studie fragt: Was passiert mit diesen eingebetteten microRNAs, wenn wir mit ASOs gezielt das Spleißen verändern?
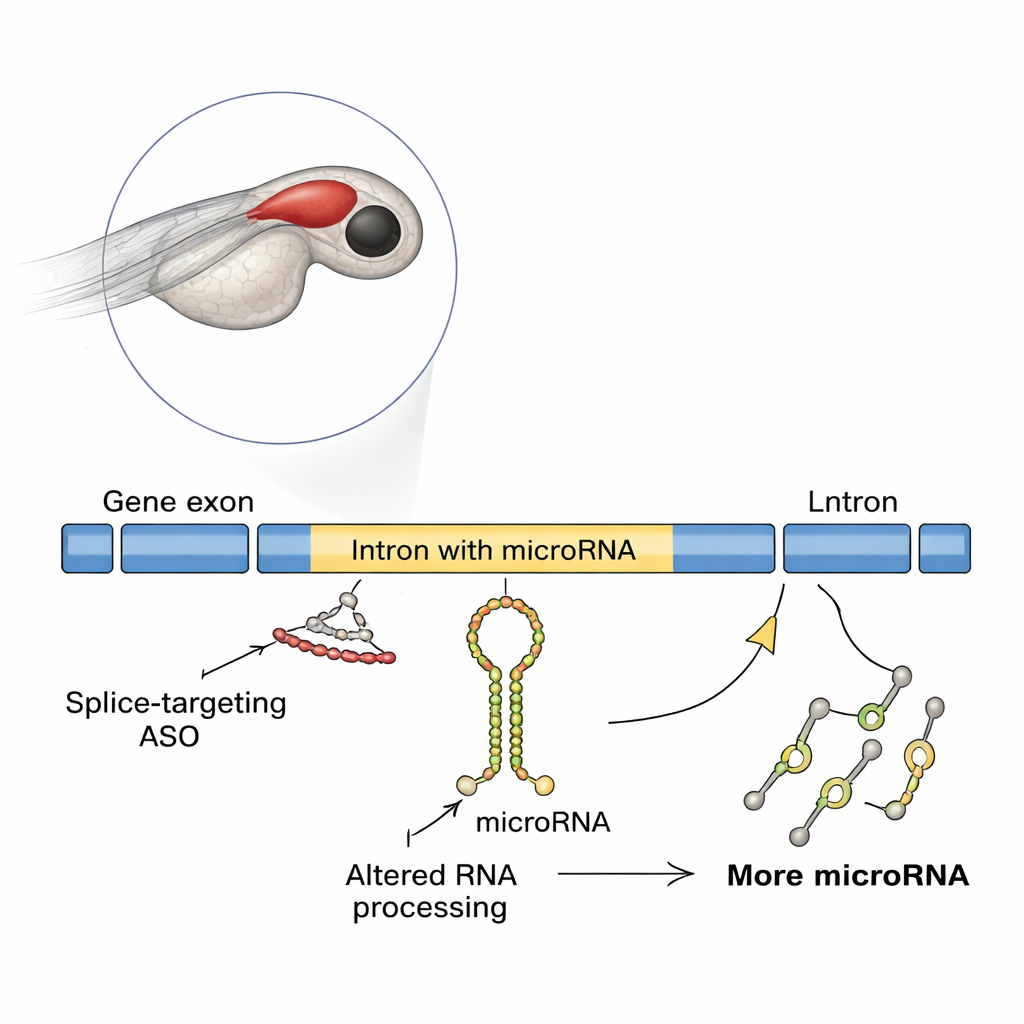
Ein überraschender Effekt im sich entwickelnden Fischgehirn
Die Forschenden nutzten Zebrafische, ein populäres Wirbeltier‑Modell, dessen transparente Embryonen die Nachverfolgung der Gehirnentwicklung erleichtern. Sie konzentrierten sich auf ein Gen namens slit3, das die Führung von Nervenfasern unterstützt und in einem seiner Introns eine microRNA namens mir-218a-1 enthält. Wenn das Team den Beginn der slit3‑Translation blockierte, sah die Entwicklung der hormonausschüttenden Hypophysenaxone normal aus. Blockierte dagegen ein anderes ASO ein bestimmtes slit3‑Spleißstelle, waren die Axone, die normalerweise zur hinteren Hypophyse ziehen, deutlich reduziert, obwohl die Zahl der Oxytocin‑produzierenden Neurone unverändert blieb. Molekulare Tests zeigten, dass dieses Spleiß‑blockierende ASO zur Introns‑Retention in der Gen‑RNA führte und unerwartet die Mengen des slit3‑Transkripts, seines langen Introns und des intron‑eingebetteten primären mir-218a-1‑Transkripts erhöhte.
MicroRNA, nicht Proteinverlust, verursacht die Fehlbildungen
Um die Ursache des axonalen Problems zu klären, verglichen die Autorinnen und Autoren mehrere Szenarien. Die alleinige Blockade der reifen mir-218a-1 veränderte die slit3‑Spiegel nicht, und ein separates ASO, das eine andere Spleißstelle nahe der microRNA anvisierte, erzeugte weder axonale Defekte noch erhöhte mir-218a-1. Entscheidenderweise erholte sich die axonale Verschaltung weitgehend, wenn das spleißblockierende slit3‑ASO zusammen mit einem ASO verabreicht wurde, das mir-218a-1 neutralisiert. Ebenso verursachte das gleiche spleißblockierende slit3‑ASO in Zebrafischen, die genetisch ohne mir-218a-1 waren, keine axonalen Defekte mehr, während die Injektion eines synthetischen mir-218a‑Mimetikums den Phänotyp in normalen Fischen nachahmen konnte. Diese Experimente deuten darauf hin, dass erhöhte intronische microRNA‑Aktivität – und nicht ein verkürztes Slit3‑Protein – der Haupttreiber der Entwicklungsstörung ist.
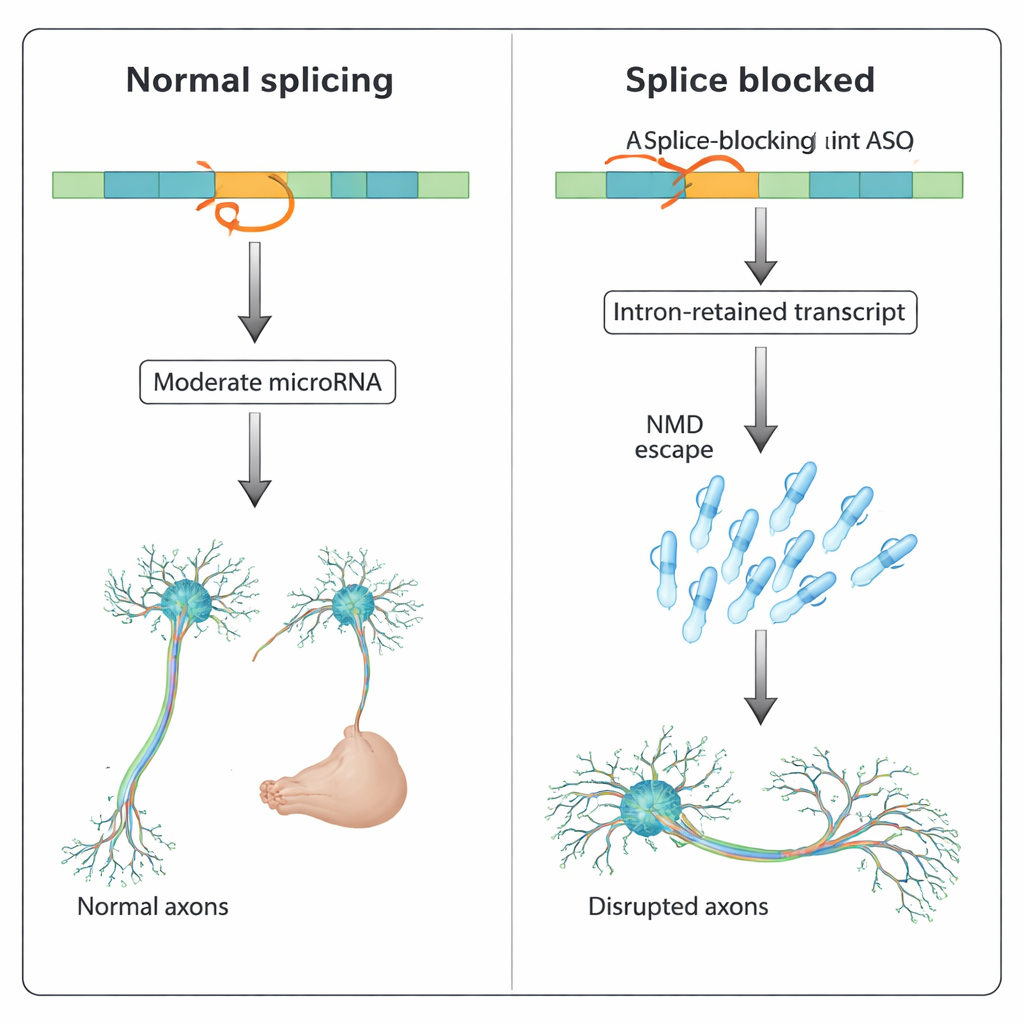
Ein weiter verbreitetes Muster über mehrere Gene hinweg
Das Team untersuchte anschließend, ob dieser Effekt einzigartig für slit3 ist. Sie durchsuchten das Zebrafisch‑Genom und fanden Dutzende proteinkodierender Gene, die intronische microRNAs beherbergen, viele davon in Entwicklungs‑ und Signalkaskaden beteiligt. Zwei solcher Gene, pank2 und dnm2a, zeigten zuvor schwere Entwicklungsstörungen, wenn ihr Spleißen durch ASOs blockiert wurde – darunter Hirn‑Flüssigkeitsansammlungen, Herzschwellungen und Körperdeformationen – Probleme, die genetische Knockouts derselben Gene nicht reproduzierten. In dieser Studie konnte das Ko‑Injizieren von ASOs, die gezielt die intronischen microRNAs mir-103 (in pank2) bzw. mir-199-5p (in dnm2a) blockierten, diese ASO‑induzierten Phänotypen teilweise retten. In einigen Fällen stellte die microRNA‑Blockade auch die Expression des Wirtsgens wieder her, in anderen nicht, was darauf hindeutet, dass erhöhte microRNA‑Aktivität selbst schädlich sein kann, sogar wenn sich die Gesamtniveaus nur mäßig verändern.
Was das für künftige Behandlungen bedeutet
Die Ergebnisse zeigen, dass spleißzielende ASOs mehr bewirken können als Exon‑Skipping oder Introns‑Retention: Sie können intron‑verbleibende Transkripte stabilisieren, die dem zellulären Qualitätskontrollsystem entgehen, und so primäre intronische microRNAs erhöhen, die dann Netzwerke von Zielgenen fehlregulieren. In sich entwickelnden Neuronen kann eine derartige ungebremste microRNA‑Aktivität das Axonwachstum und die Konnektivität verzerren. Für Wirkstoffentwickler bedeutet das: Ungewöhnliche oder „off‑target“‑Phänotypen in Tierstudien müssen nicht immer von generischen Toxizitätswegen wie der p53‑Aktivierung herrühren, sondern können durch unbeabsichtigte Effekte auf verborgene intronische RNAs ausgelöst werden. Ein sorgfältiger Vergleich von translationsblockierenden und spleißblockierenden ASOs sowie die Überwachung intronischer microRNA‑Expression könnte helfen, diese Risiken frühzeitig zu erkennen und ASO‑Designs zu verfeinern, bevor sie Patienten erreichen.
Zitation: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Schlüsselwörter: Antisense‑Oligonukleotide, microRNA, RNA‑Spleißen, Zebrafisch‑Entwicklung, Sicherheit von Gentherapien