Clear Sky Science · de
Umfassendes Stoffwechselprofil über fünf Lebensphasen im murinen Hippocampus und Kortex zeigt geschlechtsbezogene Unterschiede beim altersbedingten kognitiven Abbau
Warum die Gehirnalterung bei Frauen und Männern unterschiedlich verläuft
Viele Familien bemerken, dass Gedächtnisprobleme und Demenz, wie die Alzheimer-Krankheit, bei Frauen häufiger auftreten als bei Männern. Diese Studie stellt eine einfache, aber wichtige Frage: Verbraucht das alternende Gehirn von Weibchen und Männchen seine „Brennstoffe" unterschiedlich, auf eine Weise, die diese Lücke erklären könnte? Indem die Forschenden verfolgen, wie Mäusehirne über die gesamte Lebensspanne Zucker und andere kleine Moleküle nutzen, entdecken sie geschlechtsspezifische Muster, die dazu beitragen könnten, warum ältere Weibchen anfälliger für kognitiven Abbau sind.
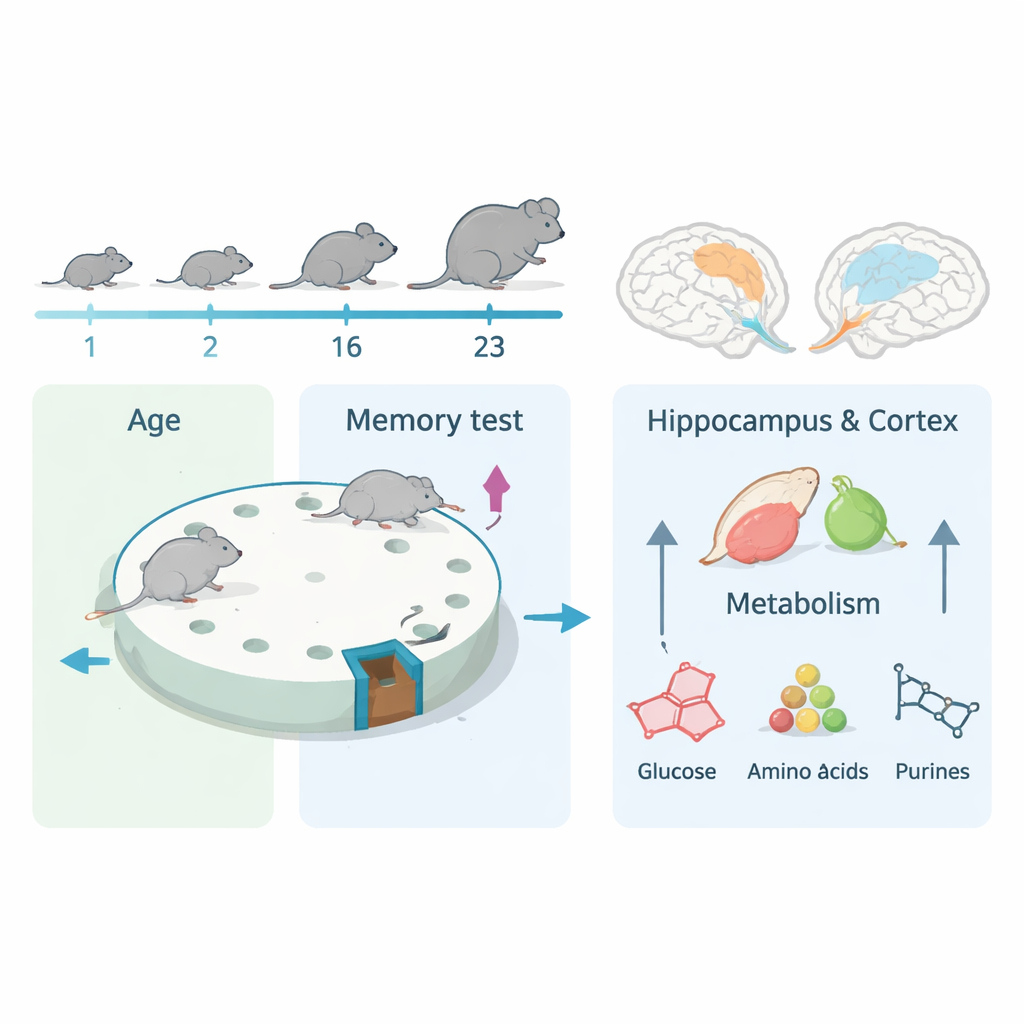
Gedächtnis verfolgen von Jugend bis ins hohe Alter
Um Gehirnchemie mit Verhalten zu verknüpfen, bestimmte das Team zuerst die Gedächtnisleistung von männlichen und weiblichen Mäusen in fünf Lebensphasen, von einem Monat (etwa Kindheit) bis 23 Monaten (hohes Alter). Mit dem Barnes-Maze, einer kreisförmigen Plattform, auf der Mäuse sich die Position einer verborgenen Fluchtbox merken müssen, stellten sie fest, dass beide Geschlechter bis 16 Monate deutliche Gedächtnisprobleme zeigten. Bis 23 Monate jedoch schnitten Weibchen deutlich schlechter ab als Männchen und benötigten länger, um den Fluchtweg zu finden. Wichtig ist, dass Unterschiede in der Gehgeschwindigkeit diese Ergebnisse nicht vollständig erklärten, was darauf hindeutet, dass der Abbau tatsächlich kognitiv und nicht nur durch langsamere Bewegung bedingt war.
Wie das alternde Gehirn seinen Zucker verbraucht
Das Gehirn lebt hauptsächlich von Glukose, einer Zuckerform. Um genau zu sehen, wie dieser Brennstoff genutzt wird, injizierten die Forschenden Mäusen eine markierte Form von Glukose, die sie beim Durchlaufen der chemischen Stoffwechselwege des Gehirns verfolgen konnten. Sie konzentrierten sich auf Hippocampus und Kortex, Regionen, die für Lernen und Gedächtnis entscheidend sind. Bei beiden Geschlechtern und in allen Altersstufen wurde Glukose schnell abgebaut und floss durch drei Hauptwege: eine schnelle Energiegewinnungskette, einen Weg, der hilft, oxidativen Stress zu bewältigen und DNA-Bausteine zu bilden, sowie den tieferen „Kraftwerks“-Kreislauf, der die meiste Energie gewinnt. Die markierten Produkte stiegen innerhalb einer halben Stunde an und schwanden bis 2,5 Stunden, was zeigt, dass die Zuckernutzung im Gehirn lebenslang schnell und dynamisch ist.
Unterschiedliche Brennstoffstrategien in weiblichen und männlichen Gehirnen
Obwohl beide Geschlechter dieselben grundlegenden Wege nutzten, änderten sich ihre Strategien mit dem Alter unterschiedlich. Junge Weibchen hatten eine insgesamt geringere Glukosedurchströmung als Männchen, leiteten aber verhältnismäßig mehr Zucker in den schützenden Weg, der bei der Bewältigung von oxidativem Stress und beim Aufbau von Nukleotiden hilft. Von frühem Erwachsenenalter bis zur Mitte des Lebens wirkten weibliche und männliche Gehirne ähnlicher. Im hohen Alter jedoch zeigte sich eine Trennung: Männchen setzten weiter auf eine gesteigerte Glukosenutzung im energieproduzierenden Zyklus, offenbar als kompensatorische Reaktion auf das Altern, während Weibchen einen deutlichen Rückgang zeigten. Gleichzeitig änderten Weibchen ihren Purinstoffwechsel — von der Herstellung wichtiger Signalmoleküle wie Adenosin und verwandter Verbindungen in jüngeren Jahren hin zu ihrem Abbau im Alter. Männchen hingegen neigten dazu, diese Energie- und Signalspeicher bis ins hohe Alter zu erhalten.
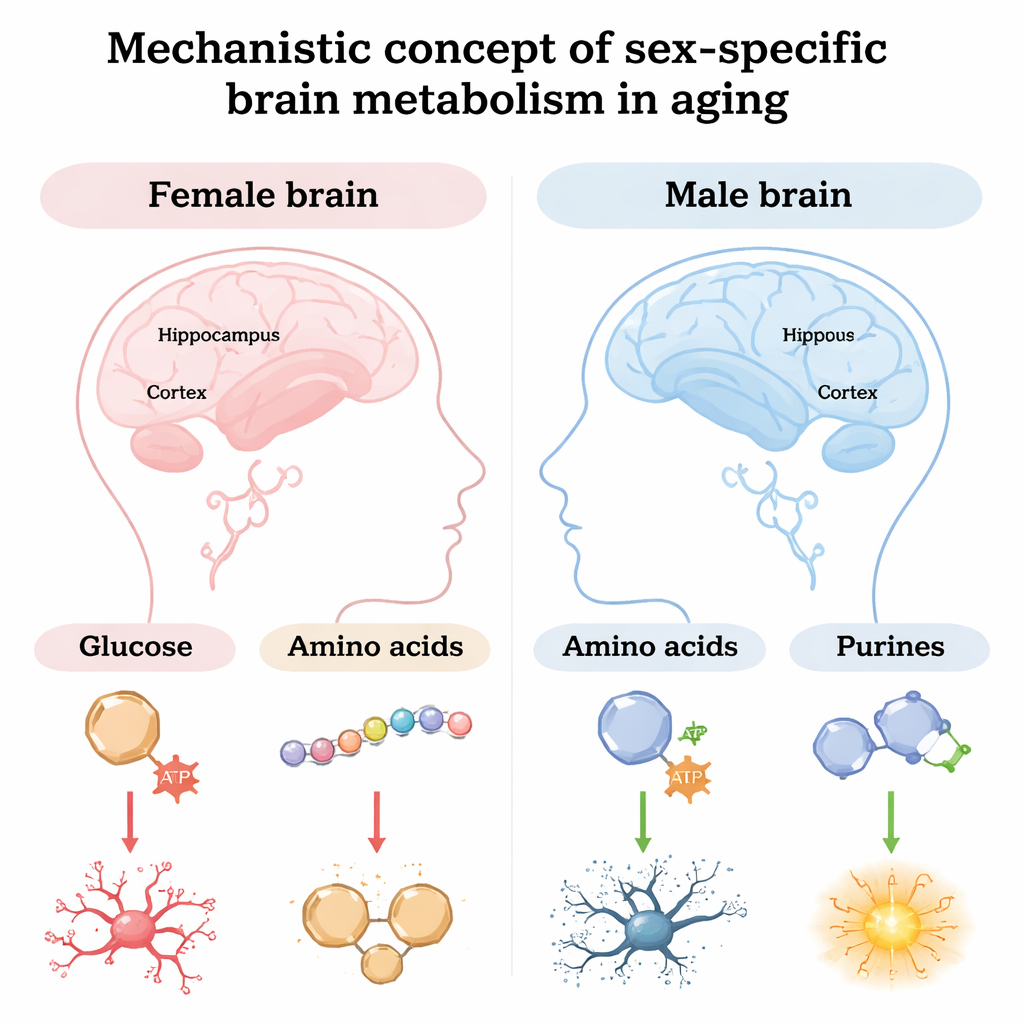
Signale, Schutz und Abfallentsorgung im alternden Gehirn
Über den Zucker hinaus kartierte das Team Hunderte weiterer kleiner Moleküle. Sie fanden ausgeprägte Geschlechtsunterschiede bei Aminosäuren, den Bausteinen von Proteinen und vielen Gehirnbotenstoffen. In der Jugend und erneut im hohen Alter zeigten Weibchen generell höhere Spiegel mehrerer Aminosäuren als Männchen. Wichtige botenstoffbezogene Moleküle, etwa solche, die von Glutamat und Aspartat abgeleitet sind, veränderten sich in einer Weise, die auf eine gesündere Myelinbildung und neuronale Unterstützung bei jungen Weibchen, aber einen Verlust schützender Moleküle und potenziellen excitotoxischen Stress bei gealterten Weibchen hindeutete. Die Studie offenbarte außerdem alters- und geschlechtsabhängige Veränderungen bei Histidin-abgeleiteten Antioxidantien und im Arginin-Harnstoff-Zyklus, der bei der Entgiftung von Ammoniak hilft. Diese Abwehr- und Abfallentsorgungssysteme schienen in der Lebensmitte besser ausbalanciert, wurden im hohen Alter jedoch gestört, besonders bei Weibchen, was ihre Anfälligkeit möglicherweise verstärkt.
Was das für gesundes Gehirnaltern bedeutet
Insgesamt zeichnen die Befunde das Bild zweier unterschiedlicher metabolischer Wege ins hohe Alter. Männliche Mäusehirne erhalten oder steigern den Zuckerabbau und den Purinaufbau im Alter, was helfen kann, Neuronen mit Energie und Signalsubstanzen zu versorgen. Weibliche Gehirne hingegen zeigen einen früheren Verlust dieser metabolischen Resilienz: abnehmende Glukosedurchströmung, ein Wechsel von Purinsynthese zu -abbau sowie größere Störungen in Aminosäure-, Antioxidantien- und Entgiftungswegen. Diese kombinierten Veränderungen stehen im Einklang mit dem stärkeren Gedächtnisverlust älterer Weibchen und könnten die höheren Demenzraten bei Frauen beim Menschen widerspiegeln. Die Arbeit unterstreicht, dass das Geschlecht nicht nur ein demografisches Merkmal ist, sondern ein biologischer Faktor, der prägt, wie das Gehirn altert — und legt nahe, dass künftige Präventions- und Behandlungsstrategien gegen kognitiven Abbau womöglich geschlechtsspezifisch angepasst werden sollten.
Zitation: Long, X., Liu, W., Chen, C. et al. Comprehensive metabolic profiling across five lifespan stages in murine hippocampus and cortex reveals sex-related variation in age-related cognitive decline. Commun Biol 9, 249 (2026). https://doi.org/10.1038/s42003-026-09527-9
Schlüsselwörter: Gehirnalterung, kognitiver Abbau, Geschlechtsunterschiede, Gehirnstoffwechsel, Alzheimer-Risiko