Clear Sky Science · de
Nimbolid mildert ARDS und Colitis ulcerosa durch Störung der Aktivierung des NLRP3-Inflammasoms
Warum die Beruhigung entgleister Entzündung wichtig ist
Viele schwere Erkrankungen — von lebensbedrohlichem Lungenversagen bis hin zu schmerzhaften Darmerkrankungen — werden nicht nur durch Erreger oder Verletzungen angetrieben, sondern durch ein überdrehtes Immunsystem des Körpers selbst. Diese Studie untersucht, ob eine natürliche Verbindung namens Nimbolid, gewonnen aus dem Neembaum, als präzise „Bremse“ auf eine mächtige Entzündungsmaschine in unseren Immunzellen wirken kann und so einen sichereren Weg eröffnen könnte, Zustände wie das akute Lungenversagen (ARDS) und Colitis ulcerosa zu behandeln.
Ein problematischer Alarm in Immunzellen
Im Zentrum dieser Erzählung steht ein molekulares Alarmsystem, das NLRP3-Inflammasom genannt wird. Wenn Immunzellen Gefahr wahrnehmen — Signale aus Infektionen, geschädigtem Gewebe oder Kristallen — kann es sich zusammenfügen wie eine Lego-Struktur aus drei Teilen: dem Sensor NLRP3, dem Adapter ASC und dem Enzym Caspase‑1. Einmal assembliert, aktiviert dieser Komplex potente Botenstoffe wie IL‑1β und IL‑18 und kann eine feurige Form des Zelltods namens Pyroptose auslösen. Zwar hilft diese Reaktion beim Beseitigen von Gefahren, doch wenn sie überaktiviert ist, trägt sie zu chronischen und akuten Erkrankungen bei, darunter Arthritis, Diabetes-Folgen, Alzheimer, ARDS und entzündliche Darmerkrankungen. Arzneimittelentwickler haben versucht, NLRP3 mit synthetischen Verbindungen zu zähmen, doch viele Kandidaten scheiterten wegen Toxizität, Nebenwirkungen oder ungünstigem Verhalten im Körper, sodass ein klarer Bedarf an sichereren und selektiveren Inhibitoren besteht.
Entdeckung eines wirksamen pflanzenbasierten Inhibitors
Die Forschenden testeten 126 natürliche Verbindungen darauf, welche die Freisetzung von IL‑1β aus Mäuse-Immunzellen am besten blockierten. Nimbolid fiel auf und reduzierte die IL‑1β-Sekretion bei den getesteten Dosen um mehr als 80 %. Weitere Experimente zeigten, dass Nimbolid die Aktivierung von Caspase‑1, die Freisetzung von IL‑1β und pyroptotischen Zelltod in mäusebasierten Knochenmarksmakrophagen stark verringerte, mit einer Wirksamkeit ähnlich dem Referenzpräparat MCC950. Wichtig ist, dass Nimbolid nicht die Freisetzung anderer Immunboten wie IL‑6 dämpfte — ein Hinweis darauf, dass es fokussiert wirkt, statt die Immunantwort allgemein herunterzufahren. Getestet gegen verschiedene Auslöser, die alle NLRP3 aktivieren — etwa ATP, Nigericin, Alumkristalle und Imiquimod — reduzierte Nimbolid konsistent die Inflammasom-Aktivität, auch in menschlichen THP‑1-Zellen. Im Gegensatz dazu blockierte es nicht zwei verwandte Inflammasome, AIM2 und NLRC4, was seine Spezifität für NLRP3 unterstreicht.
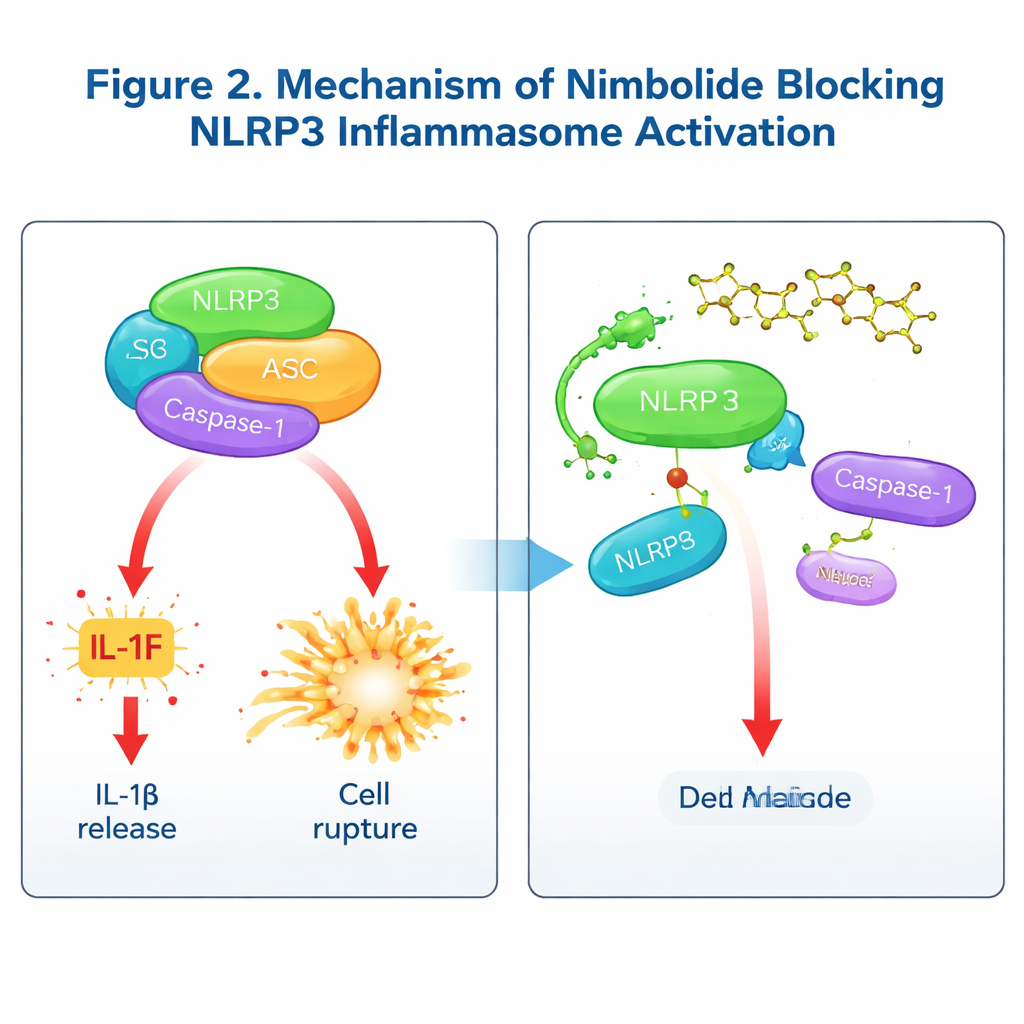
Wie Nimbolid die Entzündungsmaschine blockiert
Um zu verstehen, wie Nimbolid wirkt, prüfte das Team, ob es frühe „Priming“-Schritte über den NF‑κB-Weg stört oder die späteren Stadien, in denen das Inflammasom physisch zusammengebaut wird. Eine kurzzeitige Behandlung nach dem Priming ließ wichtige Priming-Signale und Genexpressionen unverändert, reduzierte jedoch weiterhin IL‑1β und Caspase‑1-Aktivierung — ein deutliches Zeichen, dass Nimbolid hauptsächlich den Assemblierungsschritt hemmt. Detaillierte biochemische Tests zeigten, dass Nimbolid weder Kalium- noch Kalziumflüsse, mitochondriale Schäden noch die Interaktion von NLRP3 mit seinem Helferprotein NEK7 verändert. Stattdessen stört es die entscheidende Verbindung zwischen NLRP3 und ASC, verringert die Bildung von ASC-Clustern (sogenannten Specks) und verhindert, dass NLRP3 höherstrukturelle Oligomere bildet. Bindungsassays und molekulares Modellieren zeigten, dass Nimbolid direkt an die NACHT-Region von NLRP3 an einer spezifischen Aminosäure bindet, Lys565. Wenn diese Stelle mutiert wurde, konnte Nimbolid NLRP3 nicht mehr vor Abbau schützen oder dessen Verbindung zu ASC aufbrechen, womit Lys565 als zentrales Andockziel bestätigt wurde. Bemerkenswert ist, dass andere Wirkstoffe häufig die ATPase-Aktivität von NLRP3 ins Visier nehmen, Nimbolid jedoch die Assemblierung blockiert, ohne die ATP-Nutzung zu beeinflussen — ein unabhängiger Wirkmechanismus.
Prüfung von Nimbolid in Lungen‑ und Darmerkrankungen
Als Nächstes untersuchten die Forschenden, ob dieser molekulare Effekt in Krankheitsmodellen Schutz bietet. Bei Mäusen, denen ein bakterielles Toxin zur Auslösung von ARDS verabreicht wurde, verringerte eine Gabe von Nimbolid vor dem Schädigungsereignis Gewebeschäden, Flüssigkeitsansammlungen und Proteinleckagen in den Lufträumen. Es drangen weniger Immunzellen in die Lunge ein, und die IL‑1β-Spiegel in Lungengewebe und Blut waren niedriger. Ähnliche Vorteile zeigten sich in einem Modell, bei dem das Toxin direkt in die Atemwege verabreicht wurde. In einem separaten Modell der Colitis ulcerosa, bei dem Mäuse eine chemische Substanz zum Trinken erhielten, die den Dickdarm schädigt, begrenzte Nimbolid Gewichtsverlust, verbesserte Stuhlkonsistenz und Blutungswerte, bewahrte die Dickdarmlänge und verringerte mikroskopische Zeichen von Entzündung und Gewebeerosion sowie IL‑1β im Darm. Entscheidenderweise waren genetisch veränderte Mäuse ohne NLRP3 bereits weniger krank, und Nimbolid brachte keinen zusätzlichen Nutzen, was bestätigt, dass seine Schutzwirkung von der Blockade von NLRP3 abhängt.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten ist die zentrale Erkenntnis: Nimbolid wirkt wie eine kluge Bremse an einem der stärksten entzündlichen Schalter des Körpers. Indem es sich an eine präzise Stelle von NLRP3 heftet und verhindert, dass das Inflammasom zusammenschnappt, beruhigt es übermäßige Entzündungen in Lunge und Darm, ohne die Immunabwehr breit zu unterdrücken. Zwar muss Nimbolid selbst noch in Punkten wie Stabilität und Darreichung verbessert werden, bevor es als Arzneimittel infrage kommt, doch diese Arbeit positioniert es als vielversprechenden Ausgangspunkt — und als Bauplan — für die Entwicklung der nächsten Wirkstoffgeneration gegen NLRP3-getriebene Erkrankungen wie ARDS und Colitis ulcerosa.
Zitation: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Schlüsselwörter: nimbolid, NLRP3-Inflammasom, Entzündung, akutes Lungenversagen (ARDS), Colitis ulcerosa