Clear Sky Science · de
Epigenomweite Assoziationsstudie zirkulierender Interleukin-6 verbindet DNA-Methylierung mit immunometabolischer und entzündlicher Gesundheit
Warum das für die Alltagsgesundheit wichtig ist
Chronische, niedriggradige Entzündungen beeinflussen stillschweigend unser Risiko für Krankheiten wie Typ-2-Diabetes, Herzkrankheiten und entzündliche Darmerkrankungen. Ein zentraler Akteur in diesem Prozess ist ein Signalprotein im Blut namens Interleukin‑6 (IL‑6). Diese Studie stellt eine grundlegende Frage: Wie interagiert IL‑6 mit unserem Epigenom — den chemischen Markierungen auf der DNA, die die Genaktivität steuern — und was bedeutet das für unsere langfristige Gesundheit?
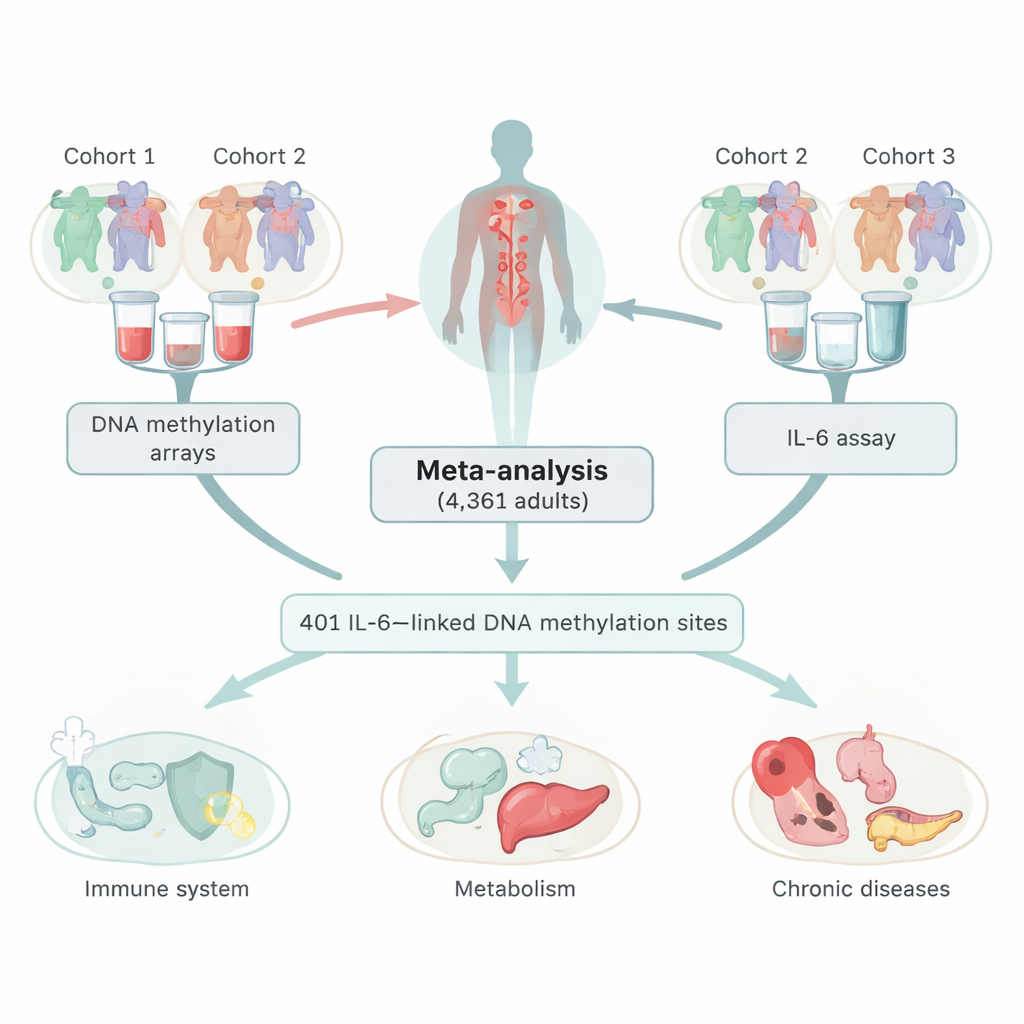
Blick auf chemische Marker auf der DNA
Die Forschenden kombinierten Daten aus drei großen europäischen Studien und betrachteten 4.361 Erwachsene, die Blutproben zur Verfügung stellten. In diesen Proben maßen sie sowohl IL‑6-Spiegel als auch DNA-Methylierung, eine verbreitete chemische Markierung auf der DNA, die Gene hoch- oder herunterregeln kann, ohne den genetischen Code zu verändern. Durch das Absuchen von über 400.000 Stellen im Genom identifizierten sie 401 Positionen, an denen die Methylierungslevel mit der Menge an zirkulierendem IL‑6 korrelierten. Die meisten dieser Stellen zeigten ein inverses Muster: höhere IL‑6-Werte gingen mit geringerer Methylierung an diesen Orten einher. Das Team überprüfte sorgfältig, dass diese Zusammenhänge nicht einfach Nebeneffekte von Rauchen, Unterschieden in Blutzelltypen oder einem anderen Entzündungsmarker, dem C‑reaktiven Protein (CRP), waren.
Verbindung von Entzündung mit Stoffwechsel und Krankheit
Als Nächstes prüften die Autorinnen und Autoren, ob diese IL‑6-assoziierten DNA-Stellen mit Signalen aus anderen großen epigenetischen Studien überlappten. Sie fanden eine starke Anreicherung für Merkmale mit entzündlichem oder metabolischem Anteil, darunter Body-Mass-Index, Blutfette, Blutdruck, Blutzucker, Typ-2-Diabetes, chronische Nierenerkrankung sowie psychiatrische und stressbedingte Erkrankungen. Viele der gleichen Methylierungsstellen waren zuvor bereits mit CRP in Verbindung gebracht worden, doch die Muster deuteten darauf hin, dass IL‑6 und CRP jeweils teilweise unterschiedliche epigenetische Signaturen tragen. Anders gesagt: Die mit IL‑6 assoziierten chemischen Markierungen sind nicht nur eine Kopie derer, die mit CRP verbunden sind, und können zusätzliche Informationen über den entzündlichen und metabolischen Zustand einer Person liefern.
Wo im Genom die Aktivität stattfindet
Um zu verstehen, was diese Methylierungsstellen bewirken könnten, kartierten die Forschenden diese auf bekannte regulatorische Regionen des Genoms. Sie fanden, dass IL‑6-assoziierte Stellen sich in aktiven Kontrollelementen wie Enhancern — DNA-Abschnitten, die Gene an- und ausschalten helfen — konzentrierten, statt in ruhigen Regionen. Diese Stellen lagen außerdem nahe Bindungssequenzen für Transkriptionsfaktoren, die IL‑6 und Stressantworten direkt regulieren, darunter NF‑κB, Atf4, CHOP und Nrf2. Durch die Kombination der Methylierungsdaten mit großen Genexpressionsdatensätzen verknüpften die Forschenden über 400 Gene mit den IL‑6-bezogenen Stellen. Viele dieser Gene stehen im Zentrum immuner und metabolischer Steuerung, darunter SOCS3, IL6R, AIM2, IFI16, MTOR und RORC, und sind an Signalwegen beteiligt, die Aktivierung und Energieverbrauch in einer spezialisierten T‑Zell‑Untergruppe (Th17-Zellen) antreiben, die bei chronischen Entzündungskrankheiten eine Rolle spielt.
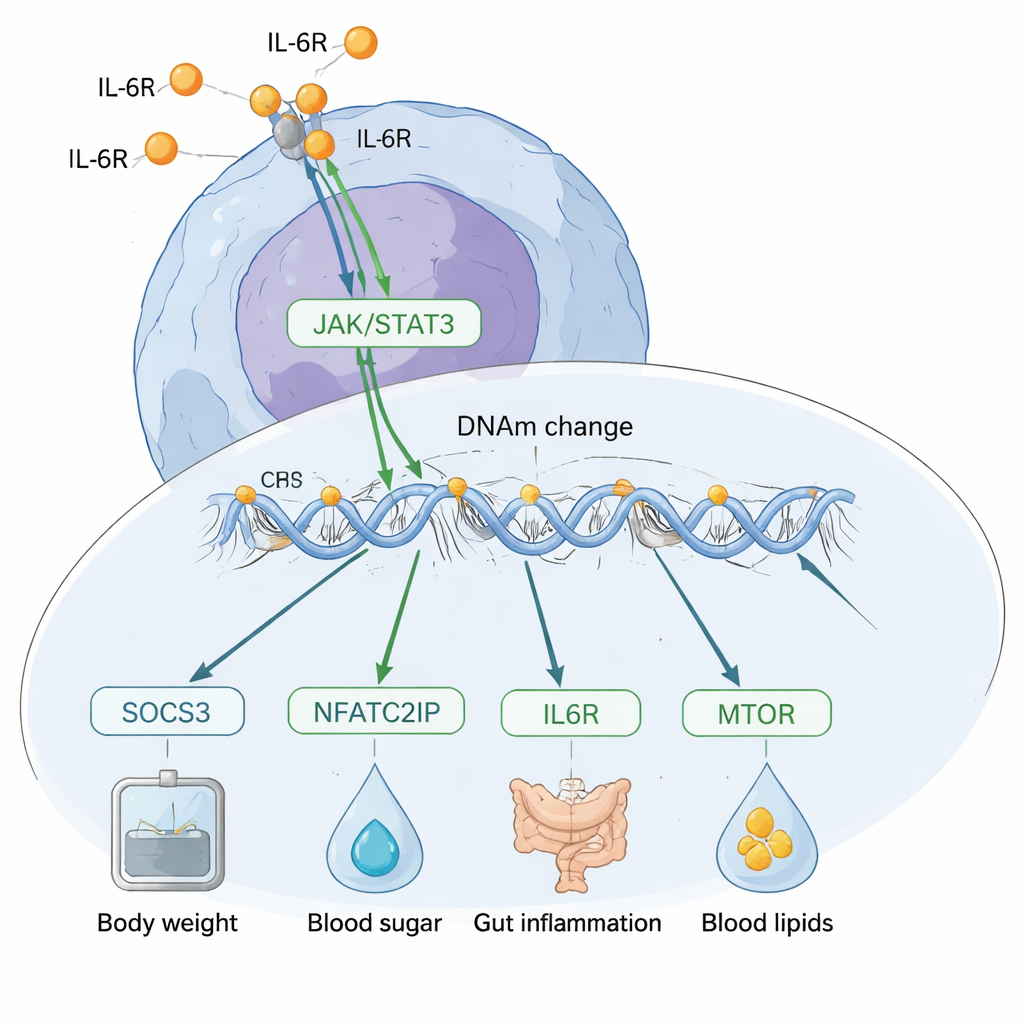
In welche Richtung läuft Ursache und Wirkung?
Eine große Herausforderung besteht darin herauszufinden, ob DNA‑Methylierung Veränderungen in IL‑6 verursacht, oder ob IL‑6 die Methylierung umgestaltet. Das Team nutzte mehrere genetische Methoden, um diese Richtung zu untersuchen. Über das Genom hinweg unterstützten ihre „Triangulations“-Analysen ein Modell, in dem IL‑6 größtenteils Änderungen in der DNA‑Methylierung antreibt, statt umgekehrt. Sie zoomten dann auf spezifische Stellen und fanden, dass Methylierungsänderungen nahe dem SOCS3-Gen offenbar die Wirkung von IL‑6 auf Risikofaktoren wie Körpergewicht, Cholesterin, CRP-Spiegel und entzündliche Darmerkrankungen vermitteln. Im Gegensatz dazu zeigte eine auffällige Stelle in der Nähe eines Genregulators namens NFATC2IP Hinweise darauf, die IL‑6-Produktion selbst zu beeinflussen und schien ebenfalls mehrere Zustände wie Body‑Mass‑Index, Typ‑2‑Diabetes und Darmentzündungen zu beeinflussen.
Was das für Prävention und Behandlung bedeutet
Für eine nichtfachliche Leserschaft ist die Kernaussage, dass IL‑6 und epigenetische Markierungen auf der DNA eng verflochten sind und viele häufige Erkrankungen berühren. Meist hinterlässt IL‑6 einen chemischen „Fußabdruck“ im Genom, besonders in Immunzellen, der pro‑entzündliche Zustände markiert und möglicherweise stabilisiert. An einigen wenigen Schlüsselstellen hingegen könnte Methylierung dazu beitragen, wie viel IL‑6 produziert wird und wie stark Immunwege reagieren. Diese Befunde machen DNA‑Methylierungsmuster zu vielversprechenden blutbasierten Indikatoren für entzündliche und metabolische Gesundheit und legen nahe, dass gezielt veränderte epigenetische Veränderungen — insbesondere rund um Gene wie SOCS3 und NFATC2IP — eines Tages die IL‑6‑blockierenden Medikamente bei der Prävention oder Behandlung chronischer Krankheiten ergänzen könnten.
Zitation: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Schlüsselwörter: Interleukin-6, DNA-Methylierung, Entzündung, metabolische Erkrankung, Epigenetik