Clear Sky Science · de
MAT2A verstärkt die PARN-Transkription über SRF, um die Glykolyse zu beschleunigen und das maligne Fortschreiten beim Osteosarkom voranzutreiben
Warum diese Studie zu Knochenkrebs wichtig ist
Osteosarkom ist die häufigste Form von Knochenkrebs bei Kindern und Jugendlichen, und die Behandlungsoptionen haben sich seit Jahrzehnten kaum verändert. Viele junge Patientinnen und Patienten haben nach wie vor schlechte Aussichten, insbesondere wenn der Krebs metastasiert oder gegen Chemotherapie resistent ist. Diese Studie enthüllt ein bisher übersehenes "Master-Schalter"-Protein namens MAT2A, das Osteosarkomzellen beim Wachstum unterstützt, ihren Energiestoffwechsel umprogrammiert und aggressive Tumoren bildet — und zeigt, dass ein auf MAT2A zielender Wirkstoff diese Tumoren in Labormodellen verlangsamen oder verkleinern kann.
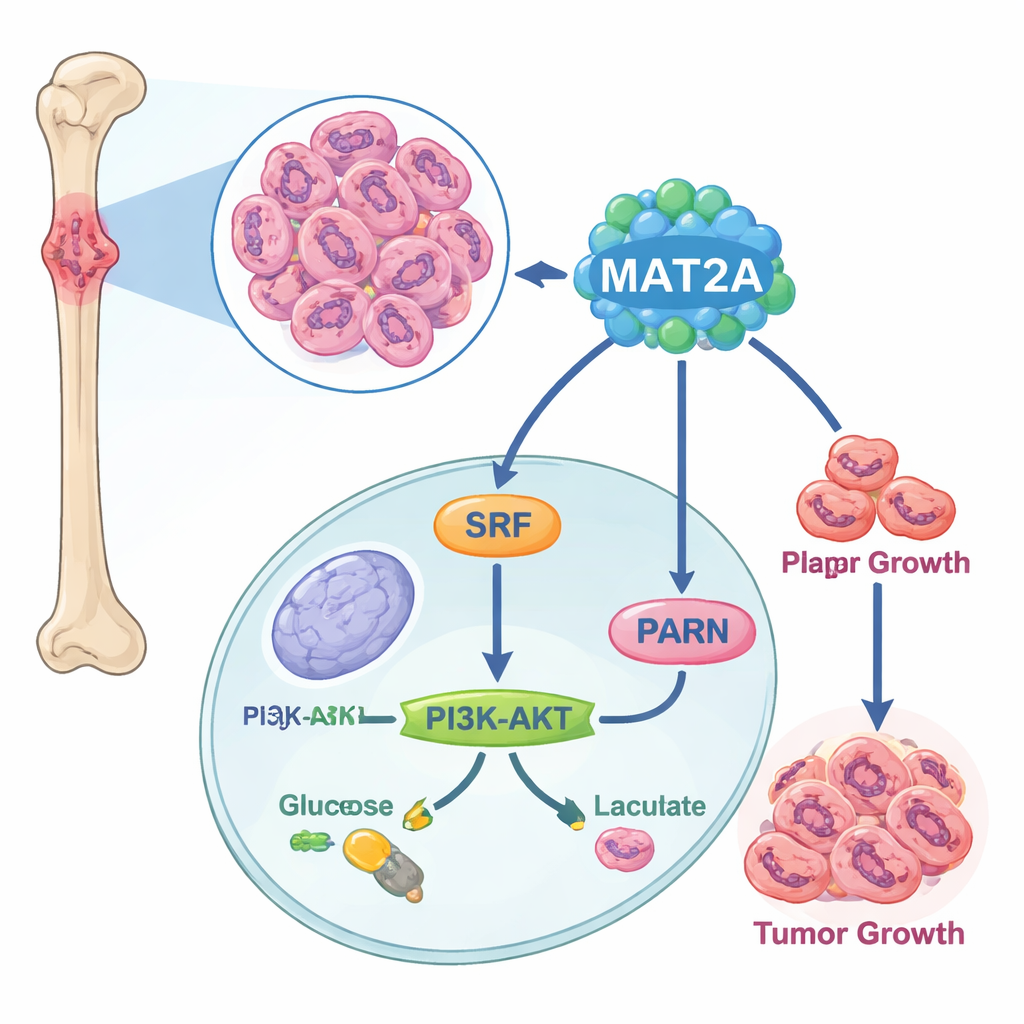
Ein versteckter Motor in Tumorzellen
Die Forschenden begannen damit, Knochenkrebsproben mit normalem Knochengewebe auf Einzelzellebene zu vergleichen. Sie fanden, dass das Osteosarkomgewebe mehr tumorbildende Zellen und weniger Immunzellen enthält und dass ein Gen im Besonderen — MAT2A — in Krebszellen ungewöhnlich aktiv war. Analysen öffentlicher Krebsdatenbanken und von im Labor gezüchteten Zelllinien bestätigten, dass die MAT2A-Spiegel im Osteosarkom deutlich höher sind als in gesundem Knochengewebe und dass Patientinnen und Patienten mit erhöhtem MAT2A tendenziell weiter fortgeschrittene Erkrankungen und Lymphknotenbefall aufwiesen. Das rückte MAT2A in den Mittelpunkt als möglichen Treiber der Krankheit statt als passiven Begleiter.
MAT2A herunterzufahren verlangsamt das Tumorwachstum
Um zu prüfen, wie wichtig MAT2A wirklich für das Tumorverhalten ist, nutzte das Team genetische Werkzeuge, um MAT2A in Osteosarkomzelllinien zu reduzieren. Wurde MAT2A ausgeschaltet, teilten sich die Krebszellen langsamer und gingen eher in programmierte Zellsterblichkeit über. Bei Mäusen, die mit diesen veränderten Zellen implantiert wurden, wuchsen die Tumoren deutlich langsamer und blieben wesentlich kleiner, obwohl das Körpergewicht der Tiere stabil blieb. Diese Experimente zeigten, dass Osteosarkomzellen stark von MAT2A für ihr Überleben und ihre Tumorbildungsfähigkeit abhängig sind.
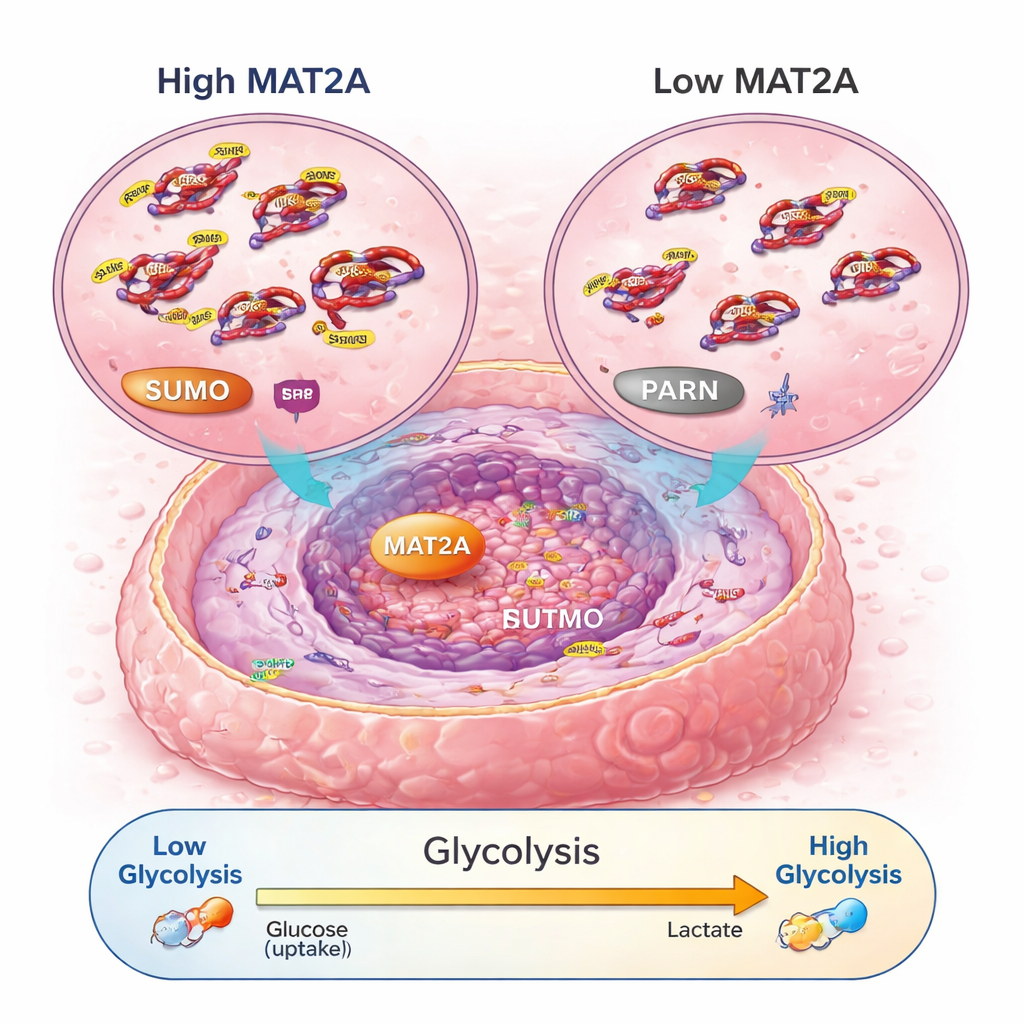
Eine Signalkette, die den Zellenergieverbrauch anheizt
Bei tiefergehenden Untersuchungen entdeckten die Wissenschaftler, dass MAT2A mehr tut als seine normale metabolische Rolle. Im Zellkern bindet es an einen Transkriptionsfaktor namens SRF und trägt durch Förderung einer chemischen Markierung namens SUMO dazu bei, SRF stabil und aktiv zu halten. SRF schaltet seinerseits ein Gen namens PARN ein, das dann den bekannten PI3K–AKT-Signalweg aktiviert und die Maschinerie der aeroben Glykolyse hochfährt — ein schnelles, aber ineffizientes Energiesystem, das Krebszellen bevorzugen. Wurde MAT2A reduziert, produzierten die Krebszellen weniger ATP (ihre Energieeinheit), nahmen weniger Glukose auf, bildeten weniger Milchsäure und kehrten eher zur ruhigen, sauerstoffabhängigen Atmung zurück. Die Störung von PARN oder AKT konnte die wachstumsfördernden und glykolysesteigernden Effekte von MAT2A aufheben, womit bestätigt wurde, dass diese Kette — MAT2A zu SRF zu PARN zu PI3K–AKT — als zentrales Energie- und Wachstumsnetzwerk im Osteosarkom wirkt.
Eine unkonventionelle Rolle und ein angreifbarer Zielpunkt
Bemerkenswerterweise unterstützte auch eine Variante von MAT2A ohne seine normale Enzymaktivität weiterhin die Stabilität von SRF und die Aktivierung von PARN, was bedeutet, dass diese krebserzeugende Rolle nicht von seiner üblichen chemischen Reaktion abhängt. Stattdessen fungiert MAT2A eher als Gerüst, das andere Proteine organisiert. Das hat praktische Konsequenzen: Medikamente müssen nicht zwingend das katalytische Zentrum blockieren, um Tumoren zu schwächen. Die Forschenden testeten einen kleinen Molekülinhibitor namens FIDAS-5, der auf MAT2A abzielt, sowohl in Zellkulturen als auch in Mausmodellen. Die Behandlung verringerte nukleäres SRF, senkte PARN- und PI3K–AKT-Signale, dämpfte die Glykolyse, verlangsamte das Zellwachstum und löste den Zelltod bei Krebszellen aus. Bei Mäusen verkleinerte oder verlangsamte FIDAS-5 Tumoren ohne auffälligen Gewichtsverlust, was auf verträgliche Nebenwirkungen in diesem Setting hindeutet.
Was das für Patientinnen, Patienten und zukünftige Therapien bedeutet
Für Nicht-Spezialistinnen und Nicht-Spezialisten ist die Kernbotschaft: Osteosarkomzellen sind auf MAT2A angewiesen, um ihre Wachstumsprogramme und ihre "Zuckerverbrennungs"-Maschinerie auf Hochtouren zu halten. Indem MAT2A zentrale Kontrollproteine stabilisiert und eine Signalkette verstärkt, beschleunigt es das Tumorwachstum und die Aggressivität. Das Blockieren dieses Proteins — entweder durch gentechnische Methoden oder durch einen Wirkstoff wie FIDAS-5 — kappt diese Unterstützung, zwingt die Krebszellen, langsamer zu werden, weniger hektisch Energie zu verbrauchen und schließlich zu sterben. Obwohl noch viel Arbeit nötig ist, bevor solche Behandlungen in die Klinik gelangen, positioniert diese Studie MAT2A als vielversprechendes neues Ziel im Kampf gegen Knochenkrebs und eröffnet einen möglichen Weg zu präziseren und weniger toxischen Therapien für junge Patientinnen und Patienten.
Zitation: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Schlüsselwörter: Osteosarkom, MAT2A, Krebsstoffwechsel, PI3K-AKT-Signalweg, gezielte Therapie