Clear Sky Science · de
Computationale Analyse der Epitope‑Heterogenität in Immunfärbungen aus Antikörper‑Verdünnungsserien
Warum die Qualität der Antikörperfärbung wichtig ist
Vom Aufspüren von Krebszellen bis zur Diagnose von Infektionen stützt sich die moderne Biologie stark auf Antikörper, die bestimmte Moleküle in Zellen „aufleuchten“ lassen. Dennoch kämpfen viele Labore stillschweigend mit einem hartnäckigen Problem: Färbungen, die zu schwach, zu verrauscht oder schlicht irreführend sind. Diese Arbeit stellt eine praktische, computerbasierte Methode vor, um aus einer routinemäßigen Antikörper‑Verdünnungsserie mehr Informationen zu gewinnen. Sie hilft Forschenden, ihre Färbungen so zu optimieren, dass Bilder sauberer werden, Messungen vertrauenswürdiger sind und sich sogar neue Wege auftun, mehrere Ziele in einem einzigen FarbkanaI zu markieren. 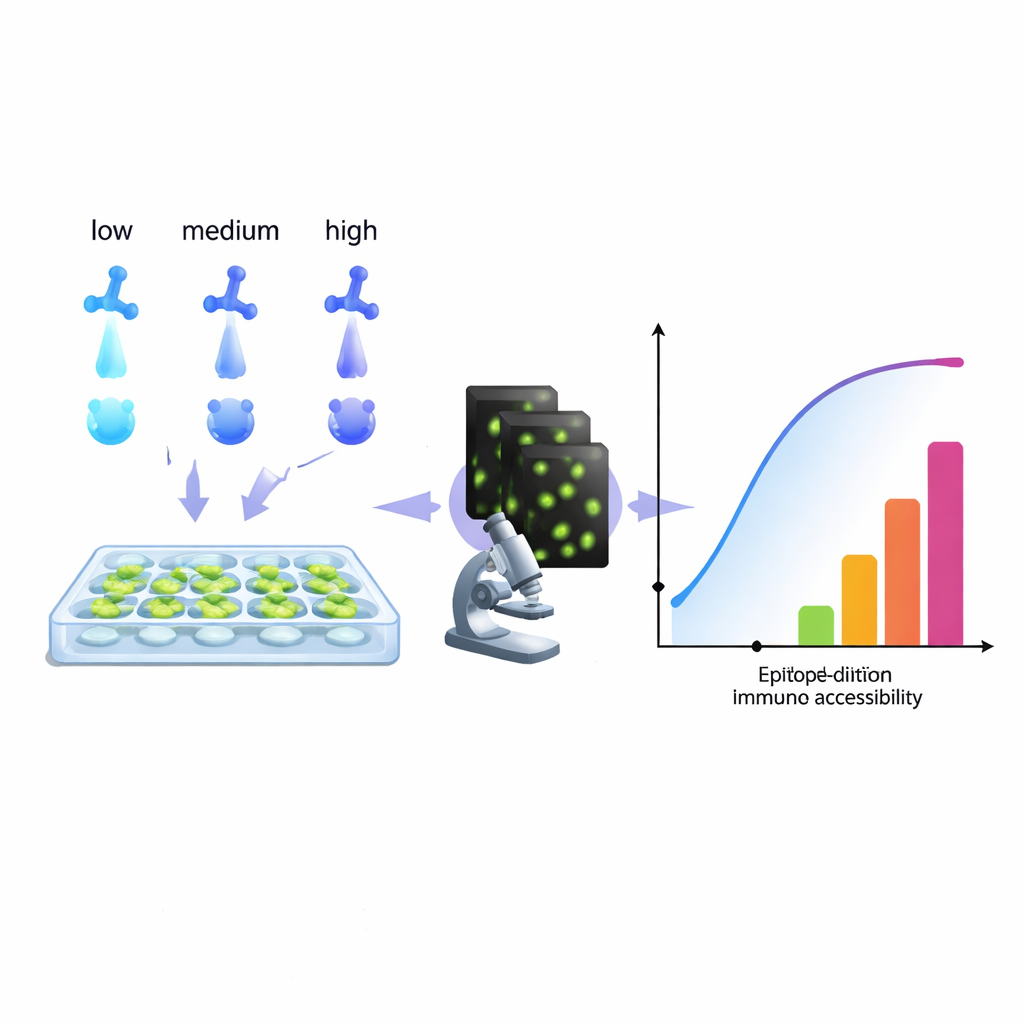
Wie Forschende üblicherweise Antikörperfärbungen justieren
Wenn Forschende ein Immunfärbeexperiment aufsetzen, wählen sie meist eine Antikörperkonzentration anhand des Datenblatts, probieren ein paar Verdünnungen aus und entscheiden sich für diejenige, die „gut aussieht“. Hinter den Kulissen bestimmen jedoch zahllose feine Faktoren — Proteinform, Dichte in der Zelle, pH und wie flexibel der Antikörper sich hineinmanövrieren kann — ob ein Antikörper haften bleibt oder ausgewaschen wird. Traditionelle Methoden zur Messung der Antikörperbindung, etwa Oberflächenplasmonresonanz, funktionieren am besten bei gereinigten Proteinen auf künstlichen Oberflächen, nicht bei dicht gepackten Zellen oder Geweben. Das bedeutet, dass die gelieferten Werte nicht unbedingt dem biologischen System entsprechen, in dem der Antikörper tatsächlich eingesetzt wird. Infolgedessen wählen Labore möglicherweise unbewusst Konzentrationen, die den unscharfen Hintergrund verstärken oder wichtige, aber weniger zugängliche Ziele verdecken.
Aus einfachen Verdünnungsserien „Zugänglichkeitskarten“ erstellen
Die Autorinnen und Autoren schlagen einen anderen Ansatz vor: Behandle eine standardmäßige Antikörper‑Verdünnungsserie als reichhaltigen Datensatz und passe sie mit einem Modell an, das widerspiegelt, was die Mikroskopie tatsächlich erfasst — Antikörper, die auch nach wiederholtem Waschen gebunden bleiben. Indem die Methode analysiert, wie das Signal mit steigender Konzentration wächst, rekonstruiert der Algorithmus ein „Zugänglichkeits‑Histogramm“. Anstatt zu versuchen, reine chemische Bindungskonstanten zu isolieren, gruppiert dieses Histogramm Zielstellen in technische „Epitopklassen“ je nachdem, wie leicht sie unter realen Bedingungen zu färben sind. Ein biologisches Epitop kann in mehrere Klassen fallen, wenn es etwa an einer Stelle einer Zelle leicht erreichbar ist und in einer überfüllten Region schwerer zugänglich. Entscheidender Vorteil: Diese Methode arbeitet direkt mit dem Mikroskopausgang, ohne gereinigte Proteine oder zusätzliche Hardware zu benötigen. Jedes Labor, das eine Verdünnungsserie durchführen und Fluoreszenz quantifizieren kann, kann prinzipiell solche Histogramme erstellen. 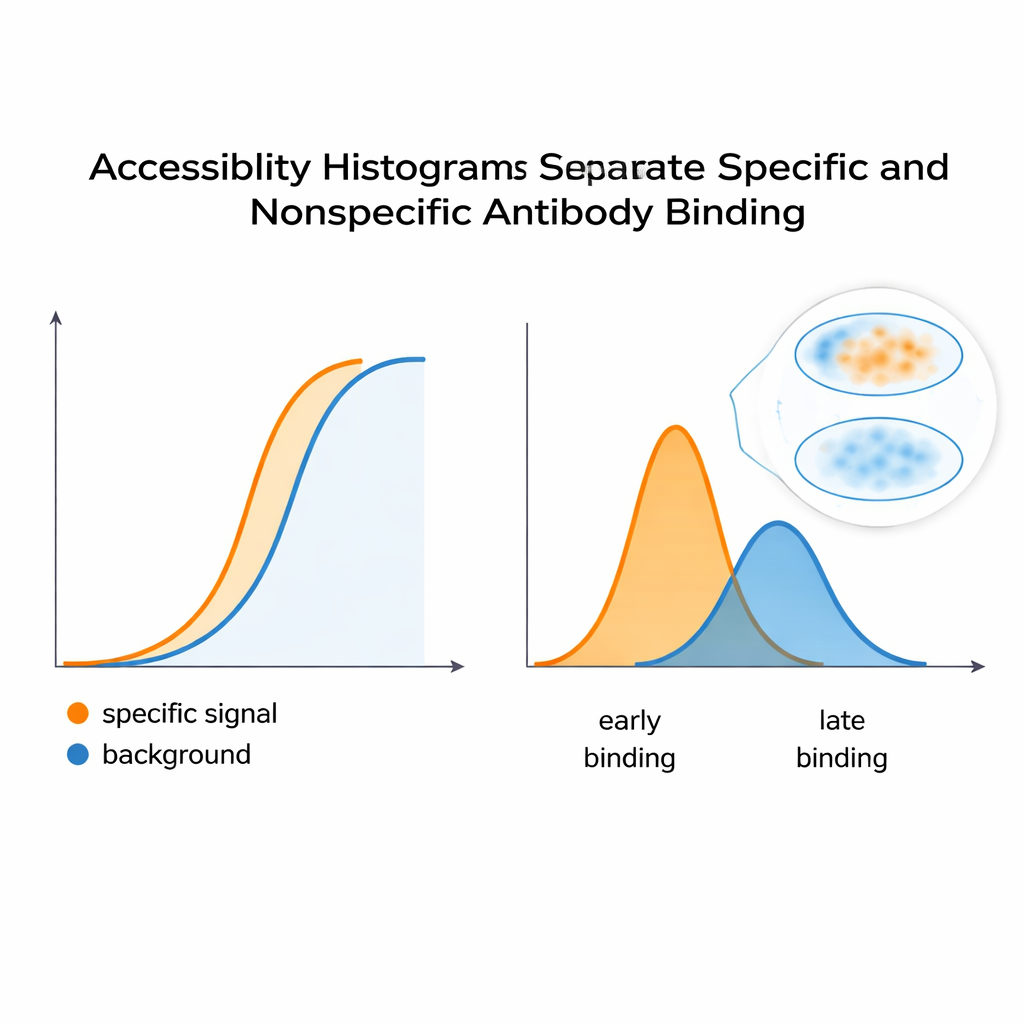
Reales Signal vom Hintergrund trennen
Um zu prüfen, ob diese Histogramme das Färbeverhalten wirklich erfassen, bauten die Forschenden ein kontrolliertes System mit HeLa‑Zellen und zwei monoklonalen Antikörpern auf: einem, das ein gewünschtes, spezifisches Signal nachahmt, und einem anderen, das wie unerwünschter Hintergrund wirkt. Gemischt zeigte die kombinierte Fluoreszenzkurve eine einzige, glatte Antwort — nichts deutete offensichtlich auf zwei verschiedene Beiträge hin. Die computationale Analyse teilte diese Kurve jedoch in separate Peaks im Zugänglichkeits‑Histogramm auf und zeigte damit mindestens zwei zugrunde liegende Epitopklassen. Eine ähnliche Strategie bei einem Antikörper, der eine formabhängige Stelle an einer regulatorischen PKA‑Untereinheit erkennt, zeigte, dass Änderungen in der Proteinkonformation — ausgelöst durch das Molekül cAMP — die Verteilung der zugänglichen Epitope verschoben. Das deutet darauf hin, dass die Methode signalisieren kann, wenn sich Proteinstrukturen öffnen oder schließen und dadurch die Bindbarkeit von Antikörpern in Zellen verändern.
Bessere Verdünnungen wählen und mehr mit einer Farbe färben
Da jeder Peak im Zugänglichkeits‑Histogramm hauptsächlich über einen bestimmten Konzentrationsbereich beiträgt, nutzen die Autorinnen und Autoren diese Peaks als Orientierung, um „Sweet‑Spot“‑Verdünnungen auszuwählen. Niedrig zugängliche Peaks, die erst bei sehr hohen Antikörperniveaus erscheinen, beinhalten wahrscheinlich unspezifische Bindung, während frühe Peaks oft das beabsichtigte Ziel widerspiegeln. Durch Modellierung, wie einzelne Peaks die gesamte Dosis‑Antwort‑Kurve aufbauen, kann das Team Verdünnungen vorschlagen, die das spezifische Signal maximieren, bevor problematische Peaks einsetzen — manchmal deutlich verdünnter als Herstellerempfehlungen. Sie erweitern diese Idee zu einer eleganten Form des „computationalen Multiplexings“: Indem dieselbe fixierte Probe mehrfach mit sorgfältig gewählten Konzentrationen gefärbt, nach jeder Runde abgebildet und frühere Bilder von späteren subtrahiert werden, isolieren sie Signale, die mit verschiedenen Zugänglichkeitsklassen verknüpft sind, und trennen so effektiv mehrere Ziele innerhalb eines einzigen Fluoreszenzkanals.
Was das für die tägliche Laborarbeit bedeutet
Einfach gesagt verwandelt diese Arbeit einen routinemäßigen Troubleshooting‑Schritt — das Durchführen einer Antikörper‑Verdünnungsserie — in ein quantitatives Werkzeug. Die Zugänglichkeits‑Histogramme helfen Forschenden, verborgene Komplexität in ihren Färbungen zu erkennen, Verdünnungen zu wählen, die irreführenden Hintergrund reduzieren, und in manchen Fällen überlappende Signale zu trennen, ohne zusätzliche fluoreszierende Marker zu benötigen. Zwar ist das zugrunde liegende Modell bewusst einfach gehalten und erfasst nicht jedes molekulare Detail, doch es ist so konzipiert, dass es leicht zu verwenden und robust gegenüber realen Daten ist. Bei breiter Anwendung könnte dieser Ansatz Antikörper‑basierte Techniken — von grundlegender Bildgebung bis zu diagnostischen Assays — zuverlässiger, aussagekräftiger und weniger vom Trial‑and‑Error abhängig machen.
Zitation: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Schlüsselwörter: Antikörperfärbung, Immunfluoreszenz, Epitopzugänglichkeit, Dosis‑Antwort, computationales Multiplexing