Clear Sky Science · de
Strategische Fortschritte für kryo‑EM-Strukturstudien kleiner (<100 kDa) GPCRs
Warum winzige Zellschalter für die Medizin wichtig sind
Ein Großteil der modernen Medizin wirkt, indem er winzige Schalter in unseren Zellmembranen anstößt — die sogenannten G-Protein-gekoppelten Rezeptoren (GPCRs). Diese Schalter erkennen Hormone, Gerüche und Arzneistoffe; etwa ein Drittel aller zugelassenen Medikamente wirkt über sie. Um sicherere und gezieltere Wirkstoffe zu entwickeln, benötigen Wissenschaftler detaillierte 3D-Aufnahmen dieser Rezeptoren, besonders ihrer „ausgeschalteten“ oder inaktiven Formen, auf die viele Medikamente gezielt wirken. Dieser Artikel erklärt, wie Forschende lernen, einige der kleinsten GPCRs mit Kryo-Elektronenmikroskopie (kryo‑EM) sichtbar zu machen — einer leistungsfähigen Bildgebungsmethode, die Moleküle in nahezu natürlichem, eingefrorenem Zustand darstellt.
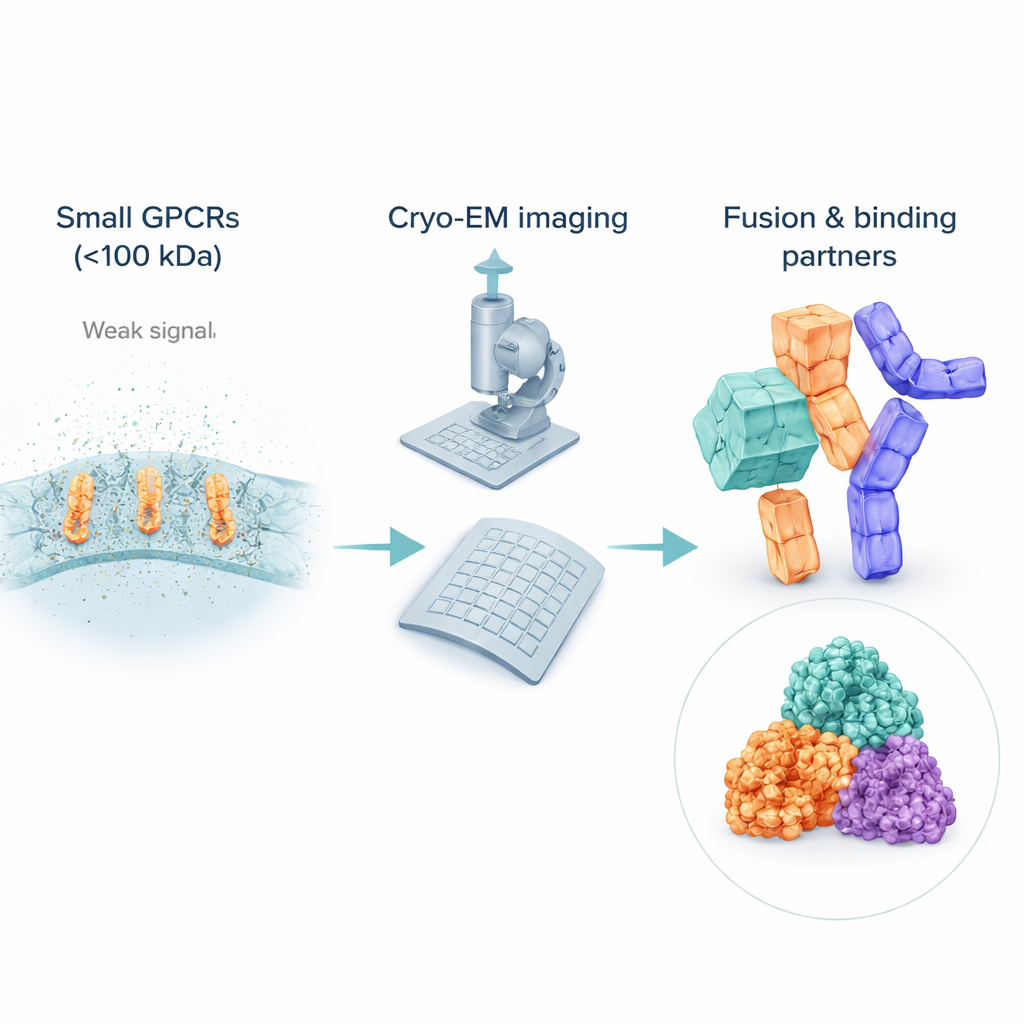
Die Herausforderung, sehr kleine Rezeptoren zu sehen
Obwohl die kryo‑EM die strukturelle Biologie revolutioniert hat, fällt ihr der Umgang mit kleinen, flexiblen Molekülen weiterhin schwer. Viele inaktive GPCRs wiegen deutlich weniger als 100 Kilodalton, was es schwierig macht, sie in verrauschten Aufnahmen zu erkennen und auszurichten. Um sie löslich zu halten, umgeben Forschende diese Rezeptoren mit Detergenzbläschen oder Lipidmimetika, die für den Elektronenstrahl oft „größer“ erscheinen als der Rezeptor selbst und das Signal des interessierenden Proteins überlagern. Im Gegensatz zu aktiven Rezeptoren, die an sperrige Partner wie G-Proteine gebunden sind, fehlen inaktiven GPCRs oft auffällige Außenmerkmale, sodass Computersysteme Probleme haben, viele Bilder zu einem scharfen 3D-Modell zu mitteln. Deshalb stammen die meisten inaktiven GPCR-Strukturen noch aus älteren Röntgenmethoden, wodurch für kryo‑EM eine Lücke genau dort entsteht, wo viele Medikamente ansetzen.
Rezeptoren durch eingebaute Helfer aufwerten
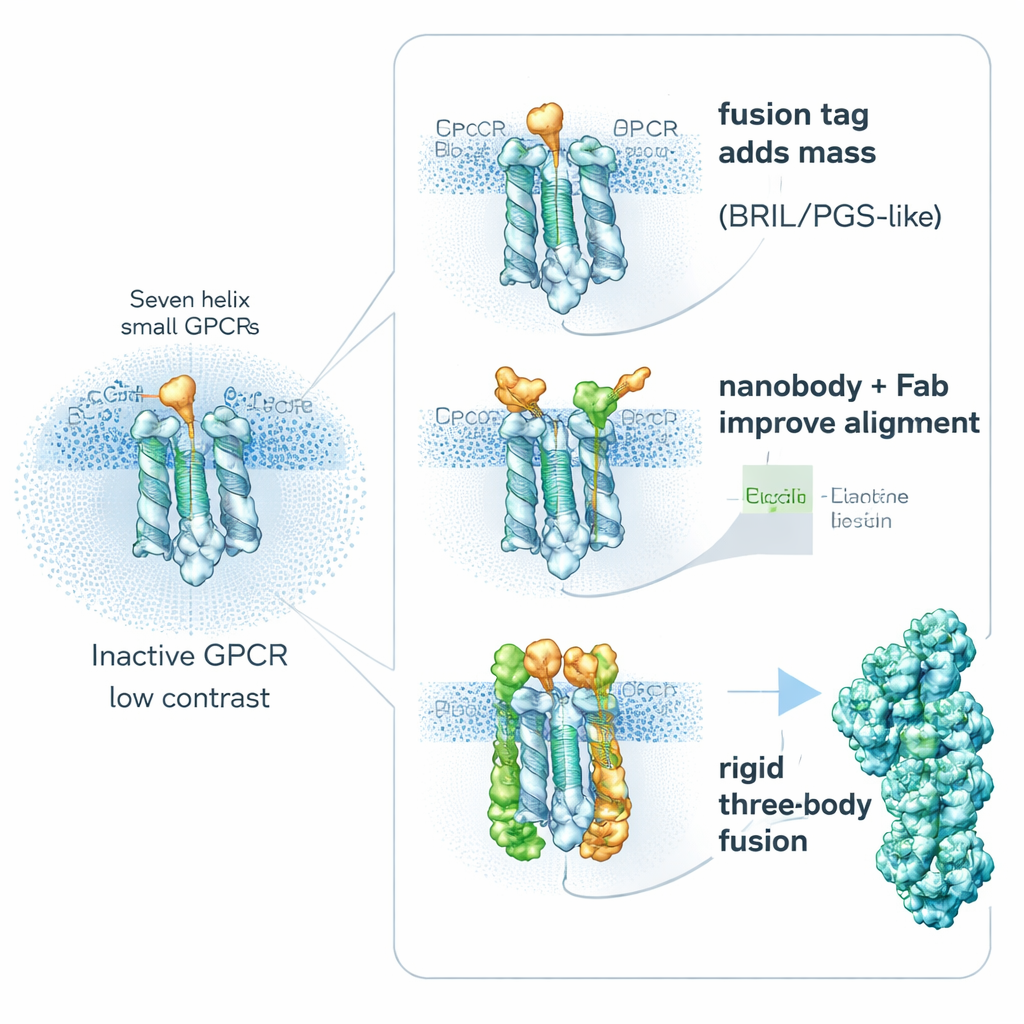
Eine zentrale Strategie ist überraschend einfach: den Rezeptor absichtlich „schwerer“ machen. Forschende fusionieren genetisch kleine, stabile Helferproteine an flexible Bereiche von GPCRs, um deren Größe und Steifigkeit zu erhöhen, ohne die wichtigen Wirkstoffbindungsstellen zu blockieren. Beliebte Helfer sind BRIL (ein Vier-Helix-Bündel), PGS (ein thermostabiler Enzymfragment) und ein größeres klammerähnliches Protein wie Calcineurin. Diese Fusionspartner werden oft in eine bewegliche innere Schleife eingesetzt, die zwei Helices verbindet. Durch das Versteifen dieses Bereichs reduzieren sie die Unschärfe durch molekulare Bewegung und liefern erkennbare Formen, die der Bildausrichtungssoftware helfen. Studien zeigen, dass die genaue Position und Orientierung des Fusionsstücks über Erfolg oder Misserfolg eines Projekts entscheiden kann: Bei einem Rezeptor verbesserte eine anders platzierte PGS-Markierung die Auflösung von unscharfen 6 Å auf deutlich klarere 3,7 Å.
Antikörper und Designer-Binder als Griffe verwenden
Ein zweiter Weg vermeidet große Fusionen am Rezeptor selbst und setzt stattdessen hochaffine „Griffe“ von außen an. Winzige Antikörperfragmente namens Nanobodies und verwandte Binder lassen sich gegen inaktive GPCRs erzeugen und an flexible innere Schleifen anheften. Ein herausragendes Beispiel ist Nanobody‑6, das zunächst als Sensor für einen Opioidrezeptor geschaffen wurde und mit geringen Anpassungen zur Stabilisierung mehrerer anderer GPCRs in ihren inaktiven Formen wiederverwendet werden konnte. Weil es außerhalb der Mitte bindet, liefert es jedem Partikel einen eindeutigen Orientierungshinweis und macht die Bildmittelung verlässlicher. Forschende erweitern dieses Prinzip oft um eine zweite Schicht — ein normales Antikörperfragment, das den Nanobody erkennt — und schaffen so einen voluminöseren, steiferen Komplex, der in der kryo‑EM klar sichtbar ist. Andere gentechnisch entwickelte Binder, wie DARPins, können als modulare Abstandshalter oder als Verbinder zu größeren Proteinkäfigen dienen und so das Signal sehr kleiner Ziele weiter verstärken.
Klügeres Proben-Design und KI-gestützte Bildverarbeitung
Das Anfügen von Helfern oder Bindern ist nur ein Teil der Lösung. Die Übersichtsarbeit betont, dass gute Strukturen mit sorgfältig konstruierten Rezeptorkonstrukten beginnen: Abtragen schlaffer Endbereiche, Einführen stabilisierender Mutationen und der Einsatz moderner Strukturvorhersagewerkzeuge, um problematische Abschnitte zu identifizieren. Bei der Bildgebung ergänzen oder ersetzen ältere Tricks wie Phasenplatten, die den Kontrast schwacher Partikel erhöhen, zunehmend künstliche Intelligenz. Deep‑Learning‑Programme können winzige Partikel in verrauschten Mikrografen aufspüren, und neue Algorithmen sortieren Bilder in unterschiedliche Formen, wenn Rezeptoren mehrere Konformationen durchlaufen. Zusammen mit fiduziellen Helfern treiben diese Fortschritte die kryo‑EM in Richtung zuverlässiger Aufklärung von Membranproteinen voran, die früher als zu klein oder zu dynamisch galten, um sie zu untersuchen.
Was das für künftige Arzneimittel bedeutet
Der Artikel kommt zu dem Schluss, dass es keinen einzigen „magischen“ Helfer gibt, der für alle Rezeptoren funktioniert, doch ein wachsendes Werkzeugkasten aus Fusionspartnern, antikörperähnlichen Bindern und KI-getriebenen Methoden öffnet schrittweise die inaktive Landschaft der GPCRs für die kryo‑EM. Für Nichtfachleute lautet die zentrale Erkenntnis: Indem kleine Rezeptoren für das Mikroskop größer und geordneter erscheinen, können Wissenschaftler endlich detaillierte Schnappschüsse der genauen Formen gewinnen, an die viele Medikamente bevorzugt binden. Diese strukturellen Blaupausen sollten die Entwicklung von Wirkstoffen beschleunigen, die diese zellulären Schalter gezielter abschalten — oder ihre Aktivität feiner regulieren — und dabei weniger Nebenwirkungen verursachen.
Zitation: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Schlüsselwörter: G-Protein-gekoppelte Rezeptoren, Kryo-Elektronenmikroskopie, Arzneimittelentdeckung, Strukturelle Biologie, Nanobody-Gerüste